Prévention, dépistage et traitement de l’hépatite C chez les personnes détenues en France
// Prevention, screening and treatment of hepatitis C among prison inmates in France
Résumé
La prise en charge des personnes détenues infectées par le virus de l’hépatite C (VHC) s’inscrit dans un parcours de soins sanitaire et pénal complexe. L’arrivée des traitements antiviraux d’action directe (AAD) de l’infection par le VHC en permettant une guérison virale dans la plupart des cas contribue à la stratégie nationale d’élimination du VHC d’ici 2025. Un examen de la littérature et des données nationales disponibles a été effectué pour structurer un recueil d’informations dans trois régions métropolitaines (40% de la population détenue). L’épidémiologie et la prise en charge des personnes détenues sont peu documentées, avec des données anciennes. L’enquête Coquelicot a montré que la population pénitentiaire avait des pratiques associées à un fort risque de contamination par le VHC majorées dans le contexte de la détention. Le dépistage à l’entrée en détention était en 2010 de 93% (Prevacar), en 2015 et 2017 de 70% et de 72% (2 études de pratiques) et en 2016 de 56,5% (Île-de-France). La séroprévalence et la prévalence des infections VHC étaient en 2010 de 4,8% et 2,5% (Prevacar) et en 2017 de 2,9% et 1,1% (Fresnes). En l’absence de recueil national d’information de prise en charge médicale du VHC, l’enquête du CNS a montré que les parcours étaient hétérogènes, avec une cascade d’accès au traitement de moins d’une personne détenue sur 2, l’insuffisance de dépistage étant l’obstacle majeur. La mise en place d’un recueil de données pérennes, le renforcement d’un dépistage pour un traitement effectif apparaissent indispensables pour l’éradication du VHC en milieu pénitentiaire.
Abstract
Care for prisoners infected with the hepatitis C virus (HCV) is complex in terms of the sanitary and penal context. The advent of direct-acting antiviral (DAA) treatments for HCV infection, allowing viral cure in most cases, has been instrumental in the national strategy to eliminate HCV by 2025. A review of literature and available national data was performed, in order to collect information on three regions in mainland France (40% of French prisoners). Epidemiology and health care among French prisoners are poorly documented with old data. The Coquelicot survey showed that the prison populations had practices associated with a high risk of HCV contamination and that these practices increased in the context of detention. HCV screening upon entry to prison was 93% in 2010 (PREVACAR), 70% in 2015 and 72% in 2017 (two national surveys) and 56.5% in 2016 (Île-de-France). Seroprevalence and prevalance of HCV infections were 4.8% and 2.5% in 2010 (PREVACAR), 2.9% and 1.1% in 2017 (Fresnes). In the absence of national data on HCV medical care, the CNS survey showed that treatment pathways were heterogeneous, resulting in a treatment cascade of less than 50% of prisoners, with inadequate screening being the major obstacle. Establishing a permanent data collection system and reinforcing screening for effective treatment appear essential for the eradication of HCV in prisons.
Introduction
L’arrivée des traitements antiviraux d’action directe (AAD) a transformé la lutte contre l’épidémie d’infection par le virus de l’hépatite C (VHC) en permettent d’obtenir une guérison virale de la plupart des patients, au terme d’un traitement court et bien toléré de 8 ou 12 semaines. L’objectif gouvernemental d’élimination de l’épidémie de VHC d’ici 2025 implique une stratégie de dépistage à large échelle et de traitement immédiat des patients présentant une hépatite chronique virale C.
Les personnes détenues représentent un groupe à forte prévalence du VHC 1,2 avec en France une séroprévalence estimée en 2010 à 4,8%, soit plus de 6 fois supérieure à celle de la population générale 3,4. Leur prise en compte dans la stratégie d’élimination de l’épidémie est par conséquent déterminante.
Le dépistage de l’infection par le VHC en milieu carcéral s’est constitué historiquement autour de la prévention et du dépistage du VIH 5. Les recommandations en vigueur prévoient de proposer systématiquement un dépistage conjoint du VIH et des virus des hépatites B et C, en particulier lors de la visite médicale obligatoire à l’entrée en détention 6. La prise en charge de l’hépatite chronique virale C en détention s’inscrit cependant dans un parcours de soins (dépistage, évaluation, suivi thérapeutique et post-thérapeutique, prévention) et pénal complexe 7. Sur saisine des pouvoirs publics, le Conseil national du sida et des hépatites virales (CNS) a procédé à un état des lieux des données disponibles et conduit des investigations complémentaires, afin d’évaluer la mise en œuvre effective des principales étapes du parcours de dépistage et d’accès au traitement par les AAD en milieu pénitentiaire.
En dépit de la forte exposition au VHC des personnes majeures incarcérées en France 3 dans les différents établissements pénitentiaires, l’épidémiologie et la prise en charge sont peu documentées, et avec des données anciennes 3. La population détenue est composée surtout d’hommes (96,4%), de nationalité française (77,7%), jeunes (âge médian 31,9 ans (près d’un quart inférieur à 25 ans)) 8. Cette population est défavorisée économiquement et socialement, avec un état de santé plus altéré que celui de la population générale 9. L’enquête Coquelicot de 2004 montrait que 61% des usagers de drogues avaient au moins un antécédent d’incarcération et parmi eux, 12% avaient eu recours à des injections de drogue en détention avec 30% de partage du matériel d’injection 10.
Méthodes
Un examen de la littérature et des données nationales disponibles depuis 2010 a été effectué, en recensant les textes relatifs à la programmation de l’action publique, les programmes et les recommandations nationales, ainsi que les études et enquêtes portant sur la prévalence, la prise en charge, la prévention du VHC chez les personnes détenues en France. L’ensemble de ces données est présenté et analysé dans le rapport et l’avis suivi de recommandations du CNS 11.
Concernant le dépistage, en l’absence de collecte systématique des données épidémiologiques dans les unités sanitaires en milieu pénitentiaire (USMP), une méthode indirecte a été développée à partir des données d’activité renseignées à des fins de suivis administratif et budgétaire par les USMP dans deux bases : l’observatoire des structures de santé des personnes détenues (OSSD), de 2012 à 2016, puis la plateforme Piramig (pilotage des rapports d’activité des missions d’intérêt général), en 2017. Ces bases ne recueillent aucune information sur les résultats, ni sur les actes médicaux consécutifs à un diagnostic. Elles fournissent cependant des données brutes sur le nombre global de tests VIH, VHB et VHC réalisés dans chaque USMP, ainsi que sur le nombre de consultations médicales d’entrée en détention. Entre 2012 et 2017, le nombre d’USMP en fonctionnement a varié entre 170 et 175. Des données complètes pour le dépistage des trois virus étaient disponibles pour 78,8% à 86,2% des USMP selon les années. Aucun biais particulier n’a été repéré concernant les USMP dont les données étaient manquantes, permettant d’estimer le nombre total de tests réalisés chaque année par simple projection à partir du taux d’exhaustivité correspondant (tableau 1). Le taux de détenus effectivement testés pour le VHC à l’entrée en 2017 a été estimé en calculant le rapport entre le nombre de tests effectués et le nombre de consultations réalisées à l’admission. Les données pour ce calcul étaient renseignées par 83% des USMP, correspondant à 86% de la population pénitentiaire.
Une étude qualitative et quantitative approfondie sur l’organisation du parcours de prise en charge du VHC a été réalisée à l’échelle de trois régions (Grand-Est, Sud et Île-de-France) représentant 38% de la population détenue en France. Le CNS a rencontré et auditionné les acteurs régionaux (ARS, Direction interrégionale des services pénitentiaires (DISP), Corevih, associations), ainsi que les personnels soignants et pénitentiaires lors de visites de dix établissements pénitentiaires choisis pour leur diversité (type d’établissements, taille, implantation géographique). Une enquête par questionnaire auprès des pharmacies à usage intérieur (PUI) des établissements hospitaliers de rattachement des USMP des établissements non visités des trois régions a permis de compléter le volet quantitatif 11.
Les caisses primaires d’assurance maladie (CPAM) n’étant pas en mesure de distinguer dans les données de remboursements les délivrances d’AAD effectuées au titre du centre national de gestion de la protection sociale des personnes écrouées (CNPE), ces données ont été recueillies auprès des PUI. Celles-ci, du fait de la prise en charge des AAD en rétrocession, sont en mesure de tracer et décompter chaque traitement initié par l’intermédiaire de l’USMP. L’enquête auprès des PUI a ainsi permis d’établir le nombre personnes détenues ayant bénéficié d’un traitement par AAD sur la période 2016-2018 dans 37 des 43 USMP des trois régions étudiées. Après éviction de sept USMP pour lesquelles les données de dépistage n’étaient pas disponibles, une estimation de la cascade d’accès au traitement par AAD des détenus porteurs d’une infection active à l’entrée en détention en 2017 a été réalisée. Pour ce calcul, le nombre de détenus entrant ayant une sérologie positive au VHC et, parmi eux, de ceux présentant une infection chronique active, a été estimé à partir des données de prévalence disponibles dans la littérature 13,16 (tableau 2).
 Agrandir l'image
Agrandir l'imageRésultats
Dépistage
L’enquête Prevacar avait trouvé, en 2010, que 93% des USMP proposaient systématiquement le dépistage des trois virus (VIH, VHB, VHC) à l’entrée en détention 3. En 2015, puis en 2017, deux enquêtes nationales de pratiques sur la prise en charge de l’hépatite C en milieu pénitentiaire ont été réalisées par questionnaire auprès des USMP, avec respectivement 38% et 43% d’USMP ayant répondu à l’enquête 12,13. Ces USMP rapportaient proposer systématiquement le dépistage à l’entrée pour 98% d’entre elles en 2015 et 94% en 2017, et le taux moyen de réalisation effective déclaré était de 70% et de 72% respectivement. Les différences observées entre les 2 périodes n’étaient pas statistiquement significatives 12,13.
Une étude conduite en Île-de-France en 2016 dans les maisons d’arrêt et quartiers maison d’arrêt montrait un taux de proposition de dépistage de 99,5% et un taux d’acceptation des dépistages de 64,7%, plus élevé chez les femmes (72,2%) que chez les hommes (64,4%) 14. Le taux de réalisation de dépistage avec un rendu de résultat en consultation était de 56,5%, avec un taux plus élevé chez les femmes (67,6%) que chez les hommes (56,1%) 14 (figure 1). Dans cette étude, outre le sexe, le lieu de naissance est associé de manière indépendante (analyse multivariée) à une probabilité supérieure d’acceptation des dépistages (personnes détenues originaires d’Afrique subsaharienne), ou inversement à une probabilité supérieure de refus (personnes détenues originaires des départements et territoires d’outre-mer, ainsi que d’Asie et d’Océanie). Une probabilité d’acceptation supérieure des dépistages était également trouvée, mais uniquement dans l’analyse univariée, chez les personnes détenues âgées de plus de 30 ans au moment de l’incarcération, ainsi que chez celles déclarant des facteurs de risque (antécédents d’infections sexuellement transmissibles, conduites à risques, consommation actuelle ou ancienne de produits psychoactifs). En revanche, aucune association significative n’a été constatée concernant le statut judiciaire (prévenu ou condamné), la récidive ou encore le statut marital.
 Agrandir l'image
Agrandir l'imageL’exploitation par le CNS des données issues des rapports d’activité des USMP montre un nombre de sérologies stable depuis 2013, autour de 50 000/an aussi bien pour le VIH que pour le VHC et le VHB (figure 2, tableau 1). L’estimation du taux de dépistage effectif à l’entrée en détention en 2017 est de 51,6%, avec une variabilité entre les régions de 36,5% à 67,2% (tableau 3). Les observations de terrain montrent que l’organisation des dépistages des trois virus repose dans la quasi-totalité des établissements sur la réalisation de sérologies par prélèvement veineux, l’utilisation de Trod demeurant exceptionnelle 11. Une partie des USMP (40% en 2017 selon les données Piramig) s’appuient à des degrés divers sur des partenariats avec un CeGIDD. Les différentes étapes du dépistage, à commencer par celle du prélèvement sanguin, peuvent être sources d’une complexité organisationnelle. Le délai entre l’acceptation des dépistages par la personne détenue et leur réalisation s’avère extrêmement variable, parfois de quelques jours dans des USMP très organisées et mobilisées, mais généralement d’une à plusieurs semaines, ce qui la rend aléatoire. Une partie des dépistages prévus ne sont finalement jamais réalisés 11. Dans la grande majorité des cas, les USMP n’ont pas organisé de rendu systématique des résultats négatifs, ni mis en place de dispositif structuré de réitération systématique de la proposition de dépistage, par exemple sur une base annuelle 11.
Prévalence
En 2010, Prevacar a permis une estimation robuste de la séroprévalence et de la prévalence des infections chroniques par le VHC en milieu carcéral, respectivement de 4,8% et 2,5%, soit des valeurs 5 à 6 fois supérieures à celles de la population générale 3,15. L’enquête nationale de pratiques sur la prise en charge de l’hépatite C en milieu pénitentiaire, réalisée par questionnaire auprès des USMP en 2015 et en 2017, a aussi fourni des estimations de la séroprévalence 12,13 qui montraient une baisse très sensible, de 4,3% en 2015 à 2,9% en 2017 12,13. En 2017, à Fresnes, la séroprévalence était de 2,9% avec une prévalence d’infections actives de 1,1% (tableau 1). La proportion d’infections actives était de 38% inférieure à celle observée dans Prevacar où elle était de 50% 3,16.
Prise en charge médicale
En l’absence de recueil d’informations de prise en charge médicale du VHC en milieu pénitentiaire, il n’y a pas de données solides disponibles pour évaluer l’accès aux différentes étapes du parcours de soins des personnes dépistées positives pour le VHC ayant débuté un traitement par les AAD.
Selon l’enquête du CNS 11, l’organisation de ce parcours demeure très séquentielle dans certains établissements, impliquant jusqu’à 4 passages à l’USMP, respectivement pour l’annonce du résultat de la sérologie, le prélèvement sanguin pour recherche de la charge virale, la consultation d’annonce du diagnostic et d’entretien médical et le début du traitement 11. Parfois, s’ajoutent des extractions vers le service spécialisé de l’établissement hospitalier de rattachement pour réalisation d’un Fibroscan® ou consultation de spécialiste, sources d’importants délais. Des contraintes organisationnelles fortes pèsent sur la coordination des parcours, en particulier dans les établissements pénitentiaires de petite ou moyenne taille ou dans les centres de détention, où la présence médicale comme la réalisation d’examens hors urgence sont discontinues. Le recours au Fibroscan® dépend de la disponibilité de cet équipement au sein des USMP. Celle-ci est très inégale, notamment selon la taille des établissements et les régions d’implantation 11. En 2017, si au total 68% des USMP disposaient d’un accès à un Fibroscan®, seulement 22% étaient équipées sur site, impliquant des extractions dans les autres cas 13. Le parcours de traitement simplifié, dont relèvent une grande majorité de patients, s’avère très inégalement mis en œuvre par les USMP. Ainsi, les délais entre le moment où le résultat du dépistage est disponible et celui où l’ensemble des éléments nécessaires à l’orientation thérapeutique sont réunis s’étendent souvent à plusieurs semaines ou mois selon les établissements 11. Par contraste, des USMP qui ont mis en place le parcours simplifié, en lien étroit avec le service spécialisé de leur établissement hospitalier de rattachement, ont pu réduire les délais de début de traitement à moins de deux semaines 11.
La chaîne d’approvisionnement des USMP en médicament relève des PUI des établissements hospitaliers de rattachement. Certains établissements pénitentiaires de très grande taille possèdent leur propre service de PUI, mais cette configuration reste exceptionnelle. Selon les observations du CNS, la mise en place d’un traitement par AAD, une fois qu’il a été prescrit, ne pose désormais plus de difficultés particulières et est effective dans des délais ne dépassant généralement pas quelques jours. Les PUI ne font état d’aucun obstacle d’ordre financier ou budgétaire depuis que les AAD dispensés aux personnes détenues sont directement facturés à l’Assurance maladie dans le cadre du régime de rétrocession 11.
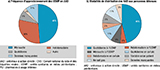
Les modalités de distribution des AAD aux personnes détenues relèvent des choix des équipes au sein des USMP et sont variables (figure 3). Le suivi du traitement par ADD proprement dit ne pose pas de problème d’organisation majeur aux USMP, tant que les personnes détenues demeurent dans l’établissement 11. Les enquêtes de pratiques conduites en 2015 puis 2017 montrent une progression de la délivrance à la semaine, qui passe de 17% à 27% des USMP entre les deux dates, pendant que la délivrance mensuelle demeure stable à 4% 12,13. Les proportions observées dans l’enquête du CNS en 2019 sont sensiblement différentes, avec une part moindre de la délivrance hebdomadaire (11%), mais plus importante (8%) concernant la délivrance mensuelle, suggérant que celle-ci a pu se développer par rapport à 2017. Les deux enquêtes demeurent cependant difficilement comparables en raison de la différence de nature des sources (USMP vs PUI) et de la taille de l’échantillon (national vs 3 régions).
des régions Grand Est, Île-de-France et Sud. Données cumulées des 3 régions : 37 USMP rattachées à 29 PUI
 Agrandir l'image
Agrandir l'imageL’enquête du CNS auprès des PUI montre une augmentation modérée du nombre total de traitements par AAD dispensées aux détenus de 2016 à 2018, avec cependant des schémas d’évolution très différents dans chacune des trois régions 11 (figure 4).
 Agrandir l'image
Agrandir l'imageLa cascade d’accès effectif au traitement par AAD en 2017 dans ces mêmes régions 11 (figure 5) montre que, parmi les personnes dont on estime qu’elles sont porteuses d’une infection par le VHC active lors de leur entrée en détention 13,16, moins d’une sur deux (47,6%) débute un traitement par AAD durant son incarcération. L’insuffisance du dépistage constitue de loin le principal obstacle. En effet, une fois dépistées, plus de huit personnes détenues éligibles au traitement par AAD sur dix (82,7%) y accèdent.
 Agrandir l'image
Agrandir l'imageDiscussion
La connaissance de l’épidémiologie et de la prise en charge du VHC en milieu carcéral en France présente d’importantes fragilités en l’absence de dispositif de collecte de données en routine. Le milieu pénitentiaire concentre pourtant une population concernée par des pratiques associées à un fort risque de contamination par le VHC, majorées dans le contexte de la détention et bien montrées par l’enquête Coquelicot 10.
Le dépistage du VHC, conjointement avec le VIH et le VHB, apparaît très généralement proposé à l’entrée en détention, dans 93% à 99,5% des cas selon les études 3,12,13,14. L’acceptation des dépistages par les détenus demeure mal connue. Seule une étude, portant sur l’Île-de-France, estime le taux d’acceptation à 64,4% 14. Le taux de réalisation effective des dépistages à l’entrée apparaît divergent selon les études. L’enquête de pratiques réalisée auprès des USMP en 2017 l’évalue à 70% 13. Au regard du questionnaire d’enquête, il se peut toutefois que les USMP aient dans leurs réponses exprimé un taux de réalisation rapporté aux détenus ayant accepté la proposition de dépistage, et non à l’ensemble de la file active des détenus entrant. L’enquête effectuée par le CNS à partir des données administratives d’activité des USMP la même année aboutit en effet à un taux nettement inférieur, de 51,6% au plan national, avec d’importantes variations régionales (36,5% à 67,2%) 11. De surcroît, ces taux tendent à être surestimés. Ils sont en effet calculés à partir du nombre total de tests réalisés par les USMP dans l’année, qui inclut, en sus des tests réalisés à l’entrée, un certain nombre de tests effectués en cours de détention, même si leur nombre est présumé modeste. L’étude réalisée en Île-de-France montre pour sa part un taux de réalisation effective à l’entrée de 56,5% 14, similaire à celui retrouvé par le CNS dans la même région (57,1%) 11. La situation française ainsi décrite peut être rapprochée des résultats d’études portant sur les prisons italiennes, qui font état d’une moyenne de dépistage de 64,6% et montrent d’importantes disparités selon les établissements 17,18. Les observations qualitatives du CNS sur l’organisation du parcours de dépistage mettent en évidence plusieurs freins concourant à allonger les délais entre l’acceptation et la mise en œuvre des dépistages, compromettant leur réalisation effective. L’utilisation de Trod demeure l’exception alors que cet outil présenterait des avantages manifestes pour simplifier les parcours, réduire les délais, permettre un rendu des résultats positifs mais aussi négatifs, et réitérer la proposition de dépistage en cours de détention.
Faute de recueil organisé des résultats des dépistages, il n’existe pas de séries de données homogènes permettant de mesurer l’évolution de la prévalence du VHC. Depuis l’étude Prévacar en 2010, seules les deux enquêtes de pratiques en 2015 et 2017 12,13 proposent des estimations nationales de séroprévalence. Une étude réalisée au centre pénitentiaire de Fresnes mesure la séroprévalence et la prévalence des infection chroniques actives à l’échelle de cet établissement en 2017 16. Ces différents résultats peuvent difficilement être comparés entre eux, au regard de questions d’exhaustivité et de représentativité des données, ainsi que de méthodologie de recueil et d’exploitation. Leur intérêt réside en revanche dans les tendances qu’ils mettent en évidence. La comparaison entre les deux vagues de l’enquête de pratiques montre une baisse très sensible de la séroprévalence, de 4,3% à 2,9% 12,13. La séroprévalence mesurée à Fresnes en 2017 est similaire (2,9%), et la prévalence d’infections actives (1,1%) 16 en nette diminution par rapport à celle trouvée en 2010 dans Prevacar. Ces évolutions sont en concordance avec la baisse de la séroprévalence et de la prévalence des infections actives observée en population générale 4,19,20,21, et pourrait être liée à la disponibilité des traitements par AAD.
En milieu pénitentiaire, les conditions règlementaires permettant de prendre en charge et traiter par les AAD l’ensemble des personnes porteuses d’une infection active par le VHC ont été réunies dès l’été 2016, soit une année plus tôt qu’en milieu ouvert, où l’indication de traitement demeurait réservée aux personnes présentant un stade de fibrose F2 ou certaines complications et/ou comorbidités. Les dispositions adoptées en 2017 permettant la simplification des parcours créent des conditions plus favorables à un accès effectif, mais les observations du CNS montrent qu’elles demeurent encore inégalement appropriées par les USMP. Les parcours peuvent être optimisés afin de réduire les délais entre le dépistage et l’initiation du traitement par AAD.
La cascade d’accès au traitement établie par le CNS 11 présente plusieurs limites. Elle s’appuie sur des données de prévalence dont la fragilité a été discutée précédemment. L’étape du diagnostic d’infection active n’a pu être estimée faute de données. Enfin, elle repose sur l’agrégation des données de seulement trois régions. Les résultats ne peuvent être simplement extrapolés à l’ensemble du territoire, notamment dans la mesure où l’on observe dans chacune des régions des tendances divergentes concernant l’évolution du nombre de traitements par AAD délivrés. Cependant, rien n’indique que le profil de la cascade pourrait être significativement différent à l’échelle nationale, puisque la proportion de détenus recevant finalement un traitement par AAD dépend principalement des performances du dépistage. Or les taux de dépistage retrouvés dans les régions étudiées sont plus élevés qu’au niveau national (57,5% vs 51,6%), ce qui suggère que le taux d’accès au traitement en France pourrait être globalement plus faible que l’estimation produite dans l’enquête régionale.
La cascade montre qu’au total, moins d’une personne sur deux potentiellement éligible au traitement par AAD à l’entrée en détention y accède effectivement durant son incarcération. L’insuffisance du dépistage constitue le principal obstacle. Une fois dépistés, les patients éligibles accèdent au traitement dans leur grande majorité. Il demeure toutefois une proportion non négligeable, de l’ordre de 15 à 20% d’entre eux, pour lesquels le traitement n’est pas initié, correspondant pour l’essentiel à des libérations intervenues, soit avant la confirmation du diagnostic, soit avant que le traitement n’ait été mis en place. Ce résultat objective l’importance, notamment au regard de la proportion importante de détenus effectuant des peines de courte durée, de réduire au maximum les délais à toutes les étapes du parcours de soin.
Conclusion
Malgré le manque de données, les méthodes indirectes développées ont permis d’évaluer les taux de détenus testés pour le VHC à l’admission et de décrire la cascade d’accès au traitement par AAD.
La mise en place d’un recueil fiable et pérenne des données de dépistage et de prise en charge en milieu pénitentiaire est cependant indispensable pour suivre la mise en œuvre et évaluer l’efficacité de la stratégie dépistage et de traitement du VHC dans la population-clé des personnes détenues.
Le renforcement du dépistage à l’entrée et au cours de la détention représente le principal défi à relever. L’organisation du parcours de soins à l’issue du dépistage doit également être optimisée pour permettre une initiation plus rapide du traitement par AAD.
Liens d’intérêts
Les auteurs déclarent n’avoir aucun lien d’intérêt au regard du contenu de l’article.
Références
35-36/2013_35-36_3.html
sante-des-populations/personnes-detenues-personnes-placees-sous-main-de-justice/article/prise-en-charge-sanitaire
infections-sexuellement-transmissibles/vih-sida/documents/article/estimation-de-la-seroprevalence-du-vih-et-du-vhc-et-profils-des-usagers-de-drogues-en-france-etude-invs-anrs-coquelicot-2004
beh/2017/14-15/2017_14-15_4.html
santepubliquefrance.fr/beh/2019/24-25/2019_24-25_1.html
Citer cet article
publiquefrance.fr/beh/2022/3-4/2022_3-4_1.html







