Administration d'œstrogènes et risque de maladie veineuse thromboembolique chez les femmes : une revue des données actuelles
// Estrogen use and risk of venous thromboembolism in women: a review of current data
Résumé
L’utilisation d’œstrogènes, seuls ou le plus souvent associés à un progestatif, est fréquente tout au long de la vie des femmes, mais elle expose à une augmentation du risque de maladie veineuse thromboembolique (MVTE). Cet effet indésirable grave dépend des modalités d’administration (molécule et dose d’œstrogènes, voie d’administration, type de progestatifs) et du contexte clinique. Les contraceptifs oraux combinés (COC) sont les formes hormonales les plus utilisées et tous augmentent le risque de MVTE. Cette augmentation est minimale avec les COC faiblement dosés en éthinylestradiol et contenant du lévonorgestrel. Les nouvelles générations de COC sont généralement les plus thrombogènes. Le risque en excès de MVTE lié au traitement hormonal de la ménopause est plus marqué en raison de l’âge plus avancé des femmes. Il peut être réduit en utilisant des œstrogènes transdermiques seuls ou associés à la progestérone. L’effet différentiel de l’œstradiol sur la coagulation sanguine en fonction de sa voie d’administration est montré dans des études mécanistiques randomisées. Le risque de MVTE est considérablement augmenté chez les femmes à haut risque (obésité, antécédent de MVTE, facteurs de risque génétique de MVTE) utilisant des œstrogènes oraux. Une part substantielle d’évènements indésirables pourrait être évitée en respectant les recommandations actuelles. L’amélioration de la sécurité d’emploi des œstrogènes implique en particulier une meilleure stratification du risque individuel et une approche personnalisée.
Abstract
The use of estrogens alone or combined with progestogens is common throughout a women’s life, but increases the risk of venous thromboembolism (VTE). This serious adverse effect depends on both hormonal preparations (molecule and dosage of estrogens, route of administration, and type of progestogens) and clinical background. Combined oral contraceptives (COC) are the most common formulations and all are associated with an increased VTE risk. Reduction in the dose of ethinylestradiol results in a decreased risk of VTE. The lowest VTE risk is found among users of COC containing low doses of ethinylestradiol combined with levonorgestrel. Overall, newer generations of COC are more thrombogenic than second generation ones. The excess risk of VTE attributable to hormone therapy is higher among postmenopausal women. It can be reduced through the use of transdermal estrogens alone or associated to progesterone. The differential effect of estrogens on thrombotic process by route of administration is supported by mechanistic randomized studies. The combination of oral estrogens use and either obesity, history of VTE or genetic risk factors for VTE substantially enhances the VTE risk. Compliance to current recommendations should prevent a significant proportion of VTE events related to estrogens use. Improving individual risk stratification and a personalized approach to estrogens use are major challenges for women’s health.
Introduction
L’administration d’œstrogènes, seuls ou associés à un progestatif, est fréquente chez les femmes pendant la vie reproductive ou après la ménopause. Entre 15 et 65 ans, plus de 8 femmes sur 10 ont recours au moins une fois aux œstrogènes. Leur mode d’administration est très variable et dépend de l’indication. Les contraceptifs oraux combinés (COC) sont les formes hormonales les plus utilisées et contiennent un œstrogène associé à un progestatif. La prise d’œstrogènes chez les femmes en âge de procréer peut être liée, plus rarement, à des troubles gynécologiques (infertilité notamment). Enfin, malgré sa remise en cause récente, le traitement hormonal de la ménopause (THM) reste utilisé par de nombreuses femmes.
L’effet thrombogène des œstrogènes est établi depuis des décennies ; il est à l’origine de l’un de ses principaux effets indésirables graves. La maladie veineuse thromboembolique (MVTE) est un événement rare pendant la vie reproductive. Son incidence est voisine de 1/1 000 femmes/an vers l’âge de 50 ans, mais elle augmente rapidement après la ménopause et atteint environ 1/100/an après 75 ans. Elle se présente le plus souvent sous la forme de thromboses veineuses profondes des membres inférieurs mais sa principale complication, l’embolie pulmonaire, explique une part importante des événements cliniques inauguraux et cause plus de 40 000 décès par an en Europe. La MVTE peut être primitive ou secondaire (immobilisation, cancer...). À côté des facteurs de risque génétiques (mutation du Facteur V Leiden, mutation G20210A du gène de la prothrombine, déficit en antithrombine, protéine C ou protéine S) et cliniques (surpoids, obésité, antécédent familial), le statut hormonal des femmes constitue un important déterminant de la MVTE.
Cette revue se propose de résumer les connaissances sur le risque de MVTE lié à l’utilisation d’œstrogènes chez les femmes en fonction de leurs indications, des nombreuses modalités d’administration et du contexte clinique.
Contraception œstroprogestative
Le recours aux COC n’a cessé de croître depuis leur apparition en France dans les années 1960. Actuellement, plus de 30% des femmes âgées de 20 à 44 ans, soient environ 3 millions d’individus, utilisent cette forme de contraception, qui représente de loin la méthode la plus utilisée dans les pays industrialisés. Les COC sont composés d’un œstrogène de synthèse (éthinylestradiol) et d’un progestatif, appartenant le plus souvent à la famille des norstéroïdes (dérivés de la testostérone). La composition des COC a considérablement varié au cours du temps. Les premières modifications ont concerné la dose d’œstrogènes. Initialement de 100 µg/jour, elle a été réduite à 50 µg/jour dans les pilules « normodosées » et, depuis les années 1980, les pilules « minidosées » délivrent entre 15 et 35 ?g/jour d’éthinylestradiol. Les COC sont généralement classés en fonction de la génération du progestatif (première génération pour la noréthistérone, deuxième pour le lévonorgestrel et troisième pour le désogestrel, le gestodène et le norgestimate). Récemment, des pilules contenant un nouveau progestatif, dérivé de la spironolactone, sont apparues sur le marché (drospirénone). Elles sont dites de quatrième génération. Enfin, certains COC, plus rarement utilisés, contiennent un progestatif de la famille des prégnanes, dérivé de la progestérone (l’acétate de cyprotérone). Une répartition des progestatifs par molécules est aujourd’hui recommandée pour tenir compte de certaines spécificités (cas du norgestimate notamment).
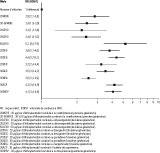
De nombreuses évaluations quantitatives du risque de MVTE associé aux COC ont été publiées. La synthèse des données actuelles présentée dans cette revue est basée sur la plus récente des méta-analyses 1, actualisée par les résultats d’une étude d’envergure menée au Royaume-Uni 2. La figure représente le risque de MVTE en fonction du type de COC (première, deuxième, troisième et quatrième génération). Comparée à la non-utilisation, la prise de COC, quelque soit son type, augmente significativement le risque de MVTE. Néanmoins, cette augmentation dépend de la dose d’œstrogènes et du type de progestatif (génération de progestatifs). Pour un même progestatif, une diminution de la dose quotidienne d’œstrogènes est associée à une moindre augmentation du risque de MVTE pour les COC de deuxième et de troisième génération (désogestrel et gestodène). Cette réduction est particulièrement nette entre 50 et 20/30 µg/jour d’éthinylestradiol pour les COC de deuxième génération. Le bénéfice est moins clair entre 20 et 30 µg/jour d’éthinylestradiol. En fonction du type de progestatif, les COC les moins à risque sont ceux de deuxième génération délivrant de l’éthinylestradiol combiné au lévonorgestrel. Comparé aux COC de deuxième génération, le risque de MVTE est environ deux fois plus élevé chez les utilisatrices de COC de troisième génération, à l’exception du norgestimate qui est associé à un risque similaire à celui du lévonorgestrel. Les contraceptifs de quatrième génération (drospirénone) et les autres types de progestatifs (acétate de cyprotérone) sont associés aux risques thrombotiques les plus élevés.
Les formes non orales d’œstroprogestatifs (patch, anneaux vaginaux) sont beaucoup plus récentes et ont été encore peu évaluées. Les premières données montrent cependant qu’elles sont associées à un risque de MVTE au moins aussi élevé que les COC de troisième génération. Enfin, le risque de MVTE chez les femmes utilisant un COC contenant du valérate d’estradiol n’a pas été évalué faute de recul suffisant.
Au total, la prise de COC augmente le risque de MVTE, mais cette augmentation dépend de la dose d’œstrogènes et du type de molécule progestative. Il est minimum pour les COC de deuxième génération faiblement dosés.
 Agrandir l'image
Agrandir l'image
Traitement hormonal de la ménopause
Longtemps encensé, aujourd’hui décrié, le THM reste utilisé par de nombreuses femmes, notamment pour corriger les troubles fonctionnels de la ménopause. En France, près d’une femme ménopausée sur deux utilisait un THM dans les années 2000, mais cette proportion a considérablement chuté avec environ 10% d’utilisatrices aujourd’hui entre 50 et 60 ans. Ce traitement est extrêmement variable dans sa composition et ses modalités d’administration. Son rapport bénéfice/risque fait aujourd’hui l’objet de nombreuses controverses. La plupart des recommandations actuelles reposent sur des travaux anglo-saxons réalisés chez des femmes utilisant des œstrogènes conjugués équins administrés par voie orale et associés à un progestatif de synthèse (acétate de médroxyprogestérone). Ces résultats ne peuvent être directement extrapolés aux traitements préférentiellement utilisés en France (estradiol administré préférentiellement par voie transdermique combiné à la progestérone micronisée).
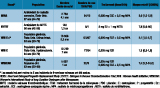
De nombreuses études d’observation ont montré une augmentation du risque thrombotique chez les femmes utilisant des œstrogènes administrés par voie orale 3. L’excès de risque est particulièrement élevé en début de traitement et augmente avec la dose d’œstrogènes. Cet effet est réversible en quelques semaines après l’arrêt du traitement et les anciennes utilisatrices ont un risque similaire à celui des femmes n’ayant jamais utilisé de traitement hormonal. La nature des œstrogènes ne semble pas intervenir de façon importante 4. Des essais randomisés ont confirmé le rôle délétère des œstrogènes oraux dans le développement de la MVTE. Les résultats reposent essentiellement sur trois essais américains (HERS, WHI E+P, WHI E) dans lesquels les femmes utilisaient des œstrogènes conjugués équins associés ou non à l’acétate de médroxyprogestérone (tableau 1). Les essais EVTET et WISDOM, réalisés respectivement en Norvège et au Royaume-Uni, ont été interrompus prématurément mais révélaient, après un an de traitement actif, une augmentation substantielle du risque de MVTE 4.
 Agrandir l'image
Agrandir l'image
L’impact des œstrogènes transdermiques sur le risque thrombotique veineux a été peu étudié. L’étude cas-témoins ESTHER (EStrogen and THromboEmbolism Risk), réalisée en France, a été la première à établir un effet différentiel du THM sur le risque thrombotique en fonction de la voie d’administration des œstrogènes 5. Elle a montré que les œstrogènes transdermiques, contrairement aux œstrogènes oraux, n’augmentaient pas le risque de thrombose. Ces résultats ont été confirmés par quatre études menées en Europe 4 et résumées dans le tableau 2. Afin d’exclure un effet potentiel des progestatifs, les données sont limitées aux femmes utilisant des œstrogènes transdermiques seuls. Les résultats sont tous négatifs, avec des risques relatifs voisins de 1.
 Agrandir l'image
Agrandir l'image
Le rôle majeur de la voie d’administration des œstrogènes est appuyé par des études mécanistiques randomisées montrant que les œstrogènes oraux induisent une hypercoagulabilité, liée en grande partie à une résistance à la protéine C activée 4,6. Cet effet délétère est dû au premier passage hépatique des œstrogènes oraux, et ce phénomène peut en grande partie être évité par les œstrogènes transdermiques qui apparaissent neutres vis-à-vis de la coagulation et de la fibrinolyse. Ce bénéfice potentiel dépend cependant du type d’œstrogène utilisé et n’est pas observé avec l’éthinylestradiol des COC, pour des raisons métaboliques probablement liées à la dégradation plus lente de la molécule.
Le rôle des progestatifs sur le risque thrombotique est aujourd’hui mieux connu et dépend fortement du type de molécule utilisée. La plus étudiée a été l’acétate de médroxyprogestérone, largement utilisé aux États-Unis et dont l’effet délétère sur la thrombose veineuse, lorsqu’il est combiné aux œstrogènes, est étayé par des études observationnelles et des comparaisons randomisées 4. En France, les résultats des études ESTHER et E3N ont montré une augmentation du risque de MVTE chez les femmes utilisant des progestatifs de type norprégnanes (acétate de nomégestrol et promégestone). En revanche, il n’a pas été mis en évidence d’effet délétère de la progestérone micronisée sur le risque de thrombose 4,7.
L’élévation du risque de MVTE lié à la prise d’un THM dépend également du contexte clinique et génétique. Des analyses stratifiées ont bien montré des niveaux de risque thrombotique particulièrement élevés chez les femmes plus âgées, obèses ou en surcharge pondérale, ayant un facteur de risque génétique de MVTE (Facteur V Leiden, mutation G20210A du gène de la prothrombine) et présentant des antécédents de MVTE. En revanche, les données françaises ont montré que les œstrogènes transdermiques ne modifiaient pas le risque de base dans ces contextes spécifiques 3,4,8. Ces résultats sont importants car ils permettent d’identifier des femmes à haut risque susceptibles de bénéficier préférentiellement de mesures préventives. La variabilité génétique des récepteurs aux œstrogènes et des voies enzymatiques impliquées dans leur dégradation n’a pas été confirmée comme un important déterminant du risque thrombotique veineux lié au THM.
Commentaires
Les œstrogènes font partie des molécules les plus prescrites chez les femmes. Leur utilisation répond à des exigences médicales mais reste bien souvent soumise à de fortes influences sociétales. La recherche d’une sécurité d’emploi optimale est plus que jamais un impératif de santé publique. La MVTE est un évènement potentiellement fatal qui contribue fortement à la balance bénéfice/risque des œstrogènes. Elle peut être en grande partie évitée en respectant les recommandations actuelles, qui reposent à la fois sur une meilleure connaissance de l’effet thrombogène des différentes formes hormonales et sur l’identification des femmes à haut risque de MVTE. Les mesures de prévention passent également par une information ciblée des femmes recourant notamment à une contraception ou un THM.
En France, le nombre d’évènements thromboemboliques veineux dus aux COC est estimé à environ 2 500/an, avec près de deux tiers des cas attribuables aux pilules de troisième et quatrième génération. Pour limiter le risque de MVTE, l’utilisation en première intention des COC de seconde génération est préconisée depuis 2012. Cette recommandation a été suivie d’une augmentation des prescriptions de COC de deuxième génération au détriment des COC de dernières générations. Ces modifications de pratiques contraceptives ont eu pour effet une diminution significative du taux d’hospitalisation pour embolie pulmonaire chez les femmes de 15 à 49 ans 9. Chez les femmes à haut risque de MVTE (obésité, antécédent de MVTE), le recours à un progestatif seul ou une contraception non hormonale devrait également permettre d’éviter un nombre substantiel de MVTE.
Chez les femmes ménopausées, le recours à un THM est beaucoup moins fréquent depuis les évaluations randomisées du rapport bénéfice/risque réalisées notamment aux États-Unis. Ce traitement reste cependant le plus efficace dans la prise en charge des troubles fonctionnels de la ménopause. Il est recommandé aujourd’hui à la dose minimum efficace et pour des courtes durées chez des femmes souffrant d’un syndrome climactérique. La MVTE apparait aujourd’hui comme le principal effet indésirable du THM, en particulier dans les premiers mois d’utilisation. Les mesures préventives visant à améliorer la sécurité d’emploi des THM vis à vis du risque de MVTE apparaissent donc particulièrement pertinentes. L’utilisation préférentielle d’œstrogènes transdermiques chez les femmes à haut risque de MVTE pourrait permettre d’éviter environ 8 000 cas d’évènement thromboembolique veineux par an dans l’Union européenne. Une stratégie ciblée sur la surcharge pondérale et les antécédents de MVTE permettrait à elle seule une approche simple et efficace en prévenant environ 80% de ces cas en excès. Ces mesures ont fait récemment l’objet de recommandations internationales 10.
En conclusion, la MVTE est un effet indésirable grave des œstrogènes. Les recherches pharmacologiques et le développement de la pharmaco-épidémiologie devraient permettre d’améliorer leur sécurité d’emploi, notamment par une meilleure stratification du risque individuel et une approche personnalisée.




