Évaluation intermédiaire de START-HPV, programme pilote de dépistage primaire par test HPV des lésions précancéreuses et cancéreuses du col utérin dans le département des Ardennes, France, 2012-2013
// Interim evaluation of START-HPV, pilot programme of HPV-based primary screening for cervical precancerous and cancerous lesions in the Ardennes area, France, 2012-2013
Résumé
Cet article présente un bilan intermédiaire des résultats du programme pilote START-HPV pour le dépistage des lésions précancéreuses et cancéreuses du col utérin. L’objectif de ce programme est de tester les conditions pratiques de mise en place d’un dépistage primaire par test HPV.
La population éligible est constituée des 32 444 femmes résidant dans les Ardennes, âgées de 31 à 65 ans, n’ayant pas fait de frottis cervico-utérin depuis 3 ans et qui sont invitées à faire un prélèvement cervico-utérin (PCU) de dépistage analysé par test HPV.
À l’issue des phases d’invitation initiale et de relance 1, le taux de participation provisoire s’établit à 6,2%. Les PCU ont été réalisés par des médecins généralistes (50,6%), des gynécologues (46,6%) ou d’autres professionnels de santé (2,8%). Le taux de PCU non conformes est de 2,2%. Le taux de tests HPV positifs est de 6,4%, la moyenne d’âge de la population participant étant de 51 ans. Parmi les femmes HPV positives, la cytologie de triage comporte des anomalies dans 43,3% des cas.
Le processus de relance 2 comprenant une proposition d’auto-prélèvement est encore en cours et se terminera courant 2014.
Malgré une phase d’inclusion non finalisée, la participation est faible dans cette population, en dépit de l’implication significative des médecins généralistes. Ceci témoigne probablement de la difficulté à mettre en place une nouvelle organisation de dépistage. Les résultats finaux de l’expérimentation START-HPV seront disponibles fin 2014.
Abstract
This article presents an interim evaluation of START-HPV results, a pilot program for cervical precancerous and cancerous lesion screening. The objective of this programme is to evaluate the conditions for implementing HPV-based primary screening.
The eligible population consists of 32,444 women living in the Ardennes area (France), aged 31-65 years, who did not have any Pap-smear in the last 3 years, and who received an invitation for a smear to be analyzed by HPV testing.
After an initial invitation and recall, a provisional estimate of participation shows a rate of 6.2%. Samples were taken by general practitioners (50.6%), gynecologists (46.6%) or other healthcare professionals (2.8%). The rate of inadequate samples was 2.2%. Samples tested HPV positive in 6.4% of cases and the mean age of attendees was 51 years old. Among HPV positive women, triage cytology demonstrated to be abnormal in 43.3% of cases.
The second recall, including a proposition for self-sampling, is still ongoing and will end in 2014.
Despite an unachieved invitation phase, participation rate is rather low in this population, even with a significant implication of general practitioners. This probably reflects the difficulty to implement a new screening organization. Final results of the START-HPV pilot screening program will be available by the end of the year.
Introduction
Une majorité des cas de cancers du col utérin sont diagnostiqués en France chez des femmes participant de façon irrégulière ou ne participant pas au dépistage de ce cancer. Ce dépistage individuel spontané repose en France sur l’examen cytologique du frottis cervico-utérin (FCU). La Haute Autorité de santé (HAS) recommande un test cytologique sur FCU tous les deux ans après deux résultats normaux à 1an d’intervalle, de 25 à 65 ans 1. La sensibilité de l’examen cytologique est connue comme imparfaite. La répétition de l’examen tous les trois ans permet de compenser partiellement ce défaut de sensibilité, compte tenu de l’évolution lente des lésions précancéreuses du col. Cependant, les études des données de remboursement montrent que l’intervalle moyen entre deux examens est plus souvent inférieur à deux ans. Les femmes n’ayant pas fait de dépistage depuis plus de trois ans peuvent donc être considérées comme peu ou pas dépistées et présentent un risque augmenté de développer une lésion précancéreuse ou cancéreuse du col utérin.
Le développement du cancer du col utérin est lié à une infection persistante à papillomavirus humains à haut risque oncogène (HPV-HR). L’ADN de ces virus peut être facilement recherché à partir d’un prélèvement cervico-utérin (PCU) par une procédure appelée « test HPV ». Des études randomisées internationales ont montré la meilleure sensibilité du test HPV par rapport au test cytologique pour le dépistage primaire des lésions précancéreuses du col utérin 2. De plus, le test HPV peut être réalisé sur des auto-prélèvements avec une sensibilité comparable à celle obtenue sur des PCU, ce qui constitue une option particulièrement intéressante pour améliorer la participation au dépistage 3.
Le programme pilote START-HPV (Sud of Primary Screening in the Ardennes Département by Setting for HPV Infection) a été initié en réponse à un appel à projets de l’Institut national du cancer (INCa) 4. Il s’appuie sur une collaboration entre la SAC 08 (Société ardennaise de cancérologie), structure de gestion du dépistage organisés des Ardennes, et le CHU de Reims. Cette expérimentation s’adresse à une population de femmes peu ou pas dépistées, résidant dans un département présentant une situation sociodémographique relativement défavorable. L’objectif principal de l’expérimentation START-HPV est de tester dans cette population les conditions pratiques de mise en place d’un dépistage primaire organisé par test HPV, avec triage cytologique en cas de résultat HPV positif. Seuls les résultats correspondant aux phases d’invitation initiale et de relance 1 sont présentés ici, la phase de relance 2 étant toujours en cours. Compte tenu du caractère provisoire des données présentées, une place importante de cet article est consacrée à la méthodologie de l’étude.
Matériel et méthode
Population-cible
La population-cible comprend 42 686 personnes et correspond à la cohorte des femmes âgées de 31 à 65 ans, résidant dans les Ardennes, bénéficiaires d’un régime d’assurance maladie, n’ayant pas bénéficié d’un remboursement de FCU dans les trois dernières années, sans antécédent de cancer du col utérin, sans antécédent d’hystérectomie totale, sans suivi en cours pour lésion cervicale et ayant donné leur consentement signé pour participer à l’étude. L’existence d’un FCU de moins de 3 ans est repérée par croisement entre les fichiers de remboursement de l’Assurance maladie, les fichiers transmis par les anatomopathologistes de la région Champagne-Ardenne et les données d’un questionnaire d’éligibilité à compléter avant participation. Les critères d’exclusion médicale sont vérifiés via le questionnaire d’éligibilité. La gestion du fichier de population est assurée par la SAC 08. Cette étude a fait l’objet d’une autorisation de la Commission nationale de l’informatique et des libertés (Cnil) et d’un avis favorable du Comité de protection des personnes (dossier 2011-A01069-32, décision du 25/11/2011).
Modalités d’invitation et de relance
La population-cible reçoit un courrier d’invitation contenant une lettre d’invitation et d’information (à conserver), un formulaire de participation personnalisé (à compléter et joindre au prélèvement) et une enveloppe T (pour retour du formulaire en cas d’exclusion). Les différentes phases de recrutement sont présentées dans la figure 1. L’invitation initiale et la relance 1 proposent un dépistage par test HPV sur PCU, prélevé par un professionnel de santé (médecin généraliste, gynécologue, sage-femme, biologiste). La relance 2 prévoit une randomisation entre un test HPV sur PCU et un test HPV sur auto-prélèvement. Les invitations initiales ont été envoyées entre mai 2012 et janvier 2013, la relance 1 entre février et septembre 2013, la relance 2 entre juin 2013 et janvier 2014. Les relances 1 et 2 sont effectuées par secteur géographique (Vouziers, Rethel, Sedan, Charleville-Mézières, Givet, Signy-le-Petit).
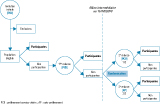 Agrandir l'image
Agrandir l'image
Dispositifs de prélèvement
Les PCU destinés à une analyse par test HPV sont réalisés avec le dispositif DNA Pap Cervical Sampler® (Qiagen). Ce dispositif ne permet pas la réalisation d’un examen cytologique. Les FCU destinés à un examen cytologique de triage sont réalisés lors d’une 2e convocation avec tout dispositif validé pour la cytologie conventionnelle ou en milieu liquide. Les auto-prélèvements sont réalisés avec le dispositif Delphi-Screener® (Delphi Bioscience), qui permet le recueil de cellules cervicales par lavage vaginal.
Test HPV de dépistage
Les PCU DNA Pap sont adressés par voie postale au CHU de Reims pour analyse centralisée par la technique Hybrid Capture 2 HPV Testing® (Qiagen). Cette technique de référence permet de détecter les 13 HPV-HR les plus fréquents. Les prélèvements sont congelés dès réception. Après une étape de dénaturation à la soude, les prélèvements sont analysés avec l’automate Rapid Capture System®, (Qiagen) selon les recommandations du fabricant. Le seuil de positivité est de 1 RLU/PC (Relative Light Units / Positive Calibrator). Les résultats sont validés puis transmis à la SAC 08 via un module Web développé spécifiquement pour l’expérimentation, qui permet d’importer les résultats dans le logiciel Neoscope® (Epiconcept). Un courrier de résultat est adressé sous 15 jours au médecin référent et à la patiente.
Modalités de suivi et de prise en charge
En cas de test de dépistage HPV négatif, il est recommandé aux femmes de réaliser leur prochain test de dépistage dans 5 ans. En cas de test de dépistage HPV positif, les femmes sont invitées à effectuer un nouveau frottis dit de « triage », qui sera analysé par examen cytologique. Si la cytologie de triage retrouve des anomalies, un examen par colposcopie-biopsie est réalisé. Si la cytologie de triage ne retrouve aucune anomalie, un prélèvement cervico-utérin de contrôle à 1 an est recommandé, pour analyse par examen cytologique et test HPV. Si les deux examens de contrôle à 1 an sont négatifs, les femmes sont invitées à faire leur prochain test de dépistage dans 5 ans. Si l’un des examens est positif, les femmes sont adressées pour colposcopie-biopsie. Ces modalités, basées sur les nombreuses publications internationales disponibles 5,6, ont été validées par l’INCa et par le Comité de protection des personnes.
Résultats
Les différentes étapes de sélection de la population-cible sont présentées dans la figure 2. Parmi les 10 242 exclusions, 73,8% correspondent à des exclusions d’ordre médical et 26,2% à une adresse non valide. Parmi les 32 444 femmes constituant la population éligible, le taux de refus de participer s’établit à 1,5%, le taux de non-répondantes à 92,3% et le taux de participation provisoire à 6,2% à l’issue des phases d’invitation initiale et de relance 1.
Parmi les 2 027 PCU adressés pour test HPV, 50,6% ont été réalisés par des médecins généralistes, 46,6% par des gynécologues et 2,8% par d’autres professionnels de santé (sages-femmes, biologistes). Dans 2,2% des cas, les PCU étaient à répéter en raison d’une non-conformité ne permettant pas la réalisation fiable du test HPV (fuite, etc.). À ce jour, 55% de ces non-conformités ont été résolues par l’envoi d’un second PCU.
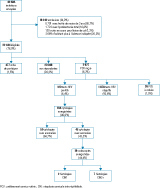 Agrandir l'image
Agrandir l'image
L’âge moyen des participantes est de 51,0 ans (+/- 10,5 ans). Le profil des 2 027 femmes ayant participé au programme START-HPV est détaillé dans la figure 3. Globalement, la participation augmente avec l’âge, avec un taux de participation qui triple quasiment entre le groupe des 31-35 ans (3,5%) et le groupe des 61-65 ans (8,9%). Selon le secteur géographique de résidence, le professionnel de santé majoritairement consulté pour la réalisation du PCU de dépistage est soit le gynécologue, soit le médecin généraliste (secteurs plus ruraux).
 Agrandir l'image
Agrandir l'image
Parmi les 2 027 tests HPV réalisés, 129 sont revenus positifs (6,4%). Le résultat de la cytologie de triage a été enregistré pour 80,6% des femmes testées HPV positives, le recueil étant toujours en cours. Parmi les 104 résultats disponibles, 43,3% des cytologies présentaient des anomalies cellulaires : 11 ASC-US, 25 LSIL, 9 HSIL (ASC-US : atypical squamous cells of undetermined significance ; LSIL : low-grade squamous intraepithelial lesion ; HSIL : high-grade squamous intraepithelial lesion). Sur les 20 examens colposcopiques enregistrés, 6 lésions de haut grade et 1 cancer épidermoïde ont été confirmés histologiquement (recueil des données de suivi non exhaustif).
Discussion – conclusion
Même si le dispositif de recrutement de l’expérimentation START-HPV n’est pas finalisé (relance 2 non prise en compte), le taux de participation provisoire de 6,2% semble particulièrement faible. En effet, dans une étude française récente s’adressant à une population peu ou pas dépistée en situation de précarité, un taux de participation de 17,8% était enregistré à l’issue de l’invitation initiale 7. Cette faible participation peut s’expliquer par la difficulté à mettre en place un nouveau circuit de dépistage : implication des médecins généralistes (alors que plus de 90% des FCU sont actuellement réalisés par les gynécologues), nouveau dispositif de prélèvement, nouveaux interlocuteurs, nouveau test de dépistage, nouvelles habitudes à mettre en place pour les professionnels de santé et pour la population-cible. Cependant, l’un des points positifs est la mobilisation importante des médecins généralistes, qui ont réalisé plus de la moitié des PCU (50,6%). Il faudra attendre plusieurs mois après la fin de la relance 2 pour évaluer le gain de participation lié à l’utilisation de l’auto-prélèvement. Il est cependant déjà clair que la proposition d’auto-prélèvement apporte un gain significatif de participation, notamment dans les tranches d’âges les plus jeunes. Par ailleurs, des actions sont menées pour améliorer le taux de participation (nouvelles actions de communication auprès de la population et des professionnels de santé, implication des centres sociaux, enquête pour identifier les freins, etc.).
La prévalence HPV-HR globale est relativement faible (6,4%) lorsqu’on la compare avec des chiffres publiés précédemment (12,2% chez les plus de 30 ans) 8. Cela est vraisemblablement lié à une différence dans la répartition des âges entre ces deux populations, la population START-HPV étant plus âgée (51 ans versus 34 ans dans Clavel et al.). Pour rappel, le pic de prévalence HPV est observé aux environs de 20-25 ans, puis diminue progressivement avec l’âge. Enfin, même si le recueil des données est encore incomplet, le pourcentage d’anomalies cytologiques retrouvées parmi les femmes avec un test HPV de dépistage positif semble particulièrement important (43,3%). Il est encore trop tôt pour dire si ces anomalies cytologiques correspondent réellement à un nombre important de lésions de haut grade prouvées sur le plan histologique. Une attention particulière est donnée au suivi de ces femmes HPV positives pour les inciter à effectuer les procédures de prise en charge prévues et éviter les perdues de vue. Les résultats finaux de participation à l’expérimentation START-HPV devraient être disponibles d’ici la fin 2014.
Remerciements
Les auteurs remercient les médecins généralistes, gynécologues, sages-femmes, biologistes, pharmaciens, répartiteurs et anatomopathologistes (Dr. Éric Arav, Dr Rémi Picot, Dr. Thérèse Mallaisy, Pr. Philippe Birembaut) ainsi que le personnel de la Société ardennaise de cancérologie (SAC 08) et du Laboratoire Pol Bouin (CHU de Reims), pour leur implication dans cette expérimentation ; l'INCa, la Région Champagne-Ardenne et le CHU de Reims pour leur soutien financier.




