Distribution des papillomavirus humains (HPV) dans des frottis effectués dans le cadre du dépistage organisé du cancer du col de l’utérus en France
// Distribution of Human Papillomavirus types in organized cervical cancer screening in France
Résumé
Introduction –
La vaccination contre les papillomavirus humains bas risque (HPV-BR) de types 6 et 11, agents des condylomes acuminés, et contre les HPV haut risque (HPV-HR) de types 16 et 18, responsables de 70% des cancers du col de l’utérus, a été introduite en France en 2008. La connaissance des caractéristiques de l’infection par les HPV et de la distribution des génotypes dans des frottis cervicaux chez des femmes non vaccinées est un préalable nécessaire à l’évaluation de l’impact de la vaccination sur l’écologie virale et les lésions cervicales associées.
Matériel et méthode –
Les prélèvements résiduels de 6 539 frottis ont été recueillis dans le cadre d’expérimentations de dépistage organisé mises en place dans quatre régions françaises. Les échantillons ont été stratifiés en fonction de l’âge des femmes et des résultats des frottis. Les prélèvements ont été analysés avec la trousse de génotypage PapilloCheck®, qui permet d’identifier 18 HPV-HR et 6 HPV-BR.
Résultats –
La prévalence de l’infection standardisée selon l’âge par les HPV 16/18 (avec ou sans autres HPV oncogènes) était de 47,2% (intervalle de confiance à 95%, IC95%: [42,4-52,1]) dans les lésions de haut grade (HSIL), de 20,2% dans les lésions de bas grade (LSIL) (IC95%: [16,7-23,7]) et de 3,9% [2,8-5,1] dans les frottis normaux. Des HPV-HR étaient détectés dans 13,7% [11,7-15,6] des frottis normaux. Les HPV 16/18 étaient détectés dans 64% des lésions de haut grade (HSIL) chez des femmes âgées de moins de 30 ans. L’HPV 16 était détecté dans 54% (27/50) des cancers invasifs du col, incluant 5 adénocarcinomes.
Conclusion –
L’HPV 16 était fréquemment retrouvé dans les HSIL et les cancers. La forte prévalence d’infection par les HPV 16/18 chez les femmes âgées de moins de 30 ans ayant des HSIL suggère que l’impact de la vaccination sera d’abord observé chez les femmes jeunes.
Abstract
Introduction –
Vaccination against low risk human papillomavirus (LR HPV) types 6 and 11, agents of genital warts, and against the high-risk HPV (HR HPV) types 16 and 18, responsible for 70% of cervical cancers, has been introduced in France in 2008. Knowledge of the characteristics of HPV infection and the distribution of genotypes in cervical smears among unvaccinated women is a prerequisite to assess the impact of the vaccination on viral ecology and cervical lesions.
Material and method –
Residual specimens of 6,539 cervical smears were collected in four French regions participating in organised cervical cancer screening pilot programs. Samples were stratified according to age and cytological grades. They were tested for HPV DNA using the PapilloCheck® genotyping test that identifies 18 HR HPV types and 6 LR HPV types.
Results –
The age-standardised prevalence rates of HPV 16 and/or 18 (with or without other oncogenic HPV types) was 47.2% (95% CI: 42.4-52.1) in high-grade lesions (HSIL), 20.2% in low-grade lesions (LSIL) (95% CI: 16.7-23.7), and 3.9% (95% CI: 2.8-5.1) in normal smears. Overall HR HPV was detected in 13.7% (95% CI: 11.7-15.6) of normal cytology. In women below 30 years of age, 64% of HSIL were associated with HPV 16 and/or 18. HPV 16 was detected in 54% (27/50) of invasive cervical cancers, including 5 adenocarcinomas.
Conclusion –
HPV 16 was frequently found in HSIL and cancers. The high prevalence of infection with HPV 16 and/or 18 among women aged under 30 with HSIL suggests that the impact of vaccination will be primarily observed among young women.
Introduction
L’infection par les papillomavirus humains (HPV) est fréquente chez les jeunes femmes. L’infection persistante par des HPV à haut risque oncogène(HPV-HR) peut conduire au cancer du col de l’utérus. À ce jour, plus de 150 génotypes de HPV ont été décrits et environ 40 d’entre eux infectent le tractus génital 1. Des études épidémiologiques ont montré que les HPV 16 et 18 étaient retrouvés dans 70% des cancers du col. Même si la prévalence de l’infection par HPV 16 est globalement semblable dans tous les pays, il existe cependant des variations dans les taux de prévalence des autres types de HPV 2.
Deux vaccins, Gardasil® (vaccin quadrivalent contre les HPV 6, 11, 16 et 18, développé par Merck, Whitehouse Station, NJ, États-Unis) et Cervarix® (vaccin bivalent contre les HPV 16 et 18, développé par GlaxoSmithKline Biologicals, Rixensart, Belgique), ont été mis sur le marché pour la prévention des lésions précancéreuses et du cancer du col de l’utérus. En France, ces vaccins ont été recommandés de 2007 à 2012 pour les jeunes filles âgées de 14 ans, avec un rattrapage pour les jeunes filles et jeunes femmes qui n’auraient pas eu de rapports sexuels, ou au plus tard dans l’année suivant le début de leur activité sexuelle et jusqu’à l’âge de 23 ans révolus. La nécessité de réviser l’âge de la vaccination est apparue récemment et la vaccination HPV est maintenant recommandée chez les jeunes filles entre 11 et 14 ans 3. La surveillance de l’évolution de l’écologie des HPV dans le contexte de la mise en place de la vaccination a été l’un des motifs de création du Centre national de référence pour les papillomavirus (CNR HPV, Institut Pasteur) en 2008.
En France, le dépistage du cancer du col est un dépistage individuel sauf en Alsace, en Martinique et en Isère, où il est organisé depuis 2001. Il est recommandé de faire un frottis tous les trois ans entre 25 et 65 ans. Des expérimentations de dépistage organisé ont été mises en place récemment dans plusieurs régions, en particulier en Auvergne, Centre-Pays de Loire, Île-de-France et dans le département du Vaucluse. Ces expérimentations ont constitué une opportunité pour obtenir des échantillons de frottis réalisés en milieu liquide sur lesquels effectuer un génotypage des HPV.
Au total, plus de 6 000 échantillons ont été collectés et analysés au CNR HPV. Les résultats présentés dans cet article décrivent la distribution des HPV-HR dans les frottis en fonction de leur grade cytologique et les taux de prévalence en fonction de l’âge des femmes. Ils serviront de base pour l’évaluation de l’impact de la vaccination sur l’écologie virale en France et pour la recherche de phénomènes de remplacement de la niche laissée vacante. En outre, ces résultats permettront d’estimer si des phénomènes de protection croisée contre d’autres génotypes non contenus dans les vaccins et d’immunité de groupe ont pris place depuis l’introduction de la vaccination.
Matériel et méthode
L’objectif était de recueillir et d’analyser avec la trousse de génotypage PapilloCheck® (Greiner Bio-One) les HPV trouvés dans 3 000 frottis normaux, 3 000 frottis anormaux répartis en 1 000 lésions mineures (ASC-US), 1 000 lésions de bas grade (LSIL), 1 000 lésions précancéreuses (HSIL et ASCH) et dans 150 suspicions de cancer/cancers invasifs du col de l’utérus. Ces effectifs avaient été calculés en fonction des données de prévalence d’anomalies cytologiques disponibles à partir des données du dépistage organisé en Alsace (association EVE, Rapport d’activité 2009) et des données 2002 du Crisap Île-de-France (Centre de regroupement informatique et statistique en anatomie pathologique).
Le recueil des échantillons sous forme de fond de tube s’est effectué entre juillet 2009 et novembre 2012. Ces échantillons provenaient de 15 sites localisés dans des départements ou régions participant aux expérimentations de dépistage organisé en Alsace (n=2), Auvergne (n=4), Centre-Pays de Loire (n=3), Île-de-France (n=5) et Vaucluse (n=1). La sélection des sites a été réalisée par le CNR HPV en collaboration avec les structures de gestion des dépistages organisés de ces régions et l’Institut national du cancer (INCa). L’objectif était de sélectionner des laboratoires privés d’anatomopathologie et des structures hospitalières qui réalisaient des frottis en phase liquide dans un milieu ayant un marquage CE et compatible avec la trousse de génotypage des HPV utilisée au CNR HPV. Pour chaque région, l’organisation du recueil des prélèvements a reposé à la fois sur des structures privées de cabinets d’anatomopathologie (recueil de frottis normaux et anormaux) et des centres hospitaliers (services de gynécologie) et anticancéreux pour le recueil des lésions précancéreuses et cancéreuses. Les frottis normaux ont été collectés selon quatre classes d’âges des femmes : 25 à 29 ans, 30-39 ans ; 40-49 ans et plus de 50 ans. Le recueil des prélèvements anormaux s’est effectué en fonction de chaque type d’anomalies cytologiques, quel que soit l’âge des femmes.
Après réception et réalisation du frottis selon les pratiques propres à chaque site, certains échantillons réalisés en milieu liquide étaient anonymisés et envoyés au CNR HPV. Les résultats des frottis étaient classés, selon la classification de Bethesda 2001, en frottis normaux, ASC-US (atypies cellulaires de signification incertaine), LSIL (lésions intraépithéliales de bas grade), HSIL (lésions intraépithéliales de haut grade) et suspicion de cancer invasif 4. La lecture des frottis était réalisée sans connaissance du résultat du test HPV.
Détection et génotypage des HPV
Les ADN viraux et cellulaires ont été extraits avec la trousse Nucleo Spin tissue® (Macherey Nagel). Le génotypage HPV a été réalisé au moyen de la trousse PapilloCheck® (Greiner Bio-One).
Analyse des données
Les HPV sont classés en fonction de leur rôle dans le développement du cancer du col en HPV à bas risque et à haut risque (HR). Les types d’HPV-HR ont été définis selon la classification de l’International Agency Research on Cancer (IARC), comme étant « potentiellement carcinogènes pour les humains ». Il s’agit des HPV 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 et 68 5.
Cinq groupes d’infection HPV ont été définis pour les analyses : (i) infection avec au moins un des 13 HPV-HR, indépendamment de la présence d’une infection avec des HPV à bas risque, (ii) infection avec HPV 16 et/ou HPV 18, indépendamment de la présence d’une infection avec un autre génotype, (iii) infection avec HPV 16 et/ou HPV 18 seul, (iv) infection avec des HPV-HR autres que HPV 16 et/ou HPV 18 et (v) infection multiple avec au moins un HPV-HR.
Les taux de prévalence d’infection HPV pour chaque type de résultat de frottis étaient calculés avec des intervalles de confiance à 95% (IC95%), avec une pondération basée sur la distribution de la population (Insee 2013). Les taux de prévalence pour les cinq groupes d’infection HPV en fonction de l’âge ont été calculés pour les femmes âgées de 25 à 65 ans avec des IC95%. Les différences de taux de prévalence par groupe d’âges et par région ont été évaluées en utilisant un test du Chi2 de Pearson. Les données ont été analysées en utilisant la version 12.0 de Stata Software® (Stata Corporation, College Station, Texas, États-Unis).
Aspects éthiques
Le projet a été soumis le 16 décembre 2009 au Pôle intégré de recherche clinique de l’Institut Pasteur, qui a émis un avis favorable à la réalisation de cette recherche.
Résultats
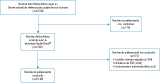
Un total de 6 539 échantillons a été reçu au CNR HPV. Parmi eux, 178 n’étaient pas utilisables pour pratiquer un génotypage des HPV car ils avaient été prélevés plus de quatre semaines avant leur arrivée au CNR. Les résultats du génotypage n’ont pu être obtenus pour 172 prélèvements du fait d’un contrôle interne négatif (104 prélèvements) ou de la présence d’un inhibiteur de PCR (64 échantillons) (figure 1).
Les résultats des tests de génotypage ont finalement pu être analysés pour 6 189 prélèvements. Le tableau 1 présente la localisation géographique des participantes et la répartition des résultats cytologiques des frottis. L’âge médian des femmes était de 36,4 ans et 5 397 d’entre elles (86,7%) appartenaient à la classe d’âge 25-65 ans pour lesquelles le dépistage du cancer du col est recommandé en France. En revanche, 588 femmes étaient âgées de moins de 25 ans (9,5%) et 234 de plus de 65 ans (3,8%).
La prévalence standardisée sur l’âge de chaque groupe d’infection HPV en fonction des résultats des frottis est présentée dans le tableau 2. Les prévalences de l’infection par les HPV-HR standardisées sur l’âge, de l’infection par les HPV 16/18 avec ou sans autre HPV-HR et de l’infection par les HPV 16/18 seuls augmentaient avec le grade du frottis de 13,7% (IC95%: [11,7-15,6]), 3,9% [2,8-5,1] et 2,7% [1,7-3,6] respectivement dans les frottis normaux à 84,4% [80,2-88,6], 47,2% [42,4-52,1] et 27,2% [22,9-31,5] dans les HSIL. À l’inverse, l’infection avec des HPV-HR autres que HPV 16 et/ou HPV 18 et l’infection multiple n’augmentaient pas avec la sévérité du résultat des frottis. Elles étaient plus élevées dans les LSIL que dans les HSIL (48,7% et 37,1%, respectivement, pour l’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 ; 49,1% et 39,9%, respectivement, pour l’infection multiple).
 Agrandir l'image
Agrandir l'image
La figure 2 présente les taux de prévalence d’infection par les HPV-HR, d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 et d’infection par les HPV 16/18 avec ou sans autre HPV-HR en fonction du grade du frottis, dans chaque classe d’âge. Quel que soit le grade du frottis, le taux de prévalence d’infection par les HPV-HR diminue avec l’âge. Dans les frottis ASC-US, la diminution la plus importante est observée après l’âge de 40 ans (57,2% chez les femmes de moins de 40 ans versus 38,1% chez les femmes plus âgées, p<0,001). Pour les frottis normaux, les ASC-US et les LSIL, le taux d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 était toujours supérieur au taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR, quel que soit l’âge des femmes. En revanche, dans les HSIL, le taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR était supérieur au taux d’infection avec des génotypes HR autres que HPV 16 et/ou HPV 18 chez les femmes de moins de 50 ans, alors que c’était le contraire chez les femmes plus âgées. Dans les frottis normaux, les ASC-US et les LSIL, une légère augmentation, non significative, du taux d’infection par les HPV-HR était observée chez les femmes âgées de plus de 65 ans comparées aux femmes âgées de 50 à 64 ans.
Les taux de prévalence de chacun des HPV identifiés avec la trousse PapilloCheck® montrent que, globalement, l’HPV 16 était détecté dans 15,2% de la population étudiée et était le génotype détecté le plus souvent quel que soit le résultat du frottis (tableau 3). L’HPV 18 était à la 12e place (2,4%). Les HPV 16 et/ou 18 étaient détectés dans 3,5% des échantillons de frottis normaux, 17,1% des frottis ASC-US, 24,1% des frottis LSIL et 55,6% des frottis HSIL. Le deuxième génotype le plus fréquemment détecté était l’HPV 51 dans les frottis normaux, l’HPV 53 dans les frottis ASC-US et les frottis LSIL, et l’HPV 31 dans les frottis HSIL. Les HPV 6 et 11 étaient seulement détectés dans, respectivement,1,9% et 0,4% des échantillons.
Cancers du col de l’utérus
Cinquante cas de diagnostic cytologique de cancer du col ont été analysés. L’âge moyen des femmes était de 50,4 ans. Aucun HPV n’a été détecté dans 1 des 5 adénocarcinomes et 3 des 45 carcinomes épidermoïdes. L’HPV 16 a été détecté dans 27 cas (54%) et était associé à d’autres génotypes dans 9 des 27 cas (dont HPV 53 dans 1 cas et HPV 66 dans 2 cas). Les HPV 53 et HPV 66 étaient détectés dans 6 cas chacun et étaient les 2e génotypes les plus fréquemment détectés. L’HPV 18 n’a été détecté ni dans les adénocarcinomes, ni dans les carcinomes épidermoïdes.
Caractéristiques de l’infection par les HPV dans les différentes régions
Dans chacune des quatre principales régions ayant participé à l’étude, les taux d’infection par les HPV-HR, d’infection par les HPV 16/18 avec ou sans autre HPV-HR et d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 variaient significativement en fonction du grade du frottis : les taux d’infection par les HPV-HR et les taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR augmentaient significativement avec la sévérité du frottis. Par contre, c’est dans les lésions de bas grade (LSIL) que les taux d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 et d’infection multiple étaient les plus élevés (données non présentées). La figure 3 présente les taux d’infection par les différents groupes d’HPV par grade de frottis dans les quatre régions. Le taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR était similaire pour les quatre régions dans les frottis normaux : il variait de 2,1 en Auvergne à 4,2% dans la région Centre-Pays de Loire (p=0,08). En revanche, dans ces frottis normaux, le taux d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 variait significativement de 7% en Auvergne à 13,5% en Île-de-France (p<0,0001). Des variations régionales significatives étaient observées pour les taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR dans les lésions de bas grade (ASC-US et LSIL). Dans les ASC-US, le taux d’infection variait de 8,5% dans la région Centre-Pays de Loire à 20,3% en Alsace (p=0,007). Dans les LSIL, il variait de 18% en Île-de-France à 31,2% en Alsace (p<0,0001).En revanche, dans les HSIL, aucune différence significative n’était observée entre les régions, ni pour les taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR, ni pour les infections avec des génotypes HR-HPV autres que HPV 16 et/ou HPV 18. Les échantillons provenant du Vaucluse (n=118) étaient en trop petit nombre pour permettre une étude spécifique.
Discussion
Ce travail constitue la première grande étude française de génotypage des HPV dans le cadre d'un programme organisé de dépistage du cancer du col utérin. Même si les femmes ne sont pas réparties sur l’ensemble du territoire, il s’agit cependant, pour 75% d’entre elles, de femmes pratiquant un frottis dans le contexte d’un dépistage organisé dans le cadre d’une initiation d’un tel programme, alors que les autres habitent dans une région (Alsace) où le dépistage est organisé depuis de nombreuses années.
Nous avons observé que 13,7% des frottis normaux étaient positifs pour la détection des HPV-HR. Des taux supérieurs à 10% ont également été observés dans les études réalisées au Royaume-Uni et en Belgique, en utilisant des méthodes reposant sur la PCR 6,7. Un taux de prévalence en Europe occidentale inférieur, de 8,4%, a été calculé par De Sanjosé et coll. dans une méta-analyse en utilisant les données de prévalence obtenues avec des tests de PCR et d’Hybrid Capture 2® (Qiagen) 8. Une partie des différences observées entre les études pourrait être attribuable à l'utilisation de tests HPV ayant des sensibilités et des spécificités différentes 9.
Nous avons observé des taux de prévalence d'infection par les HPV-HR dans les LSIL et les HSIL semblables à ceux rapportés dans d'autres études européennes et provenant de méta-analyses 10,11.
Les taux de prévalence d’infection par les HPV-HR dans les ASC-US dépendaient de l'âge. En France, les recommandations actuelles pour la prise en charge des ASC-US préconisent une colposcopie immédiate ou un 2e frottis, quel que soit l'âge de la femme (Anaes 2002 (1)). La forte diminution de tests HPV-HR positifs observée dans les ASC-US après l'âge de 40 ans suggère que cet âge pourrait constituer un âge seuil pour le triage virologique des ASC-US. L’utilisation du test HPV pour le triage des ASC-US chez les femmes âgées de plus de 40 ans permettrait de restreindre la réalisation d’une colposcopie à un tiers d’entre elles, car seulement 38% des prélèvements sont HPV-HR positifs.
Dans l'ensemble, les quatre génotypes les plus fréquemment détectés chez les femmes sans anomalies cytologiques étaient les HPV 16 (3,0%), 51 (2,8%), 56 (2,0%) et 53 (1,6%), alors que dans les HSIL, les types les plus répandus étaient les HPV 16 (50,9%), 31 (12,2%), 51 (7,2%) et 33 (6,7%). La distribution était très différente dans une étude rétrospective réalisée en France avec l’HPV 16, détecté dans 62% des néoplasies cervicales intraépithéliales 2/3 12. Cette différence pourrait être expliquée par la variation géographique des populations dépistées. Un vaccin neuf-valent recombiné est actuellement en développement et contiendra les génotypes suivants: HPV 6/11/16/18/31/33/45/52/58. Un tel vaccin ne protège pas contre les types d’HPV 51, 56 et 53, respectivement 3e, 6e et 7e génotypes les plus fréquemment détectés dans les HSIL dans notre pays 13.
Cette étude met en évidence des variations régionales parfois importantes pour les différents regroupements d’HPV dans chaque catégorie de frottis. La variation importante du taux d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 dans les frottis normaux peut s’expliquer par la distribution d’âges différente entre les régions, avec une sur-représentation de la classe d’âge 25-29 ans en Île-de-France. Les différences observées pour les frottis ASC-US peuvent être en partie liées à la définition de cette classe de frottis, qui correspond aux difficultés de classement du cytologiste avec des variations d’interprétation bien connues 14. Des variations significatives du taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR ont été observées dans les lésions de bas grade (LSIL), variant de 18% en Île-de-France à 31% en Alsace. En revanche, dans cette classe de frottis, les taux d’infection avec des génotypes HPV-HR autres que HPV 16 et/ou HPV 18 étaient stables, de 44% à 50%, quelle que soit la région. Ces différences pourraient être liées à des disparités de comportement sexuel des femmes faisant des frottis dans les différentes régions et/ou à des biais de recrutement des femmes au travers des structures dans lesquelles ces prélèvements ont été effectués. Enfin, dans les HSIL, une similitude de la répartition des taux d’infection pour chaque regroupements d’HPV a été observée dans les différentes régions, le taux d’infection par les HPV 16/18 avec ou sans autre HPV-HR étant presque 2 fois plus élevé que le taux d’infection avec des génotypes HR HPV autres que HPV 16 et/ou HPV 18. Si ces données étaient confirmées, elles rassureraient sur l’absence de disparité géographique de risque de cancer du col chez les femmes en France. Des différences similaires ont été observées en Italie, dans une étude régionale de la distribution de l’infection HPV 15.
En conclusion, cette étude est la première à décrire en détail les taux de prévalence de chaque génotype d’HPV en France dans toutes les catégories de frottis, y compris dans les cols normaux. Ces résultats aideront à estimer la proportion de lésions potentiellement évitables avec les vaccins actuels et de deuxième génération. Ils contribueront également à l'évaluation de l'impact de la vaccination sur l'écologie virale.
Remerciements
Nous tenons à remercier les collaborateurs de l’étude : G. Averous et J-J. Baldauf (CHU Hautepierre), Strasbourg ; M. Fender (Association EVE), Illkirch ; E. Schlund-Schoettel (Centre de pathologie), Schiltigheim ; C. Chevenet (laboratoire d’ACP), Aurillac ; P. Dechelotte (Hôpital Estaing), G. Fouilhoux (Centre Perrin), A. Gaillot (laboratoire d’ACP SIPATH), M-A. Grondin (Structure de Gestion ABIDEC-ARDOC) et A-G. Kaemmerlen (Polyclinique Hôtel-Dieu), Clermont-Ferrand ; A-S. Banaszuk (Cap Santé 49) et J. Marchetta (CHU), Angers ; I. de Pinieux (Cabinet Léonard de Vinci), Chambray-lès-Tours ; K. Haguenoer (CCDC), H. Marret (CHU Bretonneau), A. Ruiz (IRSA), Tours ; C. Azoulay (ADOC 94), Joinville-le-Pont ; D. Badaro (laboratoire d’ACP) et R. Dachez (Laboratoire Biomnis), Paris; C. Bergeron (Laboratoire Cerba), Saint-Ouen l’Aumône ; F. Bloget (Laboratoire d’ACP), Avon ; A. Nazac (CHU Bicêtre), Le Kremlin-Bicêtre ; H. Emptas (Laboratoire Histosud), Le Pontet ; C-P. Gautier (ADCA 84), Avignon.
L’étude a été financée par l’Institut Pasteur, l’Institut national du cancer et l’Institut de veille sanitaire.