Les antiviraux à action directe dans le traitement de l’hépatite C chronique : retour sur quatre ans
de prise en charge par l’Assurance
maladie
(janvier 2014-décembre 2017)*
// Direct-acting antivirals in the treatment of chronic hepatitis C: overview of 4 years of coverage by the French Health Insurance (January 2014-December 2017)
* Adaptation d’un article original paru dans la revue Points de repère en mai 2019 :
Dessauce C, Semenzato L, Barthélémy P. Les antiviraux à action directe (AAD) dans le traitement de l’hépatite C chronique :
retour sur 4 ans de prise en charge par l’Assurance maladie. Points de repère (Assurance maladie). 2019;(52):1-9.
Résumé
Introduction –
Depuis fin 2013, les antiviraux à action directe (AAD) révolutionnent le traitement de l’hépatite C. Leur accès a progressivement été élargi à l’ensemble des porteurs chroniques. Dans le contexte de l’objectif d’élimination de l’hépatite C fixé en 2025 en France, ce travail avait pour but d’étudier l’évolution du nombre et des caractéristiques des patients ayant initié un traitement par AAD entre 2014 et 2017.
Méthodes –
Les données sur les initiations de traitement par AAD pour les années 2014 à 2017, en France métropolitaine, ont été extraites du Système national des données de santé (SNDS) pour l’ensemble des régimes.
Résultats –
Entre 2014 et 2017, 58 943 patients ont initié un traitement par AAD : 11 500 en 2014, 13 904 en 2015, 14 291 en 2016 et 19 248 en 2017. Entre 2014/2015 et 2016/2017, l’âge médian des patients a diminué de 56 à 54 ans et la proportion d’hommes est passée de 65 à 57%. L’Île-de-France et Provence-Alpes-Côte d’Azur sont les régions où les nombres de patients ayant initié un traitement rapportés à la population étaient les plus élevés en 2017.
Conclusion –
L’accès universel aux AAD a conduit à une augmentation importante du nombre de patients ayant initié un traitement entre 2016 et 2017 (+35%) et à traiter des patients plus jeunes et plus souvent des femmes. Ces données montrent également que l’objectif de 120 000 patients traités d’ici à 2022 est à moitié atteint. La mobilisation doit néanmoins se poursuivre pour permettre l’élimination de l’hépatite C.
Abstract
Introduction –
Since the end of 2013, direct-acting antivirals (DAAs) have transformed the treatment of hepatitis C. Their access has gradually been extended to all chronic carriers. In the context of the objective of hepatitis C elimination by 2025 in France, this work aimed to study the number and the characteristics of the patients who started DAA treatment between 2014 and 2017.
Methods –
Data on DAA initiations from 2014 to 2017 for metropolitan France were extracted from the French National Health Insurance data system (SNDS) for all schemes.
Results –
Between 2014 and 2017, 58,943 patients initiated a DAA treatment: 11,500 in 2014, 13,904 in 2015, 14,291 in 2016, and 19,248
in 2017. Between 2014/2015 and 2016/2017, the median age of patients decreased from 56 to 54 years, and the proportion of
men increased from 65 to 57%. Île-
de-France and Provence-Alpes-Côte d’Azur were the regions where the number of patients initiating
DAA treatment per 100,000 inhabitants were the highest in 2017.
Conclusion –
Universal access to DAAs has led to a significant increase in the number of patients initiating DAA treatment between 2016 and 2017 (+35%) and to the treatment of younger patients and more often women. These data show that the target of 120,000 patients treated by 2022 is halfway to completion. Mobilization must continue to allow the elimination of hepatitis C.
Introduction
Le virus de l’hépatite C (VHC) provoque une infection du foie pouvant devenir chronique et entraîner, à long terme, des complications hépatiques graves (cirrhose, carcinome hépatocellulaire), nécessitant parfois une transplantation hépatique. L’infection peut être longtemps asymptomatique, entraînant un retard au dépistage et à la prise en charge.
En France métropolitaine, la prévalence de l’hépatite C chronique et le nombre de personnes non diagnostiquées sont en diminution
depuis le début des années 2000. En 2016, le nombre de personnes ayant une infection chronique était estimé à 133 466 (intervalle
de confiance à 95%,
IC95%: [56 880-312 626]). Parmi elles, 25 892 personnes [5 873-74 474] auraient une hépatite C non diagnostiquée
(voir l’article de L. Saboni et coll. dans ce numéro du BEH).
La prise en charge des personnes atteintes d’une hépatite C chronique a beaucoup progressé ces 15 dernières années, notamment grâce aux méthodes non invasives d’évaluation de la fibrose (marqueurs sériques, élastométrie impulsionnelle) qui ont permis de limiter le recours à la ponction-biopsie hépatique. Dans le même temps, le traitement de l’hépatite C chronique a connu une évolution très favorable, passant, au début des années 2000, d’un traitement par bithérapie (interféron pégylé/ribavirine), moyennement efficace (50-80% de guérison virologique selon le génotype) et mal toléré, à une trithérapie, dès 2012, associant à cette bithérapie l’un des deux premiers antiviraux à action directe (AAD) (télaprévir, bocéprévir), permettant un gain d’efficacité mais responsable d’effets indésirables graves 1.
Depuis fin 2013, les nouvelles générations d’AAD révolutionnent la prise en charge thérapeutique de l’hépatite C, en permettant, grâce à des combinaisons de molécules, la guérison de plus de 95% des patients traités avec des durées de traitement de plus en plus courtes et un très bon profil de tolérance. Outre la guérison virologique, il a été montré que la mortalité toutes causes et le risque de carcinome hépatocellulaire étaient significativement plus faibles chez les patients traités par AAD que chez les patients non traités 2. En 2017, deux AAD supplémentaires ont été commercialisés, Zepatier® et Epclusa®, ce dernier, pangénotypique permettant des mises sous traitement simplifié. Dans un premier temps, les AAD ont été réservés aux patients présentant un stade avancé de fibrose hépatique ou une comorbidité, dont la co-infection VIH. Leurs conditions de prescription et de délivrance ont été progressivement étendues, dans un premier temps aux personnes à risque élevé d’infection (instruction ministérielle du 28 juillet 2016), dont les usagers de drogues (UD), puis à l’ensemble des personnes infectées (instruction ministérielle du 6 août 2017) 3.
C’est dans ce contexte qu’en 2014, l’Organisation mondiale de la santé (OMS) a défini un cadre mondial pour l’élimination des hépatites B et C à l’horizon 2030 dans lequel la France s’est engagée 4. Dans le cadre de la stratégie nationale de santé (SNS), une des 25 mesures phares du programme national de santé publique « Priorité prévention » 2018-2022 a fixé cet objectif à l’horizon 2025 5. La SNS s’inscrit dans le cadre de l’Ondam (Objectif national des dépenses d’assurance maladie) pour un rétablissement durable de la situation des finances publiques. Elle contribue à renforcer l’efficience du système de santé en cohérence avec le plan d’appui à la transformation du système de santé. Son premier axe priorise la lutte contre l’hépatite C avec deux objectifs d’ici 2022 6 :
–une diminution de 90% de l’incidence du VHC chez les usagers de drogues (UD) par rapport à 2011 7 ;
–une réduction de 65% de la prévalence de l’hépatite C chronique en population adulte par rapport à 2014 grâce à l’accès au traitement, soit un objectif de 120 000 personnes traitées entre 2014 et fin 2022.
L’objectif principal de cette étude était de décrire l’évolution du nombre de patients ayant initié un traitement par AAD depuis 2014 et leurs principales caractéristiques. L’objectif secondaire était de décrire plus spécifiquement les patients traités par AAD dans deux populations : les patients sous traitement de substitution aux opiacés (TSO) et ceux pris en charge pour une infection par le VIH.
Méthodes
Ce travail a reposé sur l’analyse des remboursements des AAD, à partir des données issues du Système national des données de santé (SNDS) 8.
Les patients étudiés étaient ceux ayant initié un traitement par AAD (de 2e génération) entre janvier 2014 et décembre 2017, en France métropolitaine, quel que soit le régime d’assurance maladie ayant remboursé le traitement. L’initiation était définie comme une délivrance d’AAD précédée d’une période d’au moins six mois sans délivrance d’AAD. Les AAD ont été identifiés à partir de leurs codes UCD (unité commune de dispensation) ou à partir de leur prix lorsque les codes UCD étaient manquants.
Parmi les personnes ayant initié un traitement par AAD, deux sous-populations ont été étudiées :
–les personnes ayant reçu au moins une délivrance de TSO (médicaments de la classe ATC N07BC) en officine entre 2008 et 2017 ;
–les personnes prises en charge pour une infection par le VIH, repérées par la prise en charge en affection de longue durée (ALD) n°7 et/ou le fait d’avoir eu au moins trois délivrances d’antirétroviraux spécifiques du VIH remboursées (sans tenir compte des médicaments utilisés pour la prophylaxie pré-exposition du VIH ou dans le traitement de l’hépatite B) au cours de l’année d’initiation de l’AAD.
Résultats
Entre le 1er janvier 2014 et le 31 décembre 2017, 58 943 patients ont initié un traitement par AAD : 11 500 en 2014, 13 904 en 2015, 14 291 en 2016 et 19 248 en 2017 (tableau 1). Les données par trimestre et schéma thérapeutique montrent une augmentation du nombre de patients initiant un AAD au premier trimestre 2015, suite à la mise à disposition de Harvoni® en novembre 2014, et surtout au premier trimestre 2017, à la suite de la commercialisation de Zepatier® (figure 1). Ce niveau important s’est maintenu au second trimestre 2017 avec un nombre élevé de patients ayant initié un traitement par Epclusa®, inscrit sur la liste des médicaments rétrocédés en avril 2017 3.
 Agrandir l'image
Agrandir l'imageà action directe (AAD) selon la stratégie thérapeutique, France métropolitaine, 2014-2017
 Agrandir l'image
Agrandir l'imageLes patients ayant initié un traitement par AAD au cours de la période 2014-2017 étaient majoritairement des hommes (61%) (tableau 2). Les femmes étaient plus âgées que les hommes, 82% avaient au moins 50 ans (vs 70% pour les hommes). Entre les périodes 2014-2015 et 2016-2017, on observe une diminution de la proportion d’hommes (de 65% à 57%) et une diminution des âges moyens et médians, passant respectivement de 58 à 55 ans et de 56 à 54 ans, Cette baisse de l’âge est observée quel que soit le sexe : la proportion de patients d’au moins 50 ans est ainsi passée de 76% à 64% chez les hommes et de 87% à 77% chez les femmes entre les deux périodes.
par période d’initiation, sexe et classe d’âge pour l’ensemble de la population et les sous-populations TSO et VIH,
France métropolitaine, 2014-2017
 Agrandir l'image
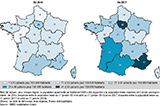
Agrandir l'imageEn 2017, le nombre de patients ayant initié un traitement par AAD pour 100 000 habitants était le plus élevé en Île-de-France et en Provence-Alpes-Côte d’Azur (PACA), puis en Occitanie et Nouvelle-Aquitaine (figure 2). Entre 2014 et 2017, les taux ont augmenté dans toutes les régions, à l’exception de la Corse, où le taux était déjà élevé en 2014 et est resté globalement stable sur la période d’étude. La Nouvelle-Aquitaine est la région où l’évolution de ce taux a été la plus importante (+20 patients pour 100 000 habitants) (tableau 1).
France métropolitaine, 2014 et 2017
 Agrandir l'image
Agrandir l'imagePatients ayant eu un remboursement pour un TSO
Sur la période 2014-2017, 8 714 personnes ayant eu un remboursement de TSO ont initié un traitement par AAD, soit 15% de l’ensemble des patients ayant initié un traitement par AAD. Le nombre annuel de patients a augmenté de façon continue au cours de la période (de +24% à +31% selon les années), passant de 1 440 en 2014 à 3 063 en 2017, soit une augmentation de 113% (tableau 3).
 Agrandir l'image
Agrandir l'imageLes patients sous TSO ayant initié un traitement par AAD étaient très majoritairement des hommes (81%). La moitié de ces patients avaient au moins 50 ans (49% des hommes, 50% des femmes). Entre les périodes 2014-2015 et 2016-2017, la proportion d’hommes est passée de 84% à 79% et la proportion de personnes d’au moins 50 ans a diminué chez les hommes (de 54% à 45%) et chez les femmes (de 59% à 46%) (tableau 2).
Les régions où la proportion de patients sous TSO parmi l’ensemble des patients ayant initié un traitement par AAD était la plus élevée sont les régions Hauts-de-France (21%) et Grand Est (20%) (tableau 1). Elles comptent parmi les régions où l’augmentation du nombre de patients a été la plus importante entre 2014 et 2017, avec la Nouvelle-Aquitaine et Pays de la Loire.
Patients pris en charge pour le VIH
Sur la période 2014-2017, 7 848 personnes prises en charge pour une infection par le VIH ont initié un traitement par AAD, soit 13% de l’ensemble des patients ayant initié un traitement par AAD. Ce nombre de patients a fortement augmenté entre 2014 et 2015 (+89%), a stagné entre 2015 et 2016 (-4%) et a diminué de façon importante entre 2016 et 2017 (-47%) (tableau 3).
Les trois-quarts des patients pris en charge pour le VIH et ayant initié un traitement par AAD étaient des hommes. Cette proportion est restée stable entre les périodes 2014-2015 et 2016-2017. Au cours de la période 2014-2017, les deux-tiers des patients avaient au moins 50 ans (64% des hommes, 71% des femmes). Cette proportion a diminué de 68% à 60% chez les hommes entre les périodes 2014-2015 et 2016-2017, tandis qu’elle est restée stable (71%) chez les femmes (tableau 2).
La proportion de patients pris en charge pour le VIH parmi les patients ayant initié un traitement par AAD était la plus élevée en PACA (19%) et en Île-de-France (18%) (tableau 1). Entre 2014 et 2017, cette proportion a diminué dans toutes les régions, à l’exception des régions Nouvelle-Aquitaine (+82%) et Île-de-France (+12%).
Discussion
Fin 2017, 58 943 patients avaient initié un traitement par AAD, soit environ la moitié de l’objectif fixé à 120 000 personnes d’ici 2022. Cela équivaut à plus de 53 000 patients guéris (en faisant l’hypothèse d’un taux de guérison de 90%, plus faible que celui constaté dans les études observationnelles 9,10, pour tenir compte de possibles défauts d’observance), contribuant ainsi à la tendance vers la diminution de la prévalence de l’infection chronique entre 2011 (192 700 [IC95%: 150 935-246 055]) 11 et 2016 (133 466 [IC95%: 56 882-312 626]) (voir article de L. Saboni et coll. dans ce numéro du BEH). Ce résultat a pu être obtenu grâce à l’ouverture progressive du périmètre de prise en charge des AAD. En 2014, seuls les patients ayant une hépatite C à un stade avancé de fibrose hépatique, ayant une co-infection par le VIH, une cryoglobulinémie symptomatique ou un lymphome B bénéficiaient d’un remboursement des AAD. Puis l’accès universel aux AAD pour toutes les personnes vivant avec le VHC, annoncé en mai 2016, a été effectif en août 2017 après l’obtention d’une baisse importante de prix. Cela a conduit à une augmentation du nombre de patients ayant initié un traitement au cours de la période d’étude, particulièrement marquée entre 2016 et 2017 (+35%).
L’année 2017 est particulièrement atypique avec un nombre très important de personnes initiant un traitement par AAD (n=19 248), notamment au cours des deux premiers trimestres. Si cette augmentation est probablement liée à l’ouverture du périmètre de prise en charge des AAD (août 2017), elle est observée avant même l’élargissement de la prise en charge. Cette forte augmentation pourrait être également liée à la commercialisation de Zepatier®, actif sur les génotypes 1 et 4, et d’Epclusa® pangénotypique (deux nouvelles associations fixes d’AAD) au début de l’année 2017. Certains prescripteurs auraient pu attendre l’arrivée de ces AAD pour initier un traitement, en raison de leur plus grande simplicité d’utilisation et de leur peu d’effets secondaires. De la même façon, une augmentation avait été observée au premier trimestre 2015, à la suite de la mise à disposition de Harvoni® fin 2014, première association fixe de deux AAD pour les génotypes 1, 3 et 4 et pour une durée de traitement de 8 à 24 semaines selon les formes cliniques. Les données trimestrielles montrent que les nouveaux schémas thérapeutiques ont été largement utilisés dès leur mise à disposition.
Avec une majorité d’hommes (61%) et un âge médian d’environ 55 ans, le profil démographique des patients ayant initié un traitement par AAD entre 2014 et 2017 était très proche de celui des patients pris en charge dans les services experts (1) 12. Entre les périodes 2014-2015 et 2016-2017, la diminution de l’âge est probablement liée à l’accès universel à partir de 2017, permettant aux patients présentant une forme peu avancée de la maladie, plus jeunes, d’être traités. Entre ces deux périodes, la proportion d’hommes a également baissé (de 65% à 57%). L’une des hypothèses est que les femmes auraient été traitées plus tardivement sur la période d’étude, du fait de la moindre sévérité de leur hépatite C chronique. En effet, les données de la littérature montrent que la vitesse de progression de la fibrose et le risque de carcinome hépatocellulaire sont moindres chez les femmes, probablement en rapport avec des facteurs de risque moins fréquents (consommation excessive d’alcool, syndrome métabolique notamment), ou du fait des propriétés antifibrosantes des œstrogènes 13.
Les régions où les nombres de patients ayant initié un AAD rapportés à la population sont les plus élevés (Île-de-France, PACA, Occitanie et Nouvelle-Aquitaine) sont celles où les taux de tests VHC confirmés positifs et de personnes bénéficiant de l’ALD pour hépatite C chronique sont les plus importants 14. Le nombre et le taux de patients ayant initié un AAD ont augmenté dans la quasi-totalité des régions entre 2014 et 2017.
Grâce à la quasi-exhaustivité des données de remboursement des AAD dans le SNDS (absence de biais de participation, exhaustivité des remboursements des médicaments délivrés) et à la spécificité des AAD dans le traitement de l’hépatite C et de leur prise en charge par l’Assurance maladie, cette analyse a permis de suivre l’évolution du nombre et des caractéristiques démographiques des patients ayant initié un AAD entre 2014 et 2017 en France métropolitaine. La principale limite est liée à l’absence d’informations épidémiologiques et cliniques (expositions à risque, stade de la maladie, génotype…).
C’est pourquoi, les personnes ayant eu au moins un remboursement de TSO ont été identifiées afin d’approcher au mieux la population d’UD (anciens ou actuels). Parmi eux, l’augmentation du nombre de patients ayant initié un AAD a été plus importante (+113%) que pour l’ensemble des personnes ayant initié un AAD (+67%). Les personnes ayant eu un remboursement de TSO représentaient 15% des personnes ayant initié un AAD au cours de la période 2014-2017. L’interprétation de cette proportion au regard de la proportion de personnes contaminées par usage de drogues parmi l’ensemble des porteurs d’hépatite C chronique ou des patients pris en charge dans les services experts (entre un quart et un tiers 11,12) doit être extrêmement prudente, en raison du recoupement imparfait des personnes ayant eu un remboursement de TSO délivré en officine de ville entre 2008 et 2017 et des personnes ayant été usagères de drogues au cours de leur vie. Les personnes avec un TSO délivré à l’hôpital ou par une structure spécialisée ne sont pas repérées. En outre, si 77% des UD fréquentant les structures de réduction des risques en 2011-2013 avaient reçu un TSO au cours des 6 mois précédents 15, cette proportion était probablement nettement inférieure chez l’ensemble des personnes ayant consommé des drogues au cours de leur vie, ou parmi les usagers injecteurs actifs au cours du dernier mois chez lesquels l’incidence du VHC atteignait 11,2 pour 100 personnes-années (IC95%: [9,0-19,0]) 7. Ces usagers actifs, souvent éloignés du système de santé, devraient bénéficier d’actions hors les murs ou d’actions « Test and treat » renforcées (consistant à proposer de façon simultanée un dépistage, un bilan pré-thérapeutique et un traitement si nécessaire) pour atteindre l’objectif d’élimination de l’hépatite C. En outre, la poursuite et l’intensification de la mise en œuvre des mesures de réduction des risques (programmes d’échanges de seringues, TSO notamment) sont indispensables pour prévenir les contaminations 16.
Les patients identifiés comme pris en charge pour le VIH représentaient 13% de l’ensemble des patients ayant initié un AAD entre 2014 et 2017. Cette proportion semble élevée au regard de la proportion de personnes co-infectées par le VIH parmi les patients pris en charge pour une hépatite C chronique dans les services experts (4-7% entre 2001 et 2007) 17 et compte tenu du fait que l’algorithme n’identifie pas la totalité des patients pris en charge pour le VIH. Cette proportion élevée pourrait s’expliquer par l’accès universel aux AAD des personnes ayant une infection par le VIH dès 2014 et par une prise en charge intégrée des soins de l’infection par le VIH et des hépatites. Le nombre de patients pris en charge pour une infection par le VIH et initiant un AAD est en diminution depuis 2016, suggérant qu’une majorité de ceux-ci ont été traités les premières années.
Perspectives
La lutte contre l’hépatite C bénéficie d’un engagement politique fort qui a permis rapidement l’accès universel au traitement par AAD. Sur le plan financier, plus de 3,5 milliards d’euros ont été remboursés par l’Assurance maladie pour les AAD entre 2014 et 2017. À ce jour, pour atteindre l’objectif des 120 000 patients traités d’ici 2022, il est nécessaire d’inclure environ 12 000 personnes par an. Pour ce faire, il faut renforcer l’identification des personnes ignorant leur statut. Cela n’est réalisable que par le maintien de la mobilisation des acteurs de première ligne, qui devrait se renforcer par la mise en place de dispositifs innovants de parcours « Test and treat » en particulier chez les UD, l’ouverture de la prescription de deux AAD pangénotypiques (Epclusa® et Maviret®) aux médecins généralistes depuis mai 2019 18 et le renforcement de l’incitation au dépistage à partir des recommandations à venir de la Haute Autorité de santé 19, et grâce à la mise en œuvre de campagnes régionales.
Liens d’intérêt
Les auteurs déclarent ne pas avoir de liens d’intérêt au regard du contenu de l’article.
Références
evaluation-des-strategies-de-depistage-des-personnes-infectees-par-le-vhc-volet-1-feuille-de-route




