Les issues de traitement des tuberculoses sensibles déclarées en France, 2008-2014
// Treatment outcome of non-resistant tuberculosis cases reported in France, 2008-2014
Résumé
La surveillance des issues de traitement des patients atteints de tuberculose maladie, introduite dans la déclaration obligatoire (DO) en France en juillet 2007, est un élément essentiel de la lutte antituberculeuse. Elle permet d’identifier les cas qui ont achevé leur traitement et sont considérés comme guéris, et les cas qui n’ont pas complété leur traitement et qui, s’ils sont contagieux, peuvent continuer à transmettre l’infection dans la communauté. Nous présentons dans cet article les résultats nationaux de cette surveillance depuis la mise à DO des issues de traitement, soit pour les cas de tuberculose maladie déclarés entre 2008 et 2014.
Les patients ont été classés en fonction de leur situation dans les 12 mois après le début du traitement en se basant sur les définitions européennes. Les tuberculoses identifiées comme multirésistantes (MDR) dans la DO ont été exclues. Des informations sur l’issue de traitement étaient disponibles pour 65% des cas, avec une amélioration des informations renseignées entre 2008 (60%) et 2014 (72%) (p<0,001). Le pourcentage de départements ne fournissant pas d’information était de 9% en 2008 et de 3% en 2014. Pendant cette période, 74,1% des cas de tuberculose, toutes formes cliniques confondues, ont achevé le traitement, cette proportion s’améliorant sensiblement au cours du temps (passant de 73,0% en 2008 à 76,9% en 2014, p<0,001). Chez les cas pulmonaires, la proportion de traitement achevé était de 73,2%, de 70,6% chez les cas pulmonaires à microscopie positive et de 74,0% chez les cas pulmonaires à culture positive. Parmi ces cas, 19,8% avaient une issue potentiellement défavorable, dont 44% étaient des perdus de vue, 25% des patients transférés, 13% des patients toujours en traitement à 12 mois, 9% des décès en lien avec la tuberculose et 9% des cas ayant arrêté et non repris leur traitement. La diminution régulière du nombre de cas avec une issue de traitement non renseignée et la diminution du nombre de départements n’ayant pas fourni d’informations sur les issues de traitement indiquent une meilleure déclaration et peut-être un meilleur suivi des cas. Le pourcentage de patients ayant achevé leur traitement, qui a augmenté sur la période d’étude, suggère une meilleure prise en charge de ces patients.
Même si ces résultats sont encourageants, ils sont insuffisants et inférieurs à l’objectif de l’Organisation mondiale de la santé d’au moins 90% de guérison pour les cas pulmonaires à microscopie positive. Ils devraient inciter ces différents acteurs à poursuivre et à renforcer cette surveillance.
Abstract
Surveillance of tuberculosis treatment outcome introduced in mandatory notification (MN) in France in July 2007, is a key component of tuberculous control. It allows identifying patients who have completed the treatment and are considered as cured, and patients who have not completed the treatment and who, if contagious, may potentially continue to transmit the infection in the community. We present in this article the results of this national surveillance since its MN, that is to say for tuberculosis cases reported between 2008 and 2014.
Patients were classified according to their situation in the 12 months after the beginning of treatment based on European definitions. Tuberculosis cases identified as multi-drug resistant (MDR) in the MN form were excluded from the analysis. Information on treatment outcome was available for 65% of the cases, with an increase in availability between 2008 (60%) and 2014 (71%) (p<0.001). The percentage of departments not providing this information was 9% in 2008 and 3% in 2014. During this period, 74.1% of tuberculosis cases completed their treatment whatever their clinical presentation, with a significant increase from 73.0% in 2008 to 76.9% in 2014, p<0.001. This proportion was 73.2% in pulmonary cases, 70.6% in pulmonary cases with a positive smear for AFB, and 74.0% in culture positive pulmonary cases. Among those cases, 19.8% had a potentially unfavorable outcome, including 44% lost-to-follow-up, 25% transferred-out, 13% still on treatment, 9% tuberculosis-related deaths, and 9% of cases having interrupted or abandoned their treatment. The regular decrease of the number of cases without information on tuberculosis treatment outcome, and the decrease in the number of departments not having supplied this information indicate a better notification of cases and possibly a better follow-up. Increase over time in the number of patients having completed their treatment suggests a better case management.
Nevertheless, even if these results are encouraging, they are below the World Health Organization target of at least 90% cured for pulmonary cases with a positive microscopy. They should encourage the different actors involved in tuberculosis control to continue and strengthen this surveillance.
Introduction
L’Organisation mondiale de la santé (OMS) estimait à 10,4 millions le nombre de nouveaux cas de tuberculose dans le monde en 2016 1. Les tendances récentes montrent cependant une décroissance globale de l’incidence, en particulier dans les pays de l’Union européenne et de l’Espace économique européen, où le taux de déclaration était de 11,7 cas/105 habitants en 2015 2. Cette diminution est également constatée en France, où 4 741 cas étaient déclarés en 2015 (contre 5 368 en 2005), soit un taux de déclaration de 7,1 cas/105 habitants 3.
La maitrise de la tuberculose nécessite l’identification rapide des cas et leur prise en charge précoce par un traitement antituberculeux adéquat et complet, permettant de guérir le patient, de limiter la transmission du bacille dans la communauté et d’éviter le développement de la résistance aux antituberculeux 4,5. Dans le cadre de la lutte antituberculeuse, la surveillance des patients traités est donc essentielle, car elle permet d’identifier les cas n’ayant pas complété leur traitement et qui, s’ils sont pulmonaires, peuvent potentiellement continuer à transmettre l’infection dans la communauté. Dans une cohorte de cas déclarés une année donnée, la proportion de cas considérés comme guéris est un indicateur-clé dans l’évaluation et le suivi du programme national de lutte antituberculeuse. En 1991, une résolution de l’Assemblée mondiale de l’OMS définissait deux objectifs pour contrôler la tuberculose : la détection d’au moins 70% des nouveaux cas de tuberculose pulmonaire à microscopie positive et la guérison de 85% d’entre eux 6. Lorsque ces objectifs sont atteints, permettant de maintenir de faibles niveaux de résistance acquise aux antituberculeux, un programme de lutte contre la tuberculose peut être considéré comme efficace 7. En 2014, dans le cadre de la nouvelle stratégie « Mettre fin à la tuberculose », ces objectifs ont été actualisés et sont désormais de dépister au moins 90% des cas et d’atteindre 90% de succès thérapeutique 8.
En France, la surveillance des issues de traitement des patients avec une tuberculose maladie, qu’elle soit pulmonaire ou non, a été recommandée par le Conseil supérieur d’hygiène publique de France en mai 2006 9 et introduite dans la déclaration obligatoire (DO) en juillet 2007. L’objectif était d’évaluer la proportion de cas ayant achevé le traitement et de dénombrer et décrire les cas ne l’ayant pas achevé, afin d’adapter la politique de lutte antituberculeuse. La surveillance des issues de traitement en France s’applique aussi aux cas non pulmonaires, qui représentaient entre 26% et 29% des cas déclarés entre 2008 et 2014. En effet, si les cas exclusivement extra-pulmonaires ne présentent pas une menace immédiate en termes de transmission, un traitement adéquat et complet est important pour la santé des patients et la surveillance des issues de traitement des cas extra-pulmonaires contribue à une évaluation des efforts de prise en charge de la tuberculose dans son ensemble.
Les résultats pour les cas déclarés en 2008 10 et 2009 11 montraient que 69% et 70% des cas pulmonaires avaient achevé leur traitement, respectivement. Cet article reprend ces résultats et intègre les résultats de l’analyse des issues de traitement des tuberculoses déclarées de 2010 à 2014, permettant ainsi de montrer les tendances depuis leur mise à DO.
Méthodes
Source de données
Les données présentées dans cet article proviennent de la DO des cas de tuberculose maladie déclarés entre 2008 et 2014. Les données de 2008 à 2010, ayant fait l’objet d’une analyse antérieurement 10,11 ont été mises à jour, principalement en tenant compte des informations saisies après publication et en enlevant de l’analyse les tuberculoses indiquées comme multirésistantes dans la DO (MDR : résistance à la rifampicine et à l’isoniazide). Nous avons également exclu les tuberculoses résistantes seulement à la rifampicine (RR) identifiées dans la fiche de DO (en effet, la résistance à la RR isolée étant souvent un indicateur de MDR, l’OMS recommande depuis mai 2016 que les tuberculoses RR soient traitées comme les tuberculoses MDR) 12.
Les cas de tuberculose sont signalés et déclarés à l’Agence régionale de santé (ARS) par les médecins et biologistes en ayant fait le diagnostic. Les informations sur l’issue de traitement sont renseignées 12 mois après le diagnostic ou la mise en place du traitement. Celles-ci sont demandées aux déclarants (directement ou via le Centre de lutte antituberculeuse – Clat) par l’ARS qui les vérifie, les saisit sur un logiciel dédié en complétant les informations du patient dont la notification initiale a été faite 12 mois auparavant, puis les transmet annuellement sous forme électronique et anonymisée à Santé publique France. Ces données sont ensuite apurées, des contrôles de cohérence sont réalisés, les doublons sont exclus et, le cas échéant, des vérifications sont effectuées auprès des Clat ou des ARS avant d’effectuer l’analyse sur un fichier validé.
Définition de tuberculose maladie et des catégories d’issues de traitement
Les définitions de tuberculose utilisées sont basées sur les définitions internationales13,14. Les cas de tuberculose à déclarer comprennent les cas avec des signes cliniques et/ou radiologiques compatibles avec une tuberculose s’accompagnant d’une décision de traitement antituberculeux standard, que ces cas soient ou non confirmés par la mise en évidence à la culture d’une mycobactérie du complexe tuberculosis. Les formes pulmonaires comprennent les atteintes du parenchyme pulmonaire, de l’arbre trachéo-bronchique ou du larynx et peuvent être associées ou non à des localisations extra-pulmonaires de la maladie. Les formes respiratoires autres (ganglionnaires intra-thoraciques ou pleurales) sont considérées comme extra-pulmonaires.
L’issue de traitement est collectée pour tout patient pour lequel une déclaration obligatoire de tuberculose maladie a été faite, sauf ceux ayant eu un diagnostic post-mortem de tuberculose. L’information sur l’issue de traitement porte sur la situation du patient 12 mois après la date de début de traitement si le patient a commencé un traitement, la date de diagnostic en cas de refus de traitement ou la date de déclaration, si la date de début de traitement et la date de diagnostic ne sont pas renseignées. Les cas sont classés dans sept catégories d’issues de traitement qui ont été définies en adaptant les recommandations européennes 15 au contexte français : (1) traitement achevé (le patient est considéré comme guéri par le médecin et a pris au moins 80% d’un traitement antituberculeux complet), qui est considéré comme l’issue favorable de traitement ; (2) décès pendant le traitement (avec ou sans lien avec la tuberculose, ou sans lien connu) ; (3) traitement arrêté et non repris (parce que le diagnostic de tuberculose n’a pas été retenu ou pour une autre raison) ; (4) patient toujours en traitement pour les raisons suivantes : traitement initialement prévu pour une durée supérieure à 12 mois (car la déclaration des issues de traitement ne s’intéresse qu’aux tuberculoses sensibles et non pas aux tuberculoses MDR évaluées à 24 et à 36 mois), traitement interrompu plus de deux mois, traitement modifié en raison d’une résistance initiale ou acquise aux antituberculeux, d’effets secondaires ou d’une intolérance au traitement, ou d’un échec du traitement initial ; (5) transfert vers un autre médecin ou établissement ; (6) patient perdu de vue ; (7) sans information.
La cohorte des cas inclus dans notre analyse exclut les cas ayant fait l’objet d’une déclaration initiale avec un diagnostic post-mortem de tuberculose et ceux dont le diagnostic de tuberculose n’a finalement pas été retenu (mycobactéries atypiques, cancer, etc.). Les cas inclus dans l’analyse ont été regroupés et présentés en quatre catégories : (a) traitement achevé ; (b) issue potentiellement défavorable comprenant les décès directement liés à la tuberculose, les traitements interrompus et non repris pour une raison autre qu’un diagnostic de tuberculose non retenu, les patients toujours en traitement à 12 mois en raison d’un traitement interrompu plus de deux mois ou d’un traitement modifié (résistance, effets secondaires ou intolérance, échec initial), les patients transférés ou perdus de vue ; (c) décès sans lien avec la tuberculose ou avec lien non renseigné ; (d) situation non évaluable : patient toujours en traitement à 12 mois du fait d’un traitement initialement prévu pour une durée supérieure à 12 mois. Cette classification est adaptée de celle généralement utilisée internationalement 16, bien que la même classification ne soit pas toujours utilisée dans tous les pays d’Europe 17. Les résultats de culture n’étant renseignés en début de traitement que pour 56% des cas déclarés et peu renseignés en fin de traitement, la proportion de guérison bactériologique n’est pas présentée ici.
Analyse des données
L’analyse a d’abord consisté à décrire les issues de traitement des cas inclus dans l’analyse par région, par année de déclaration et selon les principales caractéristiques des cas. Nous avons ensuite décrit les cas avec un traitement achevé et ceux avec une issue potentiellement défavorable selon certaines caractéristiques cliniques, microbiologiques, sociales et démographiques. Une analyse univariée a comparé les traitements achevés aux issues potentiellement défavorables, permettant de mettre en évidence des associations statistiquement significatives avec certains facteurs. L’analyse des données a été effectuée avec le logiciel Stata 12.1® (StataCorp, College Station, Texas, USA). Les comparaisons de proportions ont été faites à l’aide du test du chi2, celle des moyennes par le test de Student. Une tendance a parfois été testée. Le seuil de significativité statistique était de 5%.
Résultats
Caractéristiques de cas inclus dans l’analyse
Au total, 36 117 fiches de DO de tuberculose ont été transmises par les ARS entre 2008 et 2014 dans le cadre de la surveillance des issues de traitement. Ce nombre est légèrement supérieur (+0,5%) à celui publié sur le site de Santé publique France 18, car il comprend des cas dont les DO ont été transmises après la publication initiale. Parmi ces cas, 34 762 (96%) étaient éligibles à l’analyse, dont 22 526 (65%) ont été retenus car ayant une information sur l’issue du traitement (tableau 1).
 Agrandir l'image
Agrandir l'imageL’issue de traitement était renseignée dans 79,7% (n=1 662) des cas lorsque le médecin déclarant était un médecin de Clat, 67,7% (n=1 674) des cas s’il s’agissait d’un pneumologue libéral, 64,3% (n=17 649) des cas pour les médecins hospitaliers, 61,9% (n=720) des cas pour les biologistes hospitaliers et 55,1% (n=520) des cas pour les « autres médecins déclarants » (p<0,0001) (le type de médecin déclarant n’était pas renseigné pour 301 cas). Le nombre d’observations avec une issue de traitement renseignée et donc inclus dans l’analyse augmentait significativement au cours du temps (de 60% en 2008 à 72% en 2014, p<0,0001). Entre 2008 et 2014, le pourcentage de départements n’ayant pas fourni d’informations sur les issues de traitement est passé de 8,9% (n=9) à 3,0% (n=3), sans tendance significative pendant la période. Les cas avec une issue renseignée étaient comparables chaque année pour les principales caractéristiques sauf pour l’âge (p<0,0001), la proportion de personnes nées à l’étranger (p<0,0001), la proportion de cultures positives parmi le total des cas (p=0,015) et la proportion de cultures renseignées en début du traitement (p=0,004) qui augmentaient au cours du temps (tableau 2).
 Agrandir l'image
Agrandir l'imageLes groupes de patients avec une information sur l’issue de traitement (inclus dans l’analyse) et sans (exclus) étaient similaires pour certaines caractéristiques (âge (p=0,09), proportion de personnes nées à l’étranger (p=0,31), antécédents de tuberculose traitée (p=0,25), culture positive (p=0,73)) et différents pour d’autres. Dans le groupe de cas analysés, il y avait moins d’hommes (59,7% vs 60,9%, p=0,04) et moins de cas avec microscopie respiratoire positive (51,7% vs 53,2%, p=0,03), mais davantage de cas pulmonaires (72,3% vs 69,0%, p<0,0001) et plus de cas avec culture renseignée (62,7% vs 44,2%, p<0,0001).
Issues de traitement
Toutes formes de tuberculose confondues, 74,1% des cas avaient un traitement achevé, 19,8% une issue potentiellement défavorable, 4,8% étaient décédés sans lien avec la tuberculose ou avec un lien inconnu et 1,3% étaient non évaluables (tableau 3). Parmi les principales causes d’issues potentiellement défavorables, 44% étaient des perdus de vue, 25% des patients transférés, 13% des patients toujours en traitement à 12 mois, 9% des décès en lien avec la tuberculose et 9% des cas ayant arrêté et non repris leur traitement. La proportion de traitement achevé augmentait significativement avec le temps (p<0,001) alors que celles des décès (sans lien/lien inconnu avec la tuberculose) et des issues potentiellement défavorables diminuaient significativement avec le temps (p<0,001 pour chaque proportion).
 Agrandir l'image
Agrandir l'imageLes proportions de traitements achevés (p<0,001) et des cas non évaluables (p=0,043) diminuaient significativement avec l’âge, alors que celles des issues potentiellement défavorables (p=0,025) et des décès sans lien ou lien inconnu avec la tuberculose (p<0,0001) augmentaient significativement avec l’âge (figure 1). La proportion de départements ayant atteint au moins 85% de traitements achevés (seuil recommandé par l’OMS jusqu’en 2014) était de 13% en 2008 et 24,5% en 2014. La proportion de départements ayant une proportion de traitements achevés <70% était de 38% en 2008 et 23% en 2014 (figure 2).
 Agrandir l'image
Agrandir l'image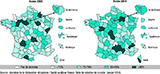 Agrandir l'image
Agrandir l'imageChez les cas pulmonaires, la proportion de traitements achevés était de 73,2% (70,6% chez les cas pulmonaires à microscopie positive et 74% chez les cas pulmonaires à culture positive). Parmi ces cas, 3 250 (20,2%) avaient une issue potentiellement défavorable, dont 1 445 (45%) perdus de vue, 831 (25%) transférés, 364 (11%) toujours en traitement, 322 (10%) décédés en lien avec la tuberculose et 288 (9%) des personnes ayant arrêté leur traitement. Un pourcentage de 1,2% des cas pulmonaires avaient une issue de traitement non évaluable.
Le pourcentage de traitement achevé était de 76,4% dans les formes exclusivement extra-pulmonaires.
Variation des issues potentiellement défavorables selon certaines caractéristiques du malade
Au total, en ayant exclu de l’analyse les décès sans lien avec la tuberculose et les patients dont l’issue de traitement n’est pas évaluable, 79% des patients avaient achevé leur traitement et 21% présentaient une issue potentiellement défavorable (tableau 4).
 Agrandir l'image
Agrandir l'imageLes issues potentiellement défavorables diminuaient d’année en année et leur fréquence variait selon les régions. Les issues potentiellement défavorables étaient significativement plus fréquentes chez les hommes, chez les malades très âgés, dans les formes cliniques pulmonaires, graves (méningées ou miliaires), contagieuses (Baar+) ou ayant une culture positive en début de traitement, chez les patients ayant des antécédents de tuberculose traitée par des antibiotiques, chez les personnes sans domicile fixe, résidant en collectivité, détenues, nées à l’étranger et résidant en France depuis moins de 2 ans, enfin chez celles n’ayant pas de profession à caractère sanitaire et social.
Les patients décédés représentaient 6,5% de la population (1 467/22 526). Parmi les décès sans lien avec la tuberculose (n=1 082), 73% survenaient après 64 ans et ce pourcentage était de 68% pour les décès en lien avec la tuberculose (n=385). Lorsqu’on observe dans cette population la part des décès liés à la tuberculose parmi l’ensemble des traitements achevés et des issues potentiellement défavorables, le pourcentage de ces décès décroit à partir de 2012 : 2,0% en 2008, 2,4% en 2009, 2,2% en 2010, 2,0% en 2011, 1,4% en 2012, 1,3% en 2013 et 1,4% en 2014 (chi2 de tendance : p=0,0003).
Discussion
Une surveillance améliorée
Suite aux deux publications sur les issues de traitement déclarées en France en 2008 et 2009 10,11, nous présentons dans cet article l’ensemble des résultats des issues de traitement depuis que celles-ci ont été mises à DO en 2007. Il s’agit de résultats importants compte tenu du grand nombre d’observations analysées sur une période de sept ans, permettant de constater de progrès dans la mise en œuvre de la surveillance des issues de traitement. Ceci est suggéré dans notre analyse par la diminution régulière du nombre de cas avec une issue de traitement non renseignée et par la diminution du nombre de départements qui n’ont pas fourni d’informations sur les issues de traitement, indiquant une meilleure déclaration des cas et peut-être un meilleur suivi. Cette amélioration pourrait s’expliquer par une plus grande sensibilisation des partenaires de cette surveillance, à travers la diffusion des données nationales 10,11, et à la discussion de cette problématique dans divers forums réguliers auxquels participent de nombreux acteurs de terrain (réunions biannuelles du réseau des Clat, Journée nationale Tuberculose organisée conjointement par la Direction générale de la santé, Santé publique France et le Centre national de référence des mycobactéries tous les deux ans). Bien qu’il soit nécessaire de l’avancer avec prudence, une hypothèse supplémentaire pour expliquer cette augmentation pourrait être une implication croissante des Clat dans la surveillance des issues de traitement (voir l’article de G Lailler et coll. dans ce même numéro 19). Ces résultats devraient encourager les différents acteurs de la lutte antituberculeuse à poursuivre les actions de contrôle menées chaque année.
Une meilleure prise en charge des patients
Notre analyse montre que le pourcentage de patients ayant achevé leur traitement a augmenté avec le temps. Même si cette augmentation est faible et inférieure à celle d’autres pays de l’Union européenne 16, elle suggère une meilleure prise en charge de ces patients. Cette tendance concerne l’ensemble du territoire national, puisque le pourcentage de départements ayant atteint un traitement achevé supérieur à 85% a presque doublé entre 2008 et 2014 ; ce n’est cependant pas le cas lorsque l’indicateur plus récent (et plus ambitieux) de 90% défini par l’OMS est utilisé : alors, ce pourcentage reste constant. La part des décès liés à la tuberculose est passée de 2,0% en 2008 à 1,4% en 2014. Ainsi, nous assistons en France à, d’une part, la baisse régulière de l’incidence de la maladie 3 et, d’autre part, à une augmentation du nombre de patients considérés comme guéris par le médecin. Il est très probable que ce dernier élément contribue à la baisse de l’incidence, puisque le but d’un traitement bien conduit est précisément de diminuer la transmission du bacille. Certains facteurs, comme une plus grande sensibilisation des cliniciens, une meilleure coordination entre les différents acteurs de la prise en charge du patient et le rôle central joué par les Clat, pourraient avoir eu un impact sur l’augmentation de la proportion de cas avec un traitement complété. Là encore, ces résultats sont encourageants et doivent conduire à poursuivre les efforts déjà entrepris.
Cependant, avec 74% de traitements achevés, les résultats de la France restent en-deçà des objectifs de l’OMS. Ce pourcentage atteignait en moyenne 78% dans les pays de l’Union européenne entre 2002 et 2011, mesuré sur les nouveaux cas pulmonaires à culture positive notifiés au Centre européen de prévention et contrôle des maladies (ECDC) 16. On note cependant que les méthodes de mesure des issues de traitement peuvent varier sensiblement entre pays, cette standardisation imparfaite pouvant limiter les comparaisons internationales 17. Limiter le nombre de patients perdus de vue et transférés et réduire le nombre global de décès (6,7% dans notre étude, très proche de la moyenne européenne de 6,5% 16 mais qui reste supérieur au seuil de 5% considéré comme acceptable par l’OMS 15) devrait permettre d’améliorer cet indicateur.
Limites de l’étude
Bien que ces résultats soient encourageants, ils doivent être interprétés avec une certaine prudence.
D’une part, environ un tiers des cas n’avait pas d’issue de traitement renseignée, et la comparaison de ce groupe avec celui dont l’issue était renseignée montre que ces deux populations diffèrent sur plusieurs caractéristiques. D’autre part, certains facteurs associés à l’issue de traitement mais non collectés dans la DO, tels que la consommation de drogues, d’alcool ou de tabac 20,21, l’infection par le VIH 22, le diabète 23 ou les conditions de vie défavorables 20,24, pourraient aussi différencier ces deux groupes et influer sur les résultats. Ces insuffisances dans le renseignement des issues de traitement s’expliquent, entre autres facteurs, par la difficulté à retrouver les malades 12 mois après la date du début du traitement, soit du fait d’adresses incomplètes dans les fiches de déclaration initiale, soit par l’absence d’indication du médecin ayant fait la déclaration initiale de tuberculose. En outre, le médecin déclarant la tuberculose et initiant le traitement peut ne pas être celui qui va suivre le patient pendant le traitement, la déclaration initiale pouvant être faite par exemple par un interne travaillant dans un service hospitalier et ayant quitté le service à la fin du semestre.
D’autre part, les patients transférés ont été classés dans la catégorie des issues potentiellement défavorables, comme recommandé par l’OMS. Or, en France, l’organisation de la prise en charge des patients fait intervenir plusieurs interlocuteurs, la prise en charge initiale à l’hôpital pouvant être suivie par un transfert dans un autre établissement ou en médecine ambulatoire. La demande d’information sur l’issue de traitement étant faite au médecin ayant fait le diagnostic initial de tuberculose, celui-ci renseigne la catégorie « patient transféré » qui ne préjuge pas si le traitement a été achevé ou si l’issue a été potentiellement défavorable. Si on considère que certains de ces patients transférés ont en fait été guéris à la fin du traitement, ce qui est probable, le pourcentage de traitements achevés dans notre étude sous-estimerait le pourcentage réel dans cette population de malades.
À noter que la DO sous-estime le nombre réel de cas MDR en France d’environ 50% par rapport au nombre indiqué par le Centre national de référence des mycobactéries (CNR MyRMA), car les résultats de l’antibiogramme ne sont pas toujours notés dans la DO. De ce fait, certains cas de tuberculose MDR n’ont pas pu être identifiés dans notre fichier et ont donc été analysés comme des tuberculoses sensibles. Quoi qu’il en soit, ces cas a priori peu nombreux ont vraisemblablement été classés dans la DO comme des cas dont le traitement était initialement prévu pour une durée supérieure à 12 mois et donc exclus de notre analyse, sans conséquence sur nos principaux résultats.
Enfin, dans l’analyse de déterminants d’issues potentiellement défavorables, nous ne présentons pas de résultats d’analyse multivariée. Ce choix est dû à l’existence de nombreuses données manquantes, nécessitant une analyse en imputations multiples dont les résultats seront publiés ultérieurement. Cependant, en raison d’un effectif important et des associations très significatives retrouvées dans l’analyse univariée, nous formulons l’hypothèse que le risque que les déterminants d’issue potentiellement défavorable identifiés ne soient plus présents après analyse multivariée est très faible.
Recommandations
La réduction du nombre de patients transférés ou perdus de vue et la bonne récupération de l’information sur l’issue de traitement chez ces patients sont deux leviers qui permettraient de mieux renseigner les issues de traitement. Il est donc nécessaire d’améliorer le recueil d’informations et de sensibiliser les professionnels de santé à cette surveillance. Une coordination plus étroite entre les différents partenaires de la surveillance, une meilleure documentation de l’adresse du patient et des échanges avec un médecin déclarant référent travaillant de façon pérenne dans un établissement hospitalier devraient favoriser une meilleure complétude des données. La télé-déclaration de la tuberculose en ligne directement par le médecin déclarant, projet actuellement en cours de développement, devrait faciliter et simplifier l’accès au dispositif de surveillance ainsi que les modalités de déclaration, simplifier le circuit entre les différents acteurs de la déclaration, réduire la charge de travail liée au remplissage des fiches par les déclarants et in fine, nous l’espérons, rendre ce système de surveillance plus efficace.
Par ailleurs, la surveillance des issues de traitement doit être renforcée, principalement dans les catégories de la population où le pourcentage de patients guéris est le plus faible. Nos premiers résultats comparant le risque d’issues potentiellement défavorables selon certaines caractéristiques cliniques, sociales ou démographiques fournissent des pistes pour cibler ces actions. La prise en compte de ces facteurs pourrait permettre de mieux orienter les efforts de surveillance et le suivi des patients tuberculeux. Ils devraient aider les cliniciens et professionnels de santé publique impliqués dans la prise en charge de ces patients à mieux connaitre les déterminants associés à la non complétion des traitements et à adapter la prise en charge en fonction des groupes à risque. Ces données contribueront aussi à générer des hypothèses à l’origine d’études complémentaires permettant de mieux comprendre les raisons des différences observées. L’analyse multivariée en cours permettra de confirmer ces premiers résultats.
Conclusion
La surveillance des issues de traitement permet de mesurer les efforts de la lutte antituberculeuse, qui repose sur une collaboration étroite entre les différents acteurs de cette surveillance et sur leur capacité à travailler ensemble. Les données fournies dans cet article sont encourageantes et devraient inciter ces différents acteurs à poursuivre et à renforcer cette surveillance. Une meilleure connaissance des raisons de non complétion des traitements est nécessaire pour pouvoir adapter la prise en charge et anticiper son éventuel échec. Cela permettra de compléter un traitement inachevé, limitant ainsi la transmission de l’infection à d’autres personnes et le développement de résistances aux antituberculeux. L’ensemble de ces mesures, associées à la poursuite des efforts d’amélioration du dépistage des cas, contribuera à une meilleure maitrise de la tuberculose en France.
Remerciements
Nous remercions les médecins et biologistes déclarants et les personnels des Clat et des ARS qui contribuent à l’amélioration de la qualité des données de surveillance de la tuberculose. Merci à Fatima Aït Belghiti (Santé publique France) pour sa contribution au processus de collecte et de validation des fichiers de données. Merci à Didier Che (Santé publique France) pour sa relecture attentive de la dernière version de ce manuscrit et à Mireille Allemand (Santé publique France) pour l’élaboration des cartes.




