La leptospirose humaine en Guyane : état des connaissances et perspectives
// Human leptospirosis in French Guiana: current knowledge and perspectives
Résumé
La leptospirose est une zoonose cosmopolite causée par les bactéries du genre Leptospira. Le climat chaud et humide de la zone intertropicale est particulièrement propice à son expansion. En Guyane, département français situé au nord-est du continent sud-américain, en région amazonienne, elle semble rare. L’objectif de cet article est de récapituler l’état des connaissances actuelles sur l’épidémiologie de leptospirose humaine en Guyane et de discuter les perspectives pour en améliorer la surveillance.
Les publications sur la leptospirose en Guyane sont rares et anciennes, datant des années 1940-1995. Les rapports annuels du Centre national de référence de la leptospirose (CNR, Institut Pasteur de Paris) montrent un nombre annuel de cas assez stable entre 1996 et 2012, variant de 6 à 18 selon les années, avec une augmentation importante de 2013 à 2015 : respectivement 36, 92 et 67 cas par an. Une étude rétrospective menée récemment sur les cas survenus entre 2007 et 2014, identifiés avec des critères diagnostiques très stricts, a comptabilisé 72 cas sur le département, parmi lesquels 12 (16,7%) cas graves et 3 (4,2%) décès. La maladie touchait principalement des hommes (86,1%) âgés de 20 à 49 ans (63,9%).
Il est probable que la leptospirose soit une maladie négligée dans la région, du fait de l’absence d’outils diagnostiques rapidement disponibles, de la méconnaissance des cliniciens de cette pathologie et de la présence de nombreuses autres pathologies à symptômes cliniques similaires en phase aiguë (paludismes, arboviroses, fièvre Q, toxoplasmose amazonienne). La mise en place d’études de plus grande ampleur est nécessaire pour connaître le véritable impact de cette maladie en Guyane.
Abstract
Leptospirosis is a cosmopolitan zoonosis caused by the bacteria of the genus Leptospira. The warm and wet climate of the intertropical zone is particularly favorable with its expansion. In French Guiana, a French territory located at the North-East of the South American continent in Amazonian area, it seems to be rare. The objective of this article is to make the inventory of current knowledge on the epidemiology of human leptospirosis in French Guiana, and to discuss the prospects concerning this disease and improve its surveillance. Publications on leptospirosis in French Guiana are rare and old, and date from 1940 to 1995. The annual reports of the National Reference Centre of Leptospirosis (NRC, Pasteur Institute) show a quite stable annual number of cases, varying from 6 to 18 between 1996 and 2012, depending on the year, with a significant increase from 2013 to 2015, respectively 36, 92 and 67 cases a year. A retrospective study conducted recently on the cases which occurred between 2007 and 2014 with very strict inclusion criteria, identified 72 cases on the territory, among whom 12 (16.7%) severe cases and 3 (4.2%) deaths. The disease affects mainly men (86.1%) aged between 20 and 49 years (63.9%). It is probable that leptospirosis is a neglected disease in the region, due to the absence of quickly available diagnostic tools, the lack of awareness of clinicians on this pathology, and the existence of many other infectious agents with similar clinical presentations during acute episodes (such as malarias, arboviruses, Q fever and Amazonian toxoplasmosis). The implementation of larger studies is necessary to know the true burden of this disease in French Guiana.
Introduction
La leptospirose est une zoonose cosmopolite causée par les bactéries de l’ordre des spirochètes et du genre Leptospira. Vingt-deux espèces sont décrites, une trentaine de sérogroupes et plus de 300 sérovars 1. Cette zoonose est particulièrement fréquente en zone intertropicale 2.
La leptospirose est considérée comme un problème de santé publique en Nouvelle-Calédonie, Wallis et Futuna et Polynésie française 3,4, à La Réunion et Mayotte 5,6 et aux Antilles françaises (Guadeloupe et Martinique) 7.
En Guyane, département français d’Amérique situé sur la côte nord-est du continent sud-américain, en région amazonienne, la leptospirose a longtemps été considérée comme anecdotique, bien que des données récentes semblent montrer qu’elle y est probablement plus fréquente qu’admis jusqu’alors 8. L’objectif de cet article est de faire un état des lieux des connaissances sur la leptospirose en Guyane, sur la base de différents travaux menés par un groupe de travail incluant des chercheurs des Centres hospitaliers (CH) de Cayenne et de Saint-Laurent du Maroni, de l’Institut Pasteur de la Guyane et du Centre national de référence de la leptospirose (CNR) à l’Institut Pasteur de Paris. Sont récapitulés ici une revue exhaustive de la littérature ancienne, une analyse des rapports annuels du CNR et une étude rétrospective menée dans les CH de Cayenne et de l’Ouest guyanais.
Données épidémiologiques connues sur la leptospirose humaine en Guyane
Données historiques
La première publication sur un cas de leptospirose en Guyane date de 1940 9. Les publications ultérieures, entre 1940 et 1980, rapportaient des petites séries de cas, principalement à Cayenne 10,11,12,13,14,15, puis deux séries de 22 et 11 patients à Saint-Laurent du Maroni, respectivement en 1986 et 1995, dont la dernière concernait exclusivement des femmes enceintes 16,17,18. Ainsi, entre 1940 et 1995, 72 cas de leptospirose humaine biologiquement confirmés et hospitalisés ont été répertoriés en Guyane 8. Les femmes y étaient plus fréquemment représentées qu’habituellement retrouvé dans la littérature, avec un sex-ratio homme/femme de 1,8 (30 hommes pour 17 femmes), probablement en raison de la série spécifique de femmes enceintes 16. L’âge médian des patients était de 29 ans (Q25-Q75: 24-39 ; min-max : 3-63 ans). Le sérogroupe a pu être identifié pour 54 cas, parmi lesquels Icterohaemorrhagiae était le plus fréquemment retrouvé (43/54 cas). Cependant, de nombreux autres sérogroupes étaient également rapportés. La létalité était de 14%, avec 7 décès parmi les 50 patients pour lesquels l’information était disponible. L’étude portant sur 11 cas de leptospirose pendant la grossesse relevait plus de 50% de décès fœtaux 16.
Données du CNR
Le CNR de la leptospirose publie chaque année, depuis 1996, un rapport sur le nombre de cas et la répartition des espèces et sérogroupes pour chaque département français, outre-mer compris. Les données guyanaises ont été colligées et rapportées au nombre d’habitants fourni par les chiffres du recensement de l’Institut national de la statistique et des études économiques (Insee). Elles indiquent une incidence annuelle relativement stable entre 1996 et 2011, avec un nombre de cas variant, selon les années, de 6 à 18, soit des taux d’incidence de 4 à 10 pour 100 000 habitants par an (figure 1) 8,19. Une nette augmentation des cas est observée à partir de 2012, leur nombre annuel passant de 25 en 2012 à 36 en 2013, puis 92 en 2014, soit une incidence annuelle de, respectivement, 11, 15 et 39 pour 100 000 habitants par an. Avec de tels chiffres, la Guyane devient l’un des territoires où l’incidence de la leptospirose est parmi les plus élevées au monde 2. Cette augmentation de l’incidence est à interpréter à l’aune d’une plus grande disponibilité des techniques diagnostiques, notamment l’envoi plus fréquent pour diagnostic précoce par Polymerase Chain Reaction (PCR), réalisée en laboratoire privé en France métropolitaine, et l’utilisation de la technique Elisa IgM, disponible depuis 2012 à l’Institut Pasteur de Guyane. L’augmentation du nombre des cas à partir de 2013 est principalement due à un plus grand nombre de tests positifs en Elisa IgM, non confirmés par MAT (test de micro-agglutination) au CNR. Cette discordance peut être interprétée sous deux angles différents : excès de sensibilité du test IgM ou défaut de sensibilité du test MAT. Ainsi, un titre d’IgM positif ne signe pas le diagnostic de leptospirose car ce test, très sensible, a une spécificité variant de 60% à 82% selon le kit utilisé 20. Il existe probablement des phénomènes d’immunité croisée, et une augmentation du titre d’IgM anti-leptospire est observée au cours d’infections telles que la dengue ou la fièvre Q. À l’inverse, le MAT est une technique qui peut être mise en défaut, notamment à la phase précoce, où une augmentation des IgM précède la positivation du MAT. Enfin, cette discordance entre IgM et MAT suggère l’existence de sérogroupes inconnus en Guyane, non détectés par le MAT. Si Icterohaemorrhagiae est le sérogroupe le plus représenté avec 34% des identifications en MAT, 17 autres sérogroupes ont été identifiés depuis 1996, traduisant une grande diversité (figure 2).
 Agrandir l'image
Agrandir l'image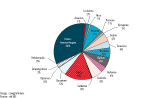 Agrandir l'image
Agrandir l'imageÉtude rétrospective 2007-2014
Une étude rétrospective transversale multicentrique a été menée sur la période 2007-2014 dans les CH de Cayenne et de Saint-Laurent du Maroni, afin de déterminer les particularités épidémiologiques et clinico-biologiques des patients atteints de leptospirose en Guyane 21. Les patients ont été identifiés à partir des résultats positifs au CNR et au laboratoire Cerba sur la période d’étude, puis les données épidémiologiques et cliniques ont été obtenues en consultant les dossiers médicaux des deux hôpitaux. Les critères d’inclusion ont été très stricts. Les cas potentiels de leptospirose ont été identifiés en combinant les résultats sérologiques (Elisa IgM et MAT) et de biologie moléculaire (PCR) positifs. Une sélection de chaque dossier a été réalisée et les cas ont été classés en trois groupes :
-cas certains : PCR positive dans un échantillon biologique, ou séroconversion MAT ≥200, ou séroascension MAT avec multiplication du titre par 4, ou titre MAT ≥400 sur au moins un prélèvement ;
-cas probable : Elisa IgM >800 et titre MAT ≥100 sur au moins une sérologie, ou séroconversion IgM avec MAT ≥100 sur au moins une sérologie, ou séroconversion MAT avec titre maximal à 100 ;
-ont été exclus les cas peu probables : séroconversion MAT ≤100 sans Elisa IgM Pasteur significatif au CNR et/ou avec un autre diagnostic prouvé, ainsi que les patients pour lesquels aucun dossier médical n’était disponible.
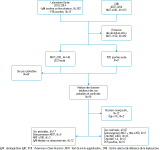
Soixante-douze patients ont été retenus, dont 17 cas probables et 55 cas certains, répartis en 70 patients du CH de Cayenne et 2 du CH de l’Ouest guyanais (figure 3). Le nombre annuel de cas de leptospirose retenus dans cette étude rétrospective est inférieur aux chiffres fournis par le CNR, qui retrouvait pour les années 2012, 2013 et 2014, respectivement 25, 36 et 92 cas, alors que l’étude n’en a retenu, respectivement, que 14, 16 et 12. Cette discordance entre les résultats de l’étude rétrospective et les données publiées par le CNR résulte des critères d’exclusion, très stricts. Cette étude retrouve néanmoins la tendance à l’augmentation du nombre de cas de leptospirose en Guyane, qui peut s’expliquer par une recherche plus systématique de la maladie et par les nouvelles techniques diagnostiques, comme cela a été observé dans les autres DOM-TOM. Cependant, pour prouver cette augmentation il faut utiliser un titre MAT>400 en zone de forte incidence, un titre test Elisa IgM supérieur à 400 suivi d’un test MAT de confirmation ou mieux la PCR. Or le titre MAT >100 utilisé ici était celui d’une zone de faible incidence.
 Agrandir l'image
Agrandir l'imageParmi ces patients, 62 (86,1%) étaient des hommes (sex-ratio H/F=6,2), d’âge médian 39 ans (Q25-Q75: 29-50,3 ; min-max 16-82) et les patients âgés de 20 à 49 ans représentaient 63,9% des cas (figure 4). Pour les patients pour lesquels les données étaient disponibles, 40/66 (61%) étaient nés à l’étranger et, parmi les 26 nés en France, 9 (14%) étaient nés en métropole et 17 en Guyane ou aux Antilles françaises. Les patients nés au Brésil étaient fortement représentés, avec presque 25% des cas. La majorité des patients résidait à Cayenne et ses environs, soit 45/72 (63%), suivie de Maripasoula (8/72, 11%) et de Saint-Laurent du Maroni (4/72, 6%) (figure 5).
 Agrandir l'image
Agrandir l'image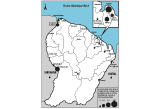 Agrandir l'image
Agrandir l'imageLa répartition annuelle des cas était fortement et positivement corrélée à la pluviométrie (coefficient de corrélation de Spearman rho=0,287, p=0,0046) (figures 6 et 7). Du fait du caractère rétrospectif de l’étude, les facteurs d’exposition étaient rarement disponibles. Cependant, une activité professionnelle à risque était retrouvée dans 64% (31/48) des cas, notamment l’orpaillage (1) (12/31) et les travaux publics (7/31). Une activité extraprofessionnelle à risque était rapportée dans 79% des cas (23/29), notamment la baignade en rivière forestière (13/16), la proximité de rongeurs avec le domicile (13/20), le jardinage (7/9) et les travaux d’entretien extérieurs (7/9).
 Agrandir l'image
Agrandir l'image Agrandir l'image
Agrandir l'imageParmi les 72 cas identifiés, 62 (86%) avaient été pris en charge en hospitalisation, dont 12 (17%) en réanimation, avec des critères de gravité habituellement reconnus dans la littérature (utilisation d’amines vasopressives et/ou ventilation mécanique et/ou nécessité d’une épuration extra-rénale). Parmi les autres atteintes sévères, on notait une hépatite fulminante dans 2 cas (3%) et un syndrome hémorragique majeur dans 2 cas (3%). L’atteinte pulmonaire était fréquente : les patients rapportaient de la toux dans 47% (32/70) des cas, une anomalie à l’auscultation était retrouvée dans 27% (19/71) des cas et une anomalie parenchymateuse était retrouvée chez 23 (36%) des 64 patients ayant bénéficié d’une radiographie thoracique. Trois personnes (4%) étaient décédées. Le diagnostic de leptospirose n’était évoqué à la prise en charge initiale que chez 14 patients, soit 20% des cas, mais 56 patients (78%) avaient reçu une antibiothérapie initiale, dont 85% par β-lactamines.
Particularités épidémiologiques de la leptospirose en Guyane
En Guyane française, territoire recouvert à 98% par de la forêt équatoriale 22, toutes les conditions sont réunies pour le développement de la leptospirose, notamment un climat caractérisé par des pluies abondantes et des températures élevées toute l’année, la présence de nombreux cours d’eau et des contacts étroits avec les animaux domestiques et la faune sauvage, notamment lors d’activités en pleine nature telles que l’extraction d’or (orpaillage) et les activités scientifiques ou sportives 23,24. L’abondance des rongeurs réservoirs de la leptospirose en zone urbaine et la forte croissance démographique urbaine sont des facteurs favorisants supplémentaires 24.
Comme justement souligné dès 1940 par Floch et coll., la connaissance de cette infection est directement liée à l’intérêt qu’y porte la communauté médicale ainsi qu’aux moyens diagnostiques disponibles, et la leptospirose est probablement plus fréquente qu’il n’y parait en Guyane 9,10,11. Aujourd’hui, la leptospirose est reconnue comme un problème de santé publique majeur aux Antilles françaises, où elle a fait l’objet d’études et de développements techniques locaux, alors qu’elle est toujours considérée comme anecdotique en Guyane, où peu de moyens lui sont dédiés.
Il existe probablement une sous-estimation de l’incidence réelle de la leptospirose en Guyane. Les explications de ce phénomène sont multiples, d’ordre à la fois clinique et microbiologique. En effet, la leptospirose, dans sa forme non sévère, a une présentation clinique souvent aspécifique, associant de la fièvre à des douleurs multiples et, en biologie, un syndrome inflammatoire avec une atteinte rénale et hépatique inconstante et modérée. Les diagnostics différentiels apparaissent particulièrement nombreux en Guyane : paludismes à Plasmodium falciparum et P. vivax, fièvre Q, toxoplasmose amazonienne, arboviroses épidémiques et/ou endémiques (dengue, chikungunya, Zika et arboviroses plus rares telles que les infections par les virus Tonate et Mayaro) 25,26,27,28,29,30. La fièvre Q, infection bactérienne due à Coxiella burnetii, est le principal diagnostic différentiel de la leptospirose, de par son incidence très élevée en Guyane, probablement la plus élevée au monde, sa présentation pulmonaire dans plus de 90% des cas et ses caractéristiques cliniques et biologiques proches : fièvre, syndrome algique, frissons, absence de point d’appel évident à l’examen clinique et présence fréquente au bilan biologique d’une thrombopénie et d’une élévation de la CRP et des transaminases. Le diagnostic de leptospirose n’est que rarement évoqué par les soignants en première intention du fait d’un possible manque de sensibilisation à cette pathologie, contrairement aux diagnostics cités précédemment et recherchés en routine face à une fièvre. En outre, il est probable que des cas de leptospirose soient traités efficacement par l’antibiothérapie probabiliste devant un tableau infectieux non spécifique d’allure bactérienne.
Si le diagnostic microbiologique du paludisme et de la dengue peut être fait rapidement (frottis sanguin, antigénémie NS1, tests diagnostiques rapides), il n’en est pour l’instant pas de même pour la leptospirose. La méthode diagnostique de référence à la phase aiguë (<7 jours) est la PCR, qui ne peut être réalisée actuellement dans le département, retardant la réception des résultats. À la phase plus tardive, le diagnostic repose sur un test commercial Elisa IgM, peu spécifique, mais dont le seuil peut être réajusté par les biologistes en fonction de l’épidémiologie locale, et confirmé jusqu’à récemment par MAT. Ce dernier test nécessite souvent d’être répété afin d’évaluer la cinétique du titre des anticorps avant d’affirmer ou non le diagnostic et d’identifier le sérogroupe responsable de l’infection.
Modalités de surveillance et perspectives
La leptospirose n’étant pas une maladie à déclaration obligatoire, les données fournies annuellement par le CNR représentent jusqu’à aujourd’hui l’unique dispositif de surveillance spécifique. Mais avec la multiplication des laboratoires réalisant les examens diagnostiques, notamment la PCR sur le sang et les IgM, passés récemment à la nomenclature (c’est-à-dire remboursés par l’Assurance maladie), et l’exclusion du MAT de la nomenclature, le rendant désormais à la charge du patient, les prélèvements seront envoyés de façon beaucoup moins systématique au CNR dont les données annuelles seront de moins en moins représentatives de la véritable incidence de la maladie.
Une étape essentielle pour bien estimer l’incidence de la maladie et pour un diagnostic rapide et optimal des patients est la disponibilité immédiate d’outils diagnostiques, notamment de la PCR, sur le département. Des acteurs de santé locaux et nationaux sont désormais impliqués dans plusieurs projets visant à améliorer la connaissance de la leptospirose et de son incidence en Guyane. Ils permettront de mettre en place un système de surveillance actif et pérenne.




