Traitements antibiotiques en établissement de santé : résultats de l’Enquête nationale de prévalence 2017, France
// Antimicrobial treatments in healthcare facilities: Results of French National Point Prevalence Survey, 2017
Résumé
Un des objectifs de l’Enquête nationale de prévalence (ENP) 2017 était de mesurer et de décrire la prévalence des patients traités par antibiotique en établissement de santé et de la comparer aux données de l’ENP 2012.
L’enquête a été réalisée sur un échantillon représentatif des établissements de santé français par sondage aléatoire avec stratification sur la région et la catégorie d’établissement. Entre le 15 mai et le 30 juin 2017, 403 établissements de santé ont participé et 80 988 patients ont été inclus.
La prévalence des patients traités par antibiotique a diminué en 2017 (15,12%, IC95% [14,22-16,06]) alors qu’elle était stable entre 2006 et 2012 (16,60%). Elle a en particulier diminué dans plusieurs secteurs de soins : en obstétrique, en soins de suite et de réadaptation (SSR) et en soins de longue durée (SLD). Elle restait la plus élevée dans les services de réanimation, secteur dans lequel un patient sur deux était traité par antibiotique.
La prévalence des patients traités par antibiotique a diminué chez les enfants de moins de 15 ans et les patients âgés de plus de 65 ans, ainsi que chez les patients les moins fragiles (patients non immunodéprimés et ceux atteints d’une maladie non fatale), ce qui pourrait suggérer un usage mieux maîtrisé des antibiotiques chez ces groupes de patients.
La dose d’antibiotique prescrite s’écarte à la hausse de la dose définie journalière (DDJ) pour l’amoxicilline et l’association amoxicilline-acide clavulanique, comme rapporté dans la littérature.
La durée des antibioprophylaxies chirurgicales, souvent prolongées au-delà de 24 heures, pose question au regard des recommandations actuelles. Elle n’a pas baissé depuis 2012 sauf dans les services de chirurgie orthopédique et traumatologique.
Un traitement sur cinq a fait l’objet d’un changement pour le même motif de prescription. Ce changement conduit plus fréquemment à une escalade qu’à une désescalade thérapeutique.
La baisse de la prévalence des patients traités par antibiotique encourage à poursuivre les actions en faveur du bon usage des antibiotiques.
Abstract
One of the objectives of the 2017 National Point Prevalence Survey (PPS) was to measure and describe the prevalence of patients treated with antibiotics in healthcare facilities, and to compare it with results of ENP from 2012.
The survey was carried out on a representative sample of French healthcare institutions by random sampling with stratification by region and category of facility. Between 15 May and 30 June 2017, 403 healthcare facilities participated in the study, and 80,988 patients were included.
The prevalence of patients treated with antibiotics decreased in 2017 (15.12%, 95%CI: [14.22-16.06]), whereas it was stable between 2006 and 2012 (16.60%). In particular, it decreased in several healthcare sectors: obstetrics, follow-up and rehabilitation care, and long-term care (LTC). It remained highest in intensive care, where, like in 2012, one in two patients was treated with antibiotics.
The prevalence of patients treated with antibiotics decreased in children under 15 years of age and patients over 65 years of age, as well as in the least frail patients (non-immunocompromised patients and those with a non-fatal disease), which may suggest more controlled use of antibiotics in these groups of patients.
The antibiotic dose prescribed is higher than the defined daily dose (DDD) for amoxicillin and the combination amoxicillin-clavulanic acid, as reported in the literature.
The duration of surgical antibiotic prophylaxis, often extended beyond 24 hours, is questionable under current recommendations. It has not decreased since 2012 except in the orthopedic surgery and trauma services.
One in five treatments was changed for the same reason for prescription. Changing antibiotics leads more frequently to escalation than to therapeutic de-escalation.
The decrease in the prevalence of patients treated with antibiotics encourages further action to promote the proper use of antibiotics.
Introduction
Une enquête nationale de prévalence des infections associées aux soins en établissement de santé (ES) a lieu tous les cinq ans en France depuis 1996. Elle comprend depuis 2001 un volet concernant les traitements anti-infectieux (AI) chez les patients hospitalisés, qui a évolué depuis 2012 en cohérence avec le protocole européen de l’European Centre for Disease Prevention and Control (ECDC) 1. Ainsi, plusieurs questions supplémentaires comme la dose d’AI ou le changement de traitement ont été introduites dans le questionnaire en 2017 pour renforcer la description des prescriptions d’AI.
Ce volet sur la consommation antibiotique (ATB) de l’ENP 2017 avait pour objectifs de mesurer la prévalence des patients traités par ATB dans les ES en France, de décrire les traitements ATB prescrits notamment par molécule, famille et grande catégorie d’indication et de comparer ces résultats avec ceux de l’ENP 2012. Il s’agissait également de mettre à disposition les données produites au niveau national et régional et de renforcer la sensibilisation des ES au suivi de la consommation d’ATB (objectifs non abordés dans cet article).
Matériel et méthode
Cette enquête transversale réalisée entre le 15 mai et le 30 juin 2017 a utilisé des méthodes standardisées décrites par ailleurs 2,3.
Le recueil de données portait sur les caractéristiques des ES (statut juridique, catégorie, région et présence d’une procédure de réévaluation des prescriptions ATB dans les 72 heures à partir de la dispensation initiale par une autre personne ou équipe que le prescripteur) et des patients (âge, sexe, service prenant en charge le patient, score de McCabe 4, déficit immunitaire (oui/non). Pour chaque patient, la présence d’un ou plusieurs traitements AI à visée systémique (ATB ou antifongique) administré au patient le jour de l’enquête était renseignée.
Pour chaque molécule d’AI étaient renseignés : 1) sa dénomination commune internationale (DCI) et sa classification ATC5 ; 2) l’indication de l’AI (i.e. contexte de prescription curatif pour infection communautaire ou nosocomiale, antibioprophylaxie (ATBP) chirurgicale ou prophylaxie médicale, indication non infectieuse) ; 3) le diagnostic principal ayant motivé le traitement AI ; 4) la dose prescrite journalière (DPJ) d’AI ; 5) la voie d’administration ; 6) la durée du traitement AI au jour de l’enquête depuis le début du traitement ; 7) le changement éventuel de traitement et la raison de ce changement et 8) la documentation du motif de prescription dans le dossier médical comme indicateur de qualité de la prescription. Il était possible de renseigner jusqu’à quatre traitements AI par patient.
Les définitions des variables étaient données dans le guide de l’enquêteur 2. La saisie des données était réalisée par les ES à l’aide d’un outil Web de saisie en ligne développée par le Centre d’appui pour la prévention des infections associées aux soins (CPias) Bretagne.
L’indicateur principal était une estimation de la prévalence des patients traités par au moins un ATB (PPT) à usage systémique (à l’exception des ATB locaux) 5 pour 100 patients hospitalisés avec son intervalle de confiance à 95% (IC95%). Les traitements antifongiques ont été exclus de cette analyse. Des rapports de prévalences des patients traités par antibiotique (RPPT) ont été calculés en analyse univariée (modèle de Poisson avec offset) pour différents facteurs de risques d’infection chez le patient : âge, sexe, score de McCabe, immunodépression. La PPT a été stratifiée par type de séjour du patient, contexte de prescription, voie d’administration, diagnostics de l’infection associée au traitement et, enfin, par molécule d’ATB prescrite. L’évolution entre 2012 et 2017 des prévalences ou des proportions brutes a été calculée par un taux d’accroissement.
La comparaison de la PPT de 2012 et 2017 a été également réalisée à l’aide de modèles multiniveaux (modèle de Poisson avec constantes aléatoires) prenant en compte la nature hiérarchique des données au niveau patient, ES et région et en ajustant sur l’âge, le sexe, le score McCabe, le type de séjour du patient et son statut immunitaire.
Pour les principaux ATB, la moyenne et la distribution des doses prescrites journalières (DPJ) exprimées en percentiles ont été calculées pour 100 patients. La DPJ des principaux ATB a été comparée à la dose définie journalière (DDJ) par le calcul du rapport DPJ/DDJ. Les valeurs des DDJ utilisées étaient celles en vigueur au 1er janvier 2017 6. Pour permettre de décrire la distribution de l’écart entre DDJ et DPJ par molécule d’ATB, ce rapport a été calculé pour chaque prescription, hors services de néonatologie ou de pédiatrie pour lesquels les DDJ ne sont pas adaptées, et uniquement lorsque la voie d’administration de l’ATB était renseignée. La comparaison DPJ/DDJ obtenue pour chaque prescription d’ATB a été répartie en trois classes : 1) la DPJ est inférieure à la DDJ d’au moins un facteur 2 (soit DPJ≤0,5 DDJ) ; 2) la DPJ est équivalente ou proche de la DDJ de moins d’un facteur 2 (soit 0,5 DDJ<DPJ<2 DDJ) ; 3) la DPJ est supérieure à la DDJ d’au moins un facteur 2 (soit DPJ≥2 DDJ). Les pourcentages de répartition des écarts dans les différentes classes ont été détaillés pour les principaux ATB.
L’analyse des données a été réalisée avec le logiciel STATA® 14.2.
Résultats
La participation des ES à l’enquête et les caractéristiques des patients sont décrites dans l’article consacré aux infections associées aux soins publié dans ce même numéro 3.
En France en 2017, 15,38% (IC95%: [14,48-16,33]) des patients hospitalisés inclus étaient traités par AI, dont 98,3% [98,0-98,5] recevaient au moins un ATB, soit une PPT de 15,12% [14,22-16,06]. La PPT observée en 2017 était plus basse que celle observée en 2012 (16,6%, soit une baisse de 8,9%). En analyse multivariée, après ajustement sur les caractéristiques des patients, cette diminution de la PPT était confirmée (p=0,009) mais plus faible (diminution relative : -1,3%).
Les patients traités par ATB en 2017 recevaient en moyenne 1,32 molécule d’ATB [1,30-1,34] et 1,34 molécule d’ATB en 2012. Par rapport à 2012, la proportion de patients recevant une seule molécule parmi les patients traités par ATB a augmenté légèrement passant de 71,3% en 2012 à 72,7% [71,5-73,9] en 2017. À l’inverse, la proportion de patients recevant deux molécules a diminué passant de 24,4% en 2012 à 23,3% [22,3-24,3] en 2017. La proportion de patients recevant trois molécules d’ATB ou plus est restée inchangée : 4,3% en 2012 et 4,0% [3,4-4,7] en 2017.
La PPT en intention curative en 2017 était égale à 12,22% [11,39-13,09]. Parmi ces traitements curatifs, les patients traités pour infection communautaire étaient plus fréquents (PPT=8,14% [7,55-8,77]) que ceux traités pour infection nosocomiale (PPT=4,14% [3,80-4,52]). La prévalence des patients avec ATBP chirurgicale était égale à 1,35% [1,17-1,56] et à 1,20% [1,05-1,38] pour les patients avec ATBP médicale. Les contextes de prescription multiples (i.e. association pour une même molécule d’un traitement curatif et prophylactique) correspondaient à une PPT de 0,19% [0,11-0,21] et celle pour une indication non infectieuse (par exemple à visée anti-inflammatoire) ou inconnue était égale à 0,39% [0,32-0,47]. Les PPT ont diminué entre 2012 et 2017 pour les infections nosocomiales (-13%) et pour les ATBP chirurgicales (-32%). En revanche, les PPT pour les autres indications sont restées stables.
La PPT variait selon l’ES. Parmi les ES ayant inclus 20 patients ou plus (n=382/403 ES), la médiane des PPT par ES était égale à 10,39% [9,09-12,5]. Un quart des ES avait une PPT inférieure à 4,40% [4,00-5,26] et un autre quart une PPT supérieure à 18,79% [17,24-20,36]. La diminution globale de la PPT entre 2012 et 2017 s’observait uniquement dans les ES du secteur public (-10%). La PPT variait selon la catégorie d’ES et selon l’ES au sein d’une même catégorie d’ES (figure 1). La PPT était beaucoup plus variable dans les cliniques MCO que dans les centres hospitaliers (CH). Par catégorie d’ES, cette diminution s’observait dans les ES de soins de suite et de réadaptation (SSR) (-15%), ainsi que dans les CH (-10%) notamment de plus de 300 lits (-6%). La PPT en Centre hospitalier régional/universitaire (CHR/CHU) n’a pas évolué entre 2012 (22,71%) et 2017 (21,53% [18,88-24,43]).
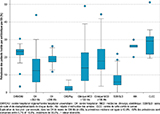 Agrandir l'image
Agrandir l'imageEn 2017, la PPT variait également selon le type de séjour, avec la PPT la plus élevée en réanimation, service dans lequel un patient sur deux était traité par ATB (tableau 1). En court séjour, la PPT était la plus faible en gynécologie-obstétrique. Par rapport à 2012, on constate une diminution de la PPT en médecine (-5%), en obstétrique (-21%), en service de moyen (SSR) (-19%) et de long séjour (SLD) (-16%). La prévalence des PPT en réanimation n’a pas évolué entre 2012 (48,77%) et 2017 (50,25% [45,43-55,06]). Enfin, la PPT variait selon la région avec la prévalence la plus élevée observée en région Île-de-France (excepté la Guyane dont l’effectif de patients est faible) et la plus faible en région Pays de la Loire (figure 2).
 Agrandir l'image
Agrandir l'image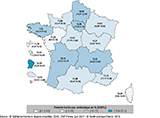 Agrandir l'image
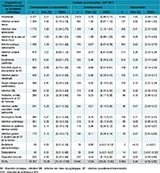
Agrandir l'imageSelon les caractéristiques des patients, les analyses univariées montrent que la PPT était plus élevée chez les hommes (17,21% [16,07-18,41]) que chez les femmes (13,23% [12,42-14,08]) (RPPT=1,30 [1,24-1,37]). Par âge, elle était la plus élevée chez les enfants de 1 à 14 ans et chez les patients âgés entre 65 et 85 ans et la plus basse chez les nourrissons de moins d’1 an ; les PPT par contexte de prescription étaient différentes selon l’âge (tableau 2). La PPT était plus élevée chez les patients atteints d’une affection engageant le pronostic vital à 1 ou 5 ans (RPPT=1,91 [1,76-2,08]), ainsi que chez les patients immunodéprimés (RPPT=2,38 [2,19-2,58]). Par rapport à 2012, la diminution globale des patients traités par ATB s’observait à la fois chez les hommes (-8%) et chez les femmes (-11%). Par classe d’âge, on constatait également, en 2017 par rapport à 2012, une diminution de la PPT chez les enfants jusqu’à 14 ans (-24%) et chez les plus âgés (-8% entre 65 et 84 ans et -13% au-delà de 85 ans). Enfin, pour les deux indicateurs de l’état de santé du patient (score McCabe et statut immunitaire), on observait une diminution de la PPT chez les patients de la classe de référence, c’est-à-dire les patients présentant une maladie non fatale (-13%) et non immunodéprimés (-11%).
 Agrandir l'image
Agrandir l'imageLes prévalences des ATB les plus fréquents et par famille, quelle que soit l’indication et pour les traitements curatifs des infections communautaires et nosocomiales, sont présentées dans le tableau 3. Tous contextes de prescriptions confondus, les 5 molécules ou associations de molécules les plus prescrites le jour de l’enquête en 2017 étaient l’association amoxicilline-acide clavulanique, la ceftriaxone, l’amoxicilline, le métronidazole et l’ofloxacine ; elles représentaient près de la moitié des molécules prescrites en ES (48,1% [46,2-50,0]). Ces 5 molécules étaient identiques en 2012, mais la prévalence de l’amoxicilline-acide clavulanique a diminué en 2017 (-12%) ; de même pour la ceftriaxone (-17%) et l’ofloxacine (-30%). Ainsi, l’ofloxacine arrivait en 5e position des ATB les plus prescrits en 2017 alors qu’elle apparaissait en 3e position en 2012. Parmi les molécules dont la prévalence a augmenté entre 2012 et 2017, on peut citer le céfotaxime (+69%), l’association pipéracilline-tazobactam (+42%) et le céfépime (+213%).
 Agrandir l'image
Agrandir l'imageLes ATB étaient principalement prescrits par voie intraveineuse (53,6% [51,5-55,6] de l’ensemble des ATB prescrits) ou par voie orale (42,9% [41,0-44,8]). Les autres voies restaient très peu utilisées : 2,5% [2,1-2,9] par voie sous-cutanée, 0,4% [0,3-0,6] par voie intramusculaire et 0,3% [0,1-0,6] par inhalation.
Les principaux diagnostics d’infections communautaires ou nosocomiales motivant les traitements étaient les pneumonies (23,0% [21,4-24,8]), les infections urinaires basses (11,9% [10,9-12,9]), les infections intra-abdominales (11,0% [9,9-12,3]) ou les infections de la peau et des tissus mous (10,1% [9,1-11,1]). On observe des différences de répartition des diagnostics selon que l’infection était nosocomiale ou communautaire (tableau 4 ; des comparaisons détaillées avec les résultats de 2012 sont présentés dans le rapport de résultats de l’ENP 2017) 7. On note une amélioration de la documentation du motif de traitement dans le dossier médical, plus élevée en 2017 (88,8% [87,4-90,1]) qu’en 2012 (85,8%).
 Agrandir l'image
Agrandir l'imageConcernant les doses d’ATB, la répartition des écarts entre les DDJ et les DPJ est présentée pour 11 ATB parmi les plus fréquents (tableau 5). La DPJ moyenne était le plus souvent supérieure à la DDJ, à l’exception de la ceftriaxone, du cotrimoxazole et de la spiramycine. Les doses prescrites s’écartaient plus fréquemment de la DDJ pour l’amoxicilline seule (91,9% [88,4-94,2] des prescriptions étaient supérieures à la DDJ de plus d’un facteur 2) ou en association à un inhibiteur des bêta-lactamases (figure 3).
 Agrandir l'image
Agrandir l'image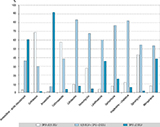 Agrandir l'image
Agrandir l'imageLa durée du traitement ATB, en cours le jour de l’enquête, variait selon le contexte de prescription. Concernant le traitement des infections nosocomiales ou communautaires, les prescriptions d’une durée supérieure à 7 jours représentaient 18,7% [17,5-20,0] des traitements. En SSR, la proportion de prescriptions d’une durée supérieure à 7 jours atteignait 38,5% [34,0-43,1] des traitements curatifs. Même après exclusion des infections fréquemment associées à des durées de traitement supérieures à 7 jours (i.e. infections cardiovasculaires, infections ostéo-articulaires et infections urinaires basses et hautes chez l’homme), les prescriptions d’une durée supérieure à 7 jours représentaient 16,2% [14,9-17,6] des traitements curatifs (données non recueillies en 2012).
Concernant l’ATBP chirurgicale, 30,1% [24,1-36,9] des ATB étaient prescrits en monodose, 17,2% [11,1-25,6] pour 1 journée et 52,7% [45,8-59,5] sur 2 jours et plus. La durée moyenne des ATBP chirurgicales était égale à 2,7 jours [2,0-3,3] et la médiane à 1 jour [1-1]. La moitié des ATBP chirurgicales longues (prescrites sur 2 jours et plus) l’étaient en chirurgie digestive (24,7% [18,6-32,0] de l’ensemble des ATBP chirurgicales) ou orthopédique et traumatologique (26,7% [20,7-33,8]) ; ces types de services étant ceux dans lesquels la plupart des ATBP chirurgicales étaient prescrites (14,4% [11,1-18,4] en chirurgie digestive et 27,8% [22,7-33,5] en chirurgie orthopédique et traumatique). Cependant, la part relative des ATBP chirurgicales prescrites sur 2 jours et plus, parmi l’ensemble des ATBP chirurgicales, était plus élevée en chirurgie digestive (60,8% [48,8-71,6]) qu’en chirurgie orthopédique et traumatique (33,9% [23,1-46,8]). Par rapport à 2012, la part des ATBP chirurgicales prescrites sur 2 jours et plus a baissé en 2017 sans toutefois être significativement différente (57,1% en 2012). Par type de chirurgie, la part des ATBP chirurgicales prescrites sur 2 jours et plus a baissé significativement uniquement en chirurgie orthopédique et traumatique (-28%) passant de 47,1% en 2012 à 33,9% [23,1-46,8] en 2017.
Sur l’ensemble des ATB prescrits le jour de l’enquête, une majorité (80,7% [79,5-81,8]) correspondait à la première molécule prescrite pour l’indication mentionnée, et 1 traitement sur 5 (19,3% [18,2-20,5]) a fait l’objet d’au moins un changement pour le même motif de prescription (données non recueillies en 2012). Pour 6,8% [6,1-7,5] de l’ensemble des traitements, l’ATB a été modifié avec escalade thérapeutique, c’est-à-dire un élargissement du spectre caractérisé par au moins une molécule d’ATB différente. Une désescalade thérapeutique est rapportée pour 5,9% [5,3-6,5] des traitements. La voie d’administration a été modifiée pour 3,4% [2,9-3,9] des ATB prescrits. Pour 0,7% [0,5-0,9] des traitements, l’ATB a été modifié en raison d’effets secondaires indésirables. Enfin, la raison du changement d’ATB est inconnue pour 2,6% [2,2-3,1] des ATB prescrits. Une désescalade était plus fréquente pour le traitement curatif des infections nosocomiales (34,3% [30,9-37,8]) que pour ceux des infections communautaires (29,0% [26,0-32,2]). À l’inverse, un changement de voie était une raison du changement d’ATB plus souvent rapportée dans le traitement des infections communautaires (20,2% [17,3-23,4]) que pour le traitement des infections nosocomiales (11,2% [8,8-14,1]).
Sur l’ensemble des ES, 86,5% [83,4-89,0] déclaraient avoir mis en place, au 31 décembre 2016, une procédure de réévaluation des prescriptions ATB dans les 72 heures, dans tous leurs services : 96,3% [91,8-98,4] en MCO et 54,6% [32,3-75,2] en CHR/CHU. Pour ces derniers, la procédure était mise en œuvre dans certains services pour 42,4% [22,1-65,6] et dans aucun service pour 3,0% [0,7-11,6] d’entre eux.
Discussion
En France en 2017, 1 patient hospitalisé sur 7 recevait un traitement ATB en ES. Le secteur le plus utilisateur d’ATB était la réanimation avec 1 patient sur 2 traité par ATB. Par rapport à 2012, on constatait une diminution globale de la PPT en ES, alors qu’elle était stable entre 2006 et 2012. Cette diminution de la PPT est cohérente avec la diminution de la consommation globale d’ATB (en DDJ/1 000 JH) observée par le réseau ATB-Raisin sur la même période (-3,2%) 8. En outre, cette diminution de PPT est conforme à la tendance observée avec le suivi des consommations par l’ANSM (Agence nationale de sécurité du médicament et des produits de santé) 9,10. Ces résultats sont encourageants d’autant que les durées de séjour ont légèrement diminué sur cette période (la durée moyenne de séjour (DMS) est passée de 5,7 jours en 2012 à 5,5 jours en 2017) 11.
Cette tendance à la diminution des traitements ATB concerne les patients les plus jeunes et les plus âgés, ainsi que les moins fragiles (patients non immunodéprimés et ceux atteints d’une maladie non fatale), ce qui suggère un usage mieux maîtrisé des ATB chez ces groupes de patients.
Près d’1 traitement curatif d’infection communautaire ou nosocomiale sur 5 est prescrit sur une durée supérieure à 7 jours. Ce constat est identique après l’exclusion des infections qui relèvent d’un traitement fréquemment supérieur à 7 jours. Cette proportion pose question, compte tenu des recommandations actuelles sur les durées de traitements qui visent à réduire au maximum les indications d’ATB de plus de 7 jours. L’objectif attendu du Programme national d’actions de prévention des infections associées aux soins (Propias) fixe à moins de 10% la proportion de traitements curatifs de plus de 7 jours non justifiés 12. Cet objectif n’est semble-t-il pas atteint. En outre, la durée de traitement a été calculée à partir de la date de début du traitement au jour de l’enquête, la date de fin du traitement n’étant pas connue. Cette durée de traitement jusqu’au jour de l’enquête est donc censurée et sous-estimée.
Concernant l’ATBP chirurgicale, on constate que la prévalence des patients traités a diminué entre 2012 et 2017 sans qu’il soit possible de vérifier si cette diminution correspond à une meilleure adéquation avec les recommandations de la Société française d’anesthésie et de réanimation (SFAR) 13. En revanche, concernant la durée de leur prescription, on constate qu’un traitement sur deux a été prescrit sur deux jours ou plus. Ces durées de prescriptions ne sont pas conformes aux recommandations de la SFAR qui prônent une prescription limitée le plus souvent à la période opératoire, parfois à 24 heures, exceptionnellement à 48 heures et jamais au-delà 13. Ce constat a déjà été fait sur la base des données du réseau ISO-Raisin 14. Il faut toutefois souligner qu’une partie des prescriptions prolongées peut correspondre à des traitements curatifs, poursuivis en post-opératoire d’une infection découverte en peropératoire, ou dans les chirurgies d’urgence à haut risque infectieux. Ce biais de classement potentiel doit être considéré alors même que les enquêteurs se fondaient souvent sur le dossier patient pour renseigner le motif de prescription. La littérature rapporte que les ATBP chirurgicales les plus courtes sont moins enregistrées que les plus longues dans le dossier patient, conduisant à un biais de sélection 15. En outre, les durées de traitements sont censurées par le jour de l’enquête, du fait du design transversal de l’enquête. Ainsi, les résultats portant sur la durée d’ATBP chirurgicales doivent être interprétés avec prudence compte tenu de ces biais. Il n’en reste pas moins que l’observation d’ATBP chirurgicales supérieures à deux jours contrevient aux recommandations, mais la proportion exacte par rapport à l’ensemble des traitements d’ATBP chirurgicales reste à mieux évaluer via des enquêtes dédiées.
L’évolution de la prévalence des traitements par molécule entre 2012 et 2017, à la baisse pour l’amoxicilline-acide clavulanique, la ceftriaxone, la ciprofloxacine et l’ofloxacine et à la hausse pour la pipéracillinetazobactam, le céfotaxime et le céfépime, est en cohérence avec l’évolution de la consommation des ATB observée par le réseau ATB-Raisin 8. L’augmentation de la prévalence du céfotaxime, conjointement à la diminution de la prévalence de la ceftriaxone, indique l’application des recommandations sur le report des prescriptions de la ceftriaxone vers le céfotaxime 16. L’augmentation importante de la prévalence de céfépime s’explique dans un contexte de tensions d’approvisionnement en pipéracilline-tazobactam.
Concernant la dose d’ATB prescrite, il faut tout d’abord souligner la qualité du recueil réalisé par les enquêteurs et, en amont, par les prescripteurs, avec moins de 1% de données manquantes sur l’ensemble des ATB prescrits. L’écart entre les DPJ et la DDJ était retrouvé pour l’amoxicilline et pour l’association amoxicilline et acide clavulanique orale, conformément à la littérature 9,17. En 2017, la DDJ de l’amoxicilline égale à 1 g (et modifiée à 1,5 g à compter de 2019) était très faible par rapport aux recommandations françaises sur les posologies de prescriptions pour cette molécule qui sont de 2 à 3 g/j chez l’adulte 10,18,19,20,21. Si l’on observait le plus souvent une DPJ plus élevée que la DDJ, on constatait aussi que certaines molécules avaient au contraire une DPJ plus basse que la DDJ. La ceftriaxone et le cotrimoxazole étaient prescrits à une dose moyenne très inférieure à leur DDJ. L’explication probable tient dans les posologies recommandées en France (1 à 2 g/j pour une DDJ de 2 g).
Les écarts pour les autres molécules peuvent se justifier en pratique par différents facteurs individuels : poids important de certains patients, augmentation de la concentration minimale inhibitrice (CMI) des agents pathogènes visés conduisant à une augmentation des posologies, augmentation des posologies chez les patients atteints de maladies graves ou instables en raison d’une augmentation de leur volume de distribution et/ou de clairance rénale, ce qui se rencontre fréquemment chez les patients en réanimation.
Une partie des données de l’ENP 2017 a été envoyée à l’ECDC pour la participation à la deuxième enquête de prévalence européenne 1. En 2017, la France présentait la prévalence des patients traités par ATB en ES de court séjour la plus faible d’Europe, après la Hongrie. Ces résultats sont cohérents avec ceux de la première enquête européenne réalisée en 2012 22. Les données complémentaires recueillies en 2017 concernant la dose d’ATB confirment la position de la France au 2e rang des pays les moins consommateurs d’ATB à l’hôpital, évaluée à partir du nombre de DDJ d’ATB à usage systémique recensées un jour donné, égale à 26,6 DDJ/100 patients 23.
Les résultats de la consommation d’ATB systémique en France en 2017 dans les ES (2,13 DDJ/1 000 hab/j) mesurée par la surveillance européenne de la consommation d’ATB (ESAC-Net) plaçaient la France au 7e rang des pays européens les plus consommateurs d’ATB après Malte, la Grande-Bretagne, la Lituanie, la Finlande, la Lettonie et l’Italie 24. Cela confirme que les résultats en incidence et en prévalence sur une journée sont difficilement comparables. Ce décalage peut en partie s’expliquer par le fait que l’enquête de prévalence en France est réalisée sur la période allant de mai à juin, période lors de laquelle les infections saisonnières sont plus rares. À l’inverse, l’incidence annuelle intègre les périodes d’épidémies saisonnières. En outre, les services inclus ne sont pas les mêmes : dans l’enquête européenne de prévalence seuls les services de court séjour sont inclus, alors que ESAC-Net porte sur les ES quel que soit le service. Ce décalage peut également s’expliquer, en partie, par la différence entre les DPJ et les DDJ, particulièrement marquée pour les amino-pénicillines, largement prescrites.
Conclusion
La diminution de la prévalence des traitements ATB entre 2012 et 2017 encourage à poursuivre à l’hôpital les actions en faveur du bon usage des ATB, qui représentent un des leviers pour la prévention de l’antibiorésistance.
Les écarts notables aux recommandations des durées de traitements curatifs et, plus encore, des antibioprophylaxies chirurgicales, révèlent une marge de progression dans la prescription d’ATB qui justifient des actions de sensibilisation ciblées auxquelles les missions nationales de surveillance et de prévention de l’antibiorésistance en établissement de santé (SPARES) et du risque infectieux en chirurgie et médecine interventionnelle (SPICMI) pourront contribuer.
Remerciements
Les auteurs remercient l’ensemble des professionnels et équipes d’enquêteurs des établissements de santé qui ont participé à cette enquête. Sincères remerciements également à François L’Hériteau, coordinateur de l’équipe Antibiorésitance au CPias Île-de-France et Emmanuel Piednoir, responsable du CPias Bretagne, pour leur relecture de cet article.
Liens d’intérêts
Les auteurs déclarent ne pas avoir de liens d’intérêt au regard du contenu de l’article. Cette étude n’a reçu aucun financement spécifique.
Références
prevalence.html
whocc.no/atc_ddd_index_and_guidelines/guidelines/
ecdc.europa.eu/en/healthcare-associated-infections-acute-care-hospitals/surveillance-disease-data/database




