Épidémiologie de la rougeole en France entre 2011 et 2018
// Measles epidemiology in France between 2011 and 2018
Résumé
Dans les suites de l’épidémie majeure de rougeole survenue en France entre 2008 et 2011, sont présentés ici les résultats de la surveillance basée sur la déclaration obligatoire de la maladie entre le 1er octobre 2011 et le 30 septembre 2018, en prenant en compte la dynamique épidémiologique de la rougeole par vagues successives, du mois d’octobre d’une année au mois de septembre de l’année suivante.
Entre octobre 2011 et septembre 2018, 5 311 cas ont été déclarés et retenus dans l’analyse. L’incidence des cas déclarés la plus élevée a concerné les enfants de moins de 1 an, atteignant, lors de la dernière vague 2017-2018, un taux de 30,7 cas pour 100 000 enfants. L’âge médian était de 15 ans. Parmi l’ensemble des cas, 1 279 (24%) ont été hospitalisés, dont 244 pour une pneumonie et 13 pour une encéphalite. Quatre cas sont décédés, âgés de 16 à 32 ans. Si le génotype D4 avait majoritairement circulé en 2011, depuis 2014 sont identifiés en France de façon quasi exclusive les génotypes D8 et B3, comme ce qui est observé dans le reste de l’Europe.
Une analyse complémentaire des données de mortalité issues du Centre d’épidémiologie sur les causes médicales de décès de l’Institut national de la santé et de la recherche médicale (CépiDc-Inserm), sur la période allant d’octobre 2008 à septembre 2018, a permis d’identifier 23 décès liés à un épisode aigu de l’infection. Six décès dus à une panencéphalite sclérosante subaiguë liée à une infection aiguë antérieure à 2008 ont été identifiés.
Ces données montrent que, fin 2018, il restait en France un réservoir de sujets réceptifs suffisant pour maintenir la transmission du virus, en particulier dans la population des jeunes adultes. Le rattrapage concernant surtout la seconde dose des enfants et des adolescents s’est amélioré au cours des années récentes, mais les couvertures vaccinales, y compris celle des nourrissons, restent néanmoins en deçà du seuil de 95% qui permettrait l’élimination de la maladie. À moyen terme, la décision du ministère de la Santé de rendre la vaccination des nourrissons obligatoire à compter de 2018 devrait aider à atteindre cet objectif.
Abstract
Following the major measles epidemic that occurred in France in 2008-2011, this paper describes surveillance results based on mandatory notification of measles between 1 October 2011 and 30 September 2018, taking into account the epidemiological dynamics of the disease through 7 consecutive 12 month periods (from October to September of the subsequent year).
From October 2011 to September 2018, 5,311 cases were reported and included in this analysis. The highest incidence of reported cases was observed in children below one year of age, with 30.7 cases per 100,000 infants reported during the last epidemic wave in 2017-2018. The median age was 15 years. Among all cases, 1,279 (24%) were hospitalized, including 244 for pneumonia and 13 for encephalitis. Four people died, aged 16 to 32 years. Although genotype D4 was the main one circulating in 2011, since 2014, genotypes D8 and B3 are the most commonly identified genotypes in France, as well as in the rest of Europe.
We made a complementary analysis on mortality data from Epidemiological Center on the Medical Causes of death of the French National Institute of Health and Medical Research (CépiDc-Inserm) over the course of the period from October 2008 to September 2018. This allowed us to identify 23 deaths related to acute measles infection, as well as 6 deaths of subacute sclerosing panencephalitis linked to measles infections prior to 2008.
Our data show that in France, at the end of 2018, there still remained a large enough reservoir of susceptible individuals to allow the measles virus transmission, especially among young adults. Catching up with a second dose of vaccine has improved in children and teenagers over the recent years, but vaccine coverage, including for toddlers, still remains below the 95% threshold that would allow eliminating the disease. In the medium term, the Ministry of Health’s decision to make infant immunization mandatory from 2018 should help achieve this goal.
Introduction
La rougeole est une maladie infectieuse parmi les plus contagieuses, et l’une des plus grandes causes de morbidité et mortalité dans le monde. Toutefois, en raison d’un réservoir unique (l’homme) et de l’existence d’un vaccin efficace, son élimination, voire son éradication, serait possible. L’interruption de la circulation endémique de la rougeole est l’un des objectifs de l’Organisation mondiale de la santé (OMS) pour la région européenne.
Pour atteindre ce but, un plan national d’élimination de la rougeole a été lancé en France en 2005, fixant notamment des objectifs d’une couverture vaccinale (CV) de 95% à l’âge de 2 ans et d’une incidence annuelle inférieure à 0,1 cas/100 000 habitants 1. Afin de mettre en œuvre des mesures de contrôle, notamment vaccinales, visant à stopper la diffusion du virus autour d’un cas et en situation de cas groupés, et de suivre les progrès vers l’élimination, la rougeole est redevenue à déclaration obligatoire (DO) en juillet 2005. Un appui au diagnostic a été mis en place avec le Centre national de référence (CNR) de la rougeole, des oreillons et de la rubéole et son laboratoire associé pour la confirmation biologique et la caractérisation des virus, notamment à partir de prélèvements salivaires 2.
Cependant, entre octobre 2008 et septembre 2011, la France a connu un épisode épidémique de grande importance avec plus de 22 000 cas déclarés. Cet épisode a été décrit dans un article précédent 3. La persistance de la circulation du virus de la rougeole dans la population était attendue, en raison de la CV insuffisante et des résultats d’une enquête de séroprévalence menée en 2013 dans la population des jeunes adultes donneurs de sang, qui montrait que 9% d’entre eux étaient toujours réceptifs vis-à-vis de la rougeole en période post épidémique 4.
L’objectif de cet article est de décrire la situation épidémiologique de la rougeole en France depuis la fin de cet épisode.
Méthodes
Nous présentons ici les données de DO recueillies entre octobre 2011 et septembre 2018. Tout cas répondant à un ou plusieurs des critères cliniques ou biologiques de la DO (1) doit être signalé sans délai à l’Agence régionale de santé (ARS), qui investigue, en lien avec la Cellule d’intervention en région (Cire) de Santé publique France si nécessaire, les cas et situations de cas groupés détectés.
Les fiches de déclaration, complétées et validées par la personne en charge de la veille sanitaire à l’ARS, sont ensuite centralisées et analysées par Santé publique France. Les déclarations invalidées au vu de résultats biologiques négatifs et celles correspondant à une rougeole post-vaccinale (2) sont exclues de l’analyse. Seuls les cas survenus chez des sujets résidant en France sont inclus dans l’analyse.
Les cas ont été classés en :
–Cas clinique : cas présentant les critères cliniques de rougeole pour lequel il n’y a pas eu d’analyse biologique, et sans lien épidémiologique avec un cas confirmé. Une déclaration pour laquelle le résultat d’un prélèvement réalisé en dehors des délais (3) s’avère négatif est classée en cas clinique.
–Cas confirmé :
–biologiquement : cas ayant présenté des signes cliniques évocateurs de rougeole et pour lequel un ou plusieurs critères de confirmation biologique étaient présents ;
–épidémiologiquement : cas clinique ayant été en contact avec un cas confirmé dans les 7 à 18 jours avant le début de l’éruption ;
Ont été considérés comme cas importés des cas confirmés avec notion de séjour à l’étranger dans les 7 à 18 jours précédant l’éruption sans que la maladie puisse être rattachée à une transmission locale sur le territoire français.
L’information sur le statut vaccinal a été analysée, lorsqu’elle était disponible, en distinguant les données déclaratives des données issues d’un document (carnet de vaccination, dossier médical...). L’analyse du statut vaccinal n’est réalisée que sur la population des personnes ciblées par le calendrier vaccinal : âgées de plus de 1 an et nées depuis 1980.
Concernant la mortalité, les données obtenues par la DO ont été revues et complétées avec celles issues de la base des certificats de décès du CépiDc-Inserm (Centre d’épidémiologie sur les causes médicales de décès de l’Institut national de la santé et de la recherche médicale), sur la période d’étude ainsi que sur la période épidémique précédente 2008-2011.
Les signalements de rougeole reçus à Santé publique France dans le cadre du dispositif de signalement des infections nosocomiales ont également été analysés.
Pour décrire les cas groupés (4) de rougeole, une application spécifique (« Voozarouge ») est à disposition des Cire. Les données collectées par ce dispositif pour les seuls cas groupés investigués par les ARS et/ou les Cire et saisis dans l’application ont été également analysées.
Les chiffres de population utilisés sont issus des estimations localisées de population (source : Institut national de la statistique et de études économiques-Insee). Les proportions ont été comparées en utilisant le test du Chi2.
Résultats
Nombre de cas signalés et classification des cas
Entre octobre 2011 et septembre 2018, 6 016 signalements de cas suspects de rougeole ont été transmis à Santé publique France. Pour 566 cas, la suspicion de rougeole n’a pas été confirmée par les résultats biologiques et 78 autres cas se sont révélés être des réactions post-vaccinales. Ces cas ont été exclus de l’analyse. De même, 61 cas survenus chez des personnes résidant hors de France ont été exclus de l’analyse.
Les 5 311 cas retenus dans l’analyse, se répartissaient en :
–2 643 cas confirmés biologiquement (50%) ;
–926 cas confirmés épidémiologiquement (17%) ;
–1 742 cas cliniques (33%).
Parmi les cas, 213 étaient importés, une majorité d’entre eux lors d’un voyage dans un autre pays d’Europe de l’Ouest (66 cas, essentiellement Espagne, Grande-Bretagne et Italie), d’un pays d’Asie (50 cas), d’Afrique (46 cas dont 30 du Maghreb) ou d’Europe de l’Est (28 cas dont 16 de Roumanie). Pour 23 cas importés, l’origine géographique n’était pas précisée.
Le nombre de cas déclarés par périodes successives de 12 mois (octobre à septembre) et le taux de déclaration pour 100 000 habitants qui en découle, se distribuaient ainsi : 1 062 cas en 2011-2012 (taux : 1,64), 286 en 2012-2013 (taux : 0,44), 275 en 2013-14 (taux : 0,43), 353 en 2014-2015 (taux : 0,55), 91 en 2015-2016 (taux : 0,14), 437 en 2016-2017 (taux : 0,68) et 2 807 en 2017-2018 (taux : 4,35).
La distribution mensuelle de ces cas sur la période est montrée sur la figure 1.
 Agrandir l'image
Agrandir l'imageRépartition géographique des cas
La distribution géographique des cas est représentée sur la figure 2 pour chacune des sept périodes de surveillance de 12 mois. Sur l’ensemble de la période d’analyse, seuls deux départements métropolitains n’ont déclaré aucun cas (Allier et Haute-Marne). Dans l’Océan Indien, La Réunion a déclaré 10 cas. Dans les départements français d’Amérique, aucun cas autochtone n’a été déclaré et si 2 cas ont été importés depuis la métropole, respectivement en Guadeloupe et en Guyane, aucun d’eux n’a été localement à l’origine d’une chaîne de transmission.
La circulation du virus a été la plus active dans la moitié de la France située au sud d’une diagonale nord-ouest/sud-est au cours de la période 2017-2018 (figure 2g).
 Agrandir l'image
Agrandir l'imageDescription des cas selon le sexe et l’âge
Le sex-ratio H/F des cas déclarés était de 1,1 (2 789/2 522), l’âge moyen de 16 ans quelle que soit la période de surveillance, avec un âge médian de 15 ans (extrêmes 1 jour à 92 ans) variant entre 9 et 17 ans selon les périodes. Sur l’ensemble des cas dont l’âge était connu (n=5 309), 510 (9,6%) ont été déclarés chez des enfants de moins de 1 an, dont 102 (1,9%) âgés de moins de 6 mois. Neuf cas de rougeole néo-natale ont été diagnostiqués.
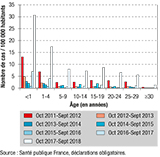
Comme le montre la figure 3, quelle que soit la période, les taux d’incidence déclarés pour 100 000 habitants les plus élevés étaient retrouvés chez les enfants âgés de moins de 5 ans, et plus particulièrement chez ceux âgés de moins de 1 an. Lors de la dernière vague de 2017-2018, le taux était de 30,7 cas déclarés pour 100 000 enfants de moins de 1 an et de 17,4 chez les enfants âgés de 1 à 4 ans. Dans les autres groupes d’âge, il était de 8,7 chez les sujets âgés de 15 à 19 ans, 8,1 chez les enfants âgés de 5 à 9 ans et 7,3 pour les 10-14 ans, de 6 pour 100 000 sujets âgés de 20 à 30 ans et de 1,3 au-delà de 30 ans.
 Agrandir l'image
Agrandir l'imageFormes cliniques
Parmi les cas déclarés, 1 279 cas étaient hospitalisés (24%). La proportion de cas déclarés avec la notion d’une hospitalisation était de 17% chez les moins de 20 ans (588/3 420) et de 37% chez les patients âgés de 20 ans et plus (691/1 889) (p<10-3).
Parmi les 1 279 cas hospitalisés, des complications étaient rapportées pour 360 cas (28%), mais seules 283 (22%) étaient détaillées, parmi lesquelles principalement des pneumopathies (244, soit 19% des cas hospitalisés) 13 encéphalites (1%), et 7 atteintes hépatiques (0,5%) (tableau). Une admission en réanimation a été nécessaire pour 41 formes compliquées (11,4%). Quatre personnes sont décédées : 3 dans un tableau de pneumopathie sévère et la quatrième dans un tableau d’encéphalite subaiguë à inclusions, 2 mois après la contamination rougeoleuse. Cette dernière ainsi qu’un des cas décédés de pneumopathie étaient sous traitement immunosuppresseur en raison d’antécédents de greffe d’organe.
 Agrandir l'image
Agrandir l'imageParmi les 4 032 cas non hospitalisés, des complications ont été rapportées pour 93 cas (2,3%), parmi lesquelles on retrouve 67 complications pulmonaires (pneumonies et bronchites), 18 complications ORL (16 otites moyennes et 2 angines), 5 hépatites, un purpura et 2 altérations de l’état général sans plus de précisions.
Statut vaccinal des cas
Le statut vaccinal a été analysé sur la population des cas éligibles à la vaccination, c’est-à-dire âgés de plus de 1 an au moment de l’infection, et nés depuis 1980, soit 4 351 cas (82%). Le statut vaccinal de ces cas était renseigné par les déclarants pour 3 793 d’entre eux, soit 87,2% des 4 351 cas notifiés. Parmi ces patients, 1 531 (40,4%) avaient cette information validée par un document (carnet de santé, dossier médical) parmi lesquels 1 327 (86,7%) n’étaient pas correctement vaccinés (<2 doses). Lorsque le statut vaccinal n’était renseigné que par l’interrogatoire, 89,6% (2 027/2 262) n’étaient pas correctement vaccinés. La différence entre ces deux proportions étant significative (p=0,005), l’analyse sur le statut vaccinal a uniquement porté sur les vaccinations validées sur document.
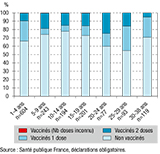
Parmi les 1 531 cas avec un statut vaccinal validé, la proportion de sujets n’ayant reçu aucune dose de vaccin contre la rougeole était de 69,1% (n=1 058), celle des sujets ayant reçu seulement une dose était de 17,6% (n=269), 12,9% avaient reçu 2 doses de vaccin (n=197) et 0,5% un nombre de doses inconnu (n=7).
La proportion de cas vaccinés avec 2 doses était différente selon le groupe d’âge, allant de 5% chez les sujets âgés de 30 à 38 ans à 24,7% chez les 20-24 ans (p<0,001) (figure 4).
 Agrandir l'image
Agrandir l'imageCas nosocomiaux
Depuis le dernier trimestre de 2011, 65 signalements de rougeole nosocomiale sont parvenus à Santé publique France. Les services d’urgence, de médecine et de pédiatrie totalisaient 74% de ces épisodes. Ces signalements recensaient 137 cas, dont un décès directement imputable à la rougeole. Parmi ces signalements, 23 correspondaient à des cas groupés avec une médiane de 3 cas par épisode (16 au maximum). Des cas parmi le personnel soignant ont été recensés dans 83% de ces épisodes de cas groupés (19/23).
Cas groupés
En collectivité, hors milieu de soins, 55 épisodes de cas groupés ont été documentés au cours de l’ensemble de la période d’étude : 20 en Provence-Alpes-Côte d’Azur, 18 en Nouvelle-Aquitaine, 6 en Auvergne-Rhône-Alpes, 4 en Île-de-France, 2 en Grand Est et Bretagne, et 1 en Occitanie, Bourgogne-Franche-Comté et Hauts-de-France.
Parmi eux, 11 ont concerné des crèches (2 à 7 cas par crèche), 18 des établissements scolaires, dont 7 lycées (2 à 100 cas par établissement), 7 des universités/écoles supérieures (5 à 45 cas), 11 des camps de gens du voyage (3 à 9 cas), les 6 autres cas groupés concernaient : trois squats, une maison communautaire, une ferme pédagogique et un rassemblement sportif (3 à 5 cas).
Au total 508 cas ont été identifiés et investigués dans ces collectivités et, parmi ces cas, 465 (91%) ont fait l’objet d’une DO à la suite de l’investigation.
Génotypage
Au cours de la période du 1er octobre 2011 au 30 septembre 2018, l’identification du génotype a été réalisée au Centre national de référence pour 1 096 échantillons positifs pour le virus de la rougeole. Les génotypes identifiés étaient principalement D8 (663 cas), D4 (200 cas) et B3 (176 cas). D’autres génotypes ont été plus rarement rapportés : D9 (n=6), H1 (n=1) et B2 (n=1).
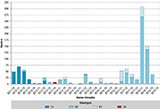
La distribution par trimestres des 4 principaux génotypes (D8, D4, B3 et D9) identifiés sur la période de surveillance est présentée sur la figure 5.
D’autre part, le génotype A (souche vaccinale) a été identifié à 12 reprises chez des patients ayant reçu 1 dose de vaccin dans les 2 semaines qui précèdent l’éruption. L’identification du génotype A a permis de différencier les réactions post-vaccinales bénignes des infections rougeoleuses à virus sauvage.
 Agrandir l'image
Agrandir l'imageLe génotype D4 avait majoritairement circulé en 2011 et était toujours présent en 2012 (souche de référence MVs/Marmande.FRA/43.11/2). En 2013, le nombre de cas de rougeole a diminué. Les génotypes identifiés alors étaient variés : génotypes D4, D8, B3 et plus rarement D9. Depuis 2014 jusqu’à fin 2018, ont été identifiés en France de façon quasi exclusive les génotypes D8 (souches MVi/Manchester.GBR/30.94/ et MVs/Frankfurt Main.DEU/17.11/) et B3 (souche MVs/Saint Denis.FRA/36.17.
Analyse de la mortalité incluant les données collectées auprès du CépiDc-Inserm (certificats de décès)
De 2008 à 2016 (5), la base du CépiDc-Inserm comportait 15 enregistrements codés pour la rougeole en cause principale de décès. Pour la même période, 10 cas de rougeole ayant fait l’objet d’une DO à Santé publique France sont décédés. Seuls 6 décès ont été recensés par les deux systèmes, tous en 2010 et 2011. Ainsi, 19 décès ont été pris en compte, auxquels s’ajoutent les 4 décès identifiés par la DO en 2017 et 2018.
La prise en compte des données du CépiDc-Inserm et des décès enregistrés sur la DO nous a donc permis de comptabiliser un total de 23 décès de rougeole sur la période d’octobre 2008 à septembre 2018.
Les circonstances du décès sont une atteinte respiratoire (pneumopathie, syndrome de détresse respiratoire aigüe) pour 12 cas, une encéphalite pour 10 cas (dont deux cas d’encéphalite à inclusion) et une myocardite ayant entraîné une défaillance cardiorespiratoire.
Pour 10 de ces personnes décédées, un terrain d’immunodépression a pu être retrouvé : 4 d’entre elles présentaient un déficit immunitaire (patient VIH+, leucémie lymphoblastique aiguë, immunodépression congénitale et immunodépression acquise) et 6 suivaient un traitement immunosuppresseur (3 en suite de greffe d’organe, 1 pour maladie de Hodgkin, 1 pour périartérite noueuse et 1 pour maladie de Crohn). Pour les 13 autres décès : 2 patients avaient des antécédents pulmonaires (bronchite chronique, bronchectasie), 4 patients ne souffraient d’aucun antécédent particulier et, pour les 7 autres, il n’a pas été possible de documenter l’existence d’antécédents.
Au-delà de ces décès survenus en lien avec l’infection aiguë, l’analyse menée sur les certificats de décès a permis d’identifier 6 décès ayant en cause principale une panencéphalite sclérosante subaiguë (PESS) : 2 décès survenus en 2008, 1 en 2009 puis 1 en 2014 et 2 en 2015, chez des sujet âgés de 19 à 64 ans.
Discussion
Les données issues des fiches de déclaration obligatoire collectées entre octobre 2011 et septembre 2018 montrent que la circulation du virus de la rougeole se poursuit en France consécutivement à la flambée épidémique de 2008-2011, avec plus de 5 300 cas déclarés sur cette période. On observe une diminution progressive de cette circulation de 2012 à 2015 jusqu’à une période de « lune de miel » en 2015-2016, précédant la survenue d’un nouvel épisode épidémique à l’automne 2017. Cette dernière vague épidémique a débuté dans la région de Nouvelle-Aquitaine où ont été déclarés 50% des 2 807 cas survenus entre octobre 2017 et septembre 2018, gagnant rapidement la quasi-totalité du territoire 5.
L’incidence des cas déclarés la plus élevée est retrouvée chez les nourrissons âgés de moins de 1 an, trop jeunes pour être vaccinés. Comme précédemment observé en 2008-2011, nos données confirment à la fois le déplacement de l’âge des cas vers des tranches d’âge plus élevées, avec 50% des cas âgés d’au moins 15 ans et, parmi eux, un risque de complications plus élevé. Sur la totalité des cas déclarés, près de 1 300 ont été hospitalisés, soit plus d’un quart, mais cette proportion atteignait 38% chez les sujets âgés de plus de 20 ans. Parmi les complications décrites, ont été signalés 244 cas de pneumopathie et 13 cas d’encéphalite. Quatre décès sont survenus, chez des sujets âgés de 16 à 32 ans ; 2 d’entre eux étaient sous traitement immunosuppresseur en raison d’antécédents de greffe d’organe. Les hospitalisations et passages aux urgences exposaient au risque de transmission nosocomiale et plusieurs foyers ont été recensés, comme décrit précédemment 6. Ceci doit conduire au renforcement des mesures barrière et du rattrapage des vaccinations parmi les professionnels de santé selon les recommandations vaccinales actuelles 7.
Les cas de rougeole restent sous-déclarés en France. Lors d’une étude, menée en 2013 en collaboration avec l’Établissement français du sang chez des donneurs de sang âgés de 18 à 32 ans, l’exhaustivité de la DO dans l’inter-région Sud-Est avait été estimée à 55% 4. L’application de ce taux à l’ensemble des tranches d’âge et des régions conduit à estimer à plus de 10 000 cas le nombre de cas réellement survenus sur la période d’étude. D’autre part, la comparaison des décès répertoriés via la DO avec les données du CépiDc-Inserm montre que la sous-notification des décès via la DO est très proche de celle des cas (10/19 soit 53%). Ce constat nous incite à considérer que ce taux de sous-déclaration des cas peut probablement aussi s’appliquer aux cas avec complications. Cela bien que nous ayons observé des proportions élevées d’hospitalisations au regard de la fréquence connue des complications graves décrites dans d’autres études 8,9, ce qui aurait pu être en faveur d’un meilleur taux de déclaration pour les cas hospitalisés.
L’absence de registres de vaccination en France et, hormis chez les plus jeunes, de carnets de vaccination individuels, explique la proportion de seulement 40% de cas éligibles à la vaccination chez qui le statut vaccinal a pu être validé sur document. Parmi eux, 86,7% n’étaient pas correctement vaccinés (69,1% n’avaient reçu aucune dose contre la rougeole et 17,6% une seule dose), et 12,9% avaient reçu deux doses de vaccin. Parmi les cas, la proportion de sujets ayant reçu deux doses de vaccin est donc en augmentation (4,7% lors de l’épisode épidémique 2008-2011). Cette augmentation, qui peut paraître paradoxale, peut vraisemblablement trouver en partie une explication avec l’amélioration de la CV avec deux doses de vaccin au cours des années récentes : non seulement pour les nourrissons de 24 mois, passant de 60,9% en 2010 à 80,1% en 2016, mais surtout en termes de rattrapage dans les tranches d’âge plus élevées : à 6 ans passant de 44,3% en 2006 à 83,2% en 2013, et à 11 ans, de 85% en 2008 à 93,2% en 2015 10.
En effet, à efficacité vaccinale constante du vaccin rougeole (estimée à 97% avec deux doses 11), plus la CV est élevée, plus la proportion de vaccinés parmi les cas augmente, en lien avec l’augmentation de la proportion relative des échecs vaccinaux parmi les cas au fur et à mesure de la diminution du nombre des non-vaccinés. De ce fait, en cas d’importation du virus de la rougeole dans une population complètement vaccinée, seuls les sujets qui n’ont pas développé d’anticorps protecteurs à la suite de la vaccination vont développer la maladie, et ainsi 100% de ces quelques cas résiduels de rougeole seront observés chez des personnes vaccinées avec deux doses 12. Certains pays expérimentent déjà ce paradoxe, tel le Portugal bénéficiant d’une CV rougeole à deux doses comprise entre 95% et 99% selon les régions, où a été décrit en 2018 un foyer épidémique de 211 cas, au sein duquel 70% des cas confirmés avaient reçu deux doses de vaccin 13. La situation française reste toutefois encore loin de ce contexte puisqu’en 2016, aucun département n’atteignait 95% de CV à deux doses (seuls sept départements se situaient entre 85% et 90% de CV à deux doses 14).
En ce qui concerne la mortalité, le travail complémentaire que nous avons effectué sur les données du CépiDc-Inserm a permis d’identifier des décès supplémentaires pour lesquels les cas de rougeole n’avaient pas fait l’objet d’une DO. Sur le total des 23 décès survenus depuis octobre 2008, au moins 10 sont survenus chez des personnes immunodéprimées et qui ne pouvaient donc être protégées que si leur entourage était lui-même immunisé contre la rougeole. Tous ces décès auraient pu être évités si l’immunité de groupe avait été suffisante, en lien avec une CV élevée, pour interrompre la circulation du virus. Cette analyse a de plus permis d’identifier 6 décès liés à une PESS. Tous ces décès concernaient des sujets âgés de 19 à 64 ans. En raison de la latence d’apparition de la PESS à la suite de l’infection (6 à 10 ans) d’une part et du délai entre les premiers signes de PESS et le décès (3 ans en moyenne) d’autre part 15, ces décès concernaient des personnes ayant toutes très vraisemblablement contracté la rougeole antérieurement à 2008.
Plusieurs pays européens ont aussi été touchés par des épidémies de rougeole au cours de ces dernières années, avec l’évolution du nombre de cas signalés détaillée dans les rapports du Centre européen de prévention et de contrôle des maladies (ECDC). Ainsi, entre le 1er octobre 2017 et le 30 septembre 2018, tous les pays (n=30) participant à la surveillance de la rougeole coordonnée par l’ECDC ont déclaré des cas 16. Outre la France, les pays ayant déclaré le plus de cas sont : la Roumanie (5 946 cas et 24 décès (6)), la Grèce (3 049 cas et 4 décès), l’Italie (2 599 et 6 décès) et le Royaume-Uni (1 019 cas, aucun décès).
Au cours de ces sept années de surveillance, ce sont sensiblement les mêmes génotypes que ceux observés en France qui ont circulé en Europe, avec des variations quant au génotype prédominant d’une année sur l’autre et d’un pays à l’autre en fonction du contexte épidémique ou non 17. Ainsi, entre le 1er janvier 2018 et le 30 juin 2018, les séquences envoyées par les CNR de la région OMS Europe et enregistrées dans la base MeaNS, montraient que les génotypes circulant étaient des génotypes B3 (n=952), D8 (n=790) et, de façon plus anecdotique, D9 (n=6) 18. L’identification des génotypes et l’analyse des séquences des virus de la rougeole circulant sont deux outils importants en termes de surveillance, permettant de valider les liens épidémiologiques, de suivre l’évolution virale et d’adapter au besoin les kits de diagnostic clinique. L’utilité qu’il y a à définir un isolement viral comme appartenant à un génotype est toutefois moindre dans les situations où ce génotype particulier montre une diversité génétique et est dépisté en grand nombre dans une vaste région géographique au cours d’une longue période, comme cela a été le cas pour le génotype D4 en Europe en 2007-2011) 19.
Conclusion
Fin 2018, le suivi épidémiologique de la rougeole montre qu’il reste en France un réservoir de sujets réceptifs suffisant pour maintenir la transmission du virus, en particulier dans la population des jeunes adultes. Depuis 2011, les messages de prévention et d’information sur la vaccination ont été renforcés en France vis-à-vis de la population générale et des acteurs de santé avec, plus particulièrement depuis 2017, la création de sites Internet dédiés (7) ainsi que la production de documents et de messages ciblant plus particulièrement les populations les plus fragiles ou les plus précaires en termes d’accès à la vaccination. De plus, depuis le 1er janvier 2018, 11 vaccinations sont désormais devenus obligatoires dans le calendrier vaccinal des nourrissons nés depuis cette date (contre 3 antérieurement), incluant la vaccination contre la rougeole 20.
L’objectif d’augmentation de la CV est non seulement de protéger directement les sujets vaccinés, mais également d’éviter la contamination des sujets vulnérables, à risque de formes graves, à travers une immunité de groupe, en particulier les personnes ne pouvant bénéficier de la vaccination (enfants âgés de moins de 1 an, personnes immunodéprimées, femmes enceintes). Cette immunité de groupe ne pourra être obtenue que grâce à des niveaux de CV très élevés dans toute la population ciblée par les recommandations actuelles. En effet, tant que la CV des nourrissons n’atteindra pas le niveau requis de 95% pour les deux doses 21 et que le rattrapage des cohortes d’enfants plus âgés et de jeunes adultes ne sera pas renforcé, on risque d’observer une alternance de vagues épidémiques suivies de périodes de « lune de miel ».
Cela pose la question de l’échéance à laquelle la France atteindra l’objectif d’élimination de la rougeole, alors que cet objectif avait été initialement adopté pour 2010, lors de la mise en place du plan d’élimination de la rougeole et de la rubéole congénitale en 2005. À moyen terme, la décision du ministère chargé de la Santé de rendre la vaccination des nourrissons obligatoire à compter de 2018 devrait toutefois contribuer à la réalisation de cet objectif.
Remerciements
Nous remercions tous les acteurs de la DO, cliniciens, bio‑logistes et professionnels des ARS et Cire.
Références
pii=18-00224.
Citer cet article
sation.gouv.fr/gf/cerfa_12554.do




