Épidémie d’infections invasives à méningocoque B dans le Beaujolais (Rhône), 2016 : organisation de la vaccination et résultats
// Community outbreak of serogroup B invasive meningococcal disease in Beaujolais, Rhône (France) 2016: Organization of the immunization campaign and results
Résumé
Introduction –
La survenue d’une épidémie d’infections invasives à méningocoque B sur une zone restreinte du département du Rhône a conduit l’Agence régionale de santé Auvergne-Rhône-Alpes (ARS) à organiser, d’avril à juin 2016, une campagne de vaccination exceptionnelle ciblant les personnes âgées de 2 mois à 24 ans, résidant ou gardées ou scolarisées ou travaillant sur cette zone.
Planification de la campagne –
Dans un contexte d’accès restreint au vaccin, une offre de vaccination graduée a été proposée, depuis l’offre existante jusqu’au déploiement de centres de vaccination dédiés en passant par la vaccination en milieu scolaire. La gratuité et une pharmacovigilance renforcée ont été garanties. La couverture vaccinale (CV) a été suivie afin d’ajuster le dispositif au fil du temps.
Résultats –
Sur 4 438 personnes à vacciner résidant dans la zone, 2 038 ont reçu une dose de vaccin Bexsero®, 1 716 personnes deux doses et 7 enfants trois doses. La CV estimée globale était de 47% à une dose et de 40% à deux doses. Elle variait selon la classe d’âge et la commune de résidence. La CV à deux doses était de 63% pour les 3-11 ans, de 36% pour les 12-15 ans, de 30% pour les 0-3 ans et de 8% pour les 16-24 ans. Près des trois quart (74%) des doses ont été dispensées en milieu scolaire et 15% par les médecins libéraux.
Avec 152 notifications d’effets indésirables (EI) adressées au Centre régional de pharmacovigilance (CRPV) pour 4 069 doses administrées au total, le taux de notification pour 100 doses administrées était de 3,7%. Au total, 309 EI ont été rapportés, pour un profil de tolérance au vaccin qui était globalement conforme aux données du résumé des caractéristiques du produit.
Discussion –
Les CV les plus hautes ont été obtenues en milieu scolaire. Outre cette facilitation de l’accès à l’information et à la vaccination pour les familles, les séances ont été proposées rapidement après l’alerte. Les CV les plus basses des 0-3 ans et des 16-24 ans posent question, au regard de l’incidence élevée de la maladie dans ces classes d’âge. La méconnaissance du vaccin par les professionnels de santé, l’absence de connaissance sur la durée de protection, un vaccin non accessible initialement en pharmacie et peut-être une certaine défiance de la population envers les vaccinations, ont contribué pour partie à ces résultats.
Abstract
Introduction –
The occurrence of a community outbreak of serogroup B invasive meningococcal disease (IMD) on a limited geographical area of the Rhône district (France) prompted the local health agency (Agence régionale de santé – ARS) to organize a vaccination campaign between April and June 2016. The target population was people aged 2 months-24 years, living, cared for, studying or working in the epidemic zone.
Campaign planning –
In a context of restricted access to vaccines, the ARS has proposed a graduated vaccination campaign, starting from the existing offer to the deployment of dedicated vaccination centers and vaccination in schools. Free vaccination and enhanced pharmacovigilance were guaranteed. Vaccination coverage was continuously monitored in order to adjust the organization of the campaign.
Results –
The target population comprised 4,438 people, of whom 2,038 received one dose, 1,713 two doses and 7 three doses of vaccine. The overall vaccination coverage (VC) was estimated at 47% for one dose and 40% for two doses, and varied according to age, and place of residence. The estimated VC at two doses was the highest for children 3-11 years old (63%) and the lowest for 0-3 years old (30%) and 16-24 years old (8%). Nearly three-fourths (74%) of doses were administered in school settings and GPs accounted for 15% of the doses administered. With 152 reports of adverse effects (AE) sent to the Regional Pharmacovigilance Centre (CRPV) for 4,069 doses administered, the notification rate was 3.7 for 100 doses administered. In all, 309 AE were reported for a tolerance profile of the vaccine which complied with the summary of the product characteristics.
Discussion –
The highest VC rates were observed in school settings. In addition to facilitating access to information and vaccination for families, sessions were proposed shortly after the alert. The lowest VCs for 0-3 and 16-24 year-olds pose question, given the high incidence of the disease in these age groups. The lack of knowledge on the vaccine by health professionals, the lack of knowledge on long term protection, a vaccine initially unavailable in pharmacies, and perhaps a certain mistrust of the population towards vaccinations, contributed in part to these results.
Introduction
Entre le 29 février et le 20 mars 2016, une épidémie clonale de 4 cas d’infections invasives liées à une souche rare de méningocoque B (IIMB) (deux grappes de 2 cas, la deuxième grappe étant survenue dans une même classe d’école maternelle) est survenue dans une zone rurale de 15 km de diamètre située au nord du département du Rhône 1. Cette épidémie a motivé l’organisation d’une campagne de vaccination par l’Agence régionale de santé Auvergne-Rhône-Alpes (ARS). Une cellule d’expertise multidisciplinaire a défini les communes concernées et la population ciblée par la vaccination : les enfants et jeunes adultes âgés de 2 mois à 24 ans résidant, gardés, scolarisés ou travaillant dans la zone épidémique.
Cet article a pour objet de présenter les modalités pratiques de mise en œuvre de la campagne de vaccination, qui s’est déroulée principalement du 1er avril au 30 juin 2016, et ses résultats en termes de couverture vaccinale (CV) et de pharmacovigilance.
Planification de la campagne
Référentiels
L’ARS s’est appuyée sur le Guide des vaccinations 2012 de l’Institut national de prévention et d’éducation pour la santé (bonnes pratiques vaccinales) 2 et le guide de préparation d’une campagne de vaccination exceptionnelle du Ministère des Affaires sociales et de la Santé de 2012 3 pour définir, avec les professionnels de santé de terrain, un dispositif gradué depuis l’utilisation de l’offre de vaccination existante jusqu’au déploiement de centres de vaccination dédiés.
En France, un seul vaccin contre le méningocoque B dispose d’une autorisation de mise sur le marché (AMM) : le vaccin Bexsero®. Les schémas vaccinaux appliqués à la population-cible étaient issus de l’avis du Haut Conseil de santé publique (HCSP) du 25 octobre 2013 relatifs à l’utilisation du Bexsero® 4 (tableau 1) et conformes au résumé des caractéristiques du produit (RCP). De deux à trois doses sont recommandées en primovaccination selon l’âge à l’initiation du schéma vaccinal. La population-cible comptant environ 4 500 sujets (dont 4 338 résidant dans la zone épidémique), le besoin en vaccins était estimé à 9 000 doses pour la couvrir entièrement.
Principes et organisation
Une gratuité totale a été garantie aux familles. L’ARS a pris en charge le coût des actes médicaux libéraux, une partie du coût des vaccins ainsi que les frais d’organisation de la campagne. L’Assurance maladie a remboursé 65% des coûts du vaccin à l’ARS.
Le Conseil départemental du Rhône (service de Protection maternelle et infantile, PMI) et l’Éducation nationale ont mis à disposition les équipes de vaccinateurs (médecins, infirmiers, puéricultrices et secrétariat) dans les établissements scolaires.
Pour assurer le pilotage opérationnel, l’ARS a constitué une cellule interne réunissant des professionnels de la veille sanitaire du Rhône et un pharmacien du pôle sécurité des activités de soins et vigilances. Une infirmière a été recrutée à temps plein. Un appui a été demandé au pool des médecins de l’ARS pour le maintien de l’activité de veille sanitaire. D’autres services de l’ARS ont contribué au déploiement de la campagne (secrétariat et direction générale). Un pilotage institutionnel, porté par la direction de la Santé publique et les directions support (achats, finances), assurait la validation des engagements financiers, la communication et la réponse aux sollicitations de la presse.
Approvisionnement en vaccins et autres matériels
À la différence du Royaume-Uni, le vaccin Bexsero® ne fait pas partie du calendrier vaccinal en France et ses indications sont limitées. Avec l’appui de la Direction générale de la santé et de l’Agence nationale de sécurité du médicament et des produits de santé (ANSM), l’ARS a préempté les 9 000 doses estimées nécessaires auprès de l’unique fabricant, permettant l’obtention d’un prix négocié.
Pour assurer la disponibilité du vaccin tout au long de la campagne, l’ARS a passé sept commandes auprès du laboratoire-fabricant. Le stockage des vaccins a été réalisé dans la chambre froide du laboratoire d’analyses médicales du centre hospitalier (CH) le plus proche de la zone épidémique. Assurée initialement par l’ARS, puis par un logisticien de la Réserve sanitaire mobilisé par l’Établissement de préparation et de réponse aux urgences sanitaires (Eprus, intégré en mai 2016 au sein de Santé publique France), la livraison des vaccins dans les établissements scolaires a été réalisée dans le respect de la chaîne du froid (glacières électriques puis location d’un véhicule réfrigéré, réfrigérateurs sur les lieux de vaccination).
Les consommables financés par l’ARS et les matériels relatifs aux déchets d’activités de soins ont été commandés et fournis par le CH.
À partir du 1er juin, pour la deuxième dose, les familles ont eu la possibilité de se faire vacciner par leur médecin traitant. À ce stade, le nombre de deuxièmes doses à faire appliquer par les médecins libéraux avait été estimé à environ 500, hors établissements scolaires. L’ARS a passé des conventions avec 12 officines qui ont pu se faire livrer en vaccins par leur grossiste-répartiteur. Un système de bons à deux feuillets (l’un rempli par le pharmacien et le second par le médecin) a permis le remboursement de ces professionnels de santé par l’ARS, à la fois du coût du vaccin et de la consultation de vaccination. La complétude du feuillet médecin permettait de suivre la CV.
Pharmacovigilance renforcée
Cette campagne de vaccination avec Bexsero® étant la première en France depuis son AMM en 2013, une pharmacovigilance renforcée a été mise en place avec l’aide du Centre régional de pharmacovigilance (CRPV) de Lyon. Elle s’est appuyée sur une fiche de déclaration spécifique remise systématiquement à chaque personne vaccinée en main propre avec une enveloppe T et les coordonnées téléphoniques du CRPV.
Suivi de la couverture vaccinale
La CV a été suivie par la Cellule d’intervention de Santé publique France (Cire) en région Auvergne-Rhône-Alpes tout au long de la campagne, en récupérant les fichiers des personnes vaccinées remplis dans les centres de vaccination, puis les feuillets des professionnels de santé libéraux. Elle a été calculée en rapportant le nombre de vaccinations (numérateur) à la population-cible (dénominateur). La CV n’a donc pu être estimée que lorsque le dénominateur était connu ou estimé, à savoir pour les personnes résidant dans la zone épidémique ou celles fréquentant les établissements scolaires.
Offre de vaccination, acteurs impliqués dans la campagne (figure 1)
Renforcement de l’offre de vaccination existante
Avec le soutien logistique de l’ARS et du Comité départemental d’hygiène sociale (CDHS), structure départementale de vaccination publique, des séances de vaccination dédiées ont été mises en place dans deux centres de PMI (situés en périphérie de la zone) pour augmenter l’offre à destination des enfants de moins de 6 ans et, surtout, des enfants non scolarisés de moins de 3 ans. De même, les permanences de l’antenne locale du CDHS située à proximité de la zone épidémique ont été augmentées.
Organisation de vaccinations dans les établissements scolaires et autres lieux de garde
Les établissements scolaires desservant la zone épidémique étaient au nombre de 21 : 15 localisés dans la zone épidémique
(crèche, écoles maternelle et élémentaires, maison familiale et rurale, cours d’anglais privé), 5 établissements publics du
secondaire (4 collèges et un lycée) en périphérie de la zone et 1 école privée secondaire située hors du département. Ces
21 établissements ont été ciblés pour l’application de la première dose entre le 6 avril et le 14 mai et de la deuxième dose
du 6 au 24 juin. Le planning a dû tenir compte des vacances de printemps, du 11 au 24 avril, retardant la vaccination dans
six établissements primaires (figure 1). Pour pallier cette difficulté et augmenter l’offre de proximité, il a été fait appel, à partir des congés de printemps, à la Réserve sanitaire pour armer des centres communaux ad hoc
(voir ci-après).
Les vaccinations scolaires ont été intégralement assurées par les équipes médicales et paramédicales de la PMI et de l’Éducation nationale. Les parents devaient signer le formulaire d’autorisation de vacciner leurs enfants et joindre le carnet de santé. Il leur était également demandé de fournir leur numéro de sécurité sociale pour un remboursement de l’ARS par l’Assurance maladie.
Le suivi en temps réel de la CV montrant de faibles taux de vaccination sur les tranches d’âge des 11-24 ans durant les vacances de printemps, des séances de vaccination, initialement non prévues, ont été programmées dans les collèges, le lycée et l’établissement privé tous situés hors zone, du 9 au 14 mai.
Des lieux de vaccination ad hoc
Ce dispositif a été renforcé par des permanences de soirée (18 à 20 heures) et le samedi de 9 à 11 heures, assurées par des médecins libéraux du secteur dans les locaux de la maison médicale de garde desservant la zone épidémique. Une offre alternative était ainsi proposée jusqu’au 31 mai 2016 aux familles d’enfants de moins de 3 ans, non concernées par les vaccinations scolaires, qui ne s’étaient pas déplacées en PMI ni dans un centre dédié. Enfin, un centre communal de vaccination ad hoc armé par la Réserve sanitaire a été ouvert alternativement dans la salle des fêtes de trois communes de la zone épidémique. Ces permanences, mises en place dès le 15 avril (fin de la première semaine des vacances de printemps), accueillaient la population-cible, du lundi au samedi inclus, de 11 à 18 heures. Les séances de vaccination communale, peu fréquentées, ont ensuite été réduites à 2 jours par semaine (mercredi et samedi) puis elles ont été interrompues définitivement à la mi-mai. Pour la deuxième dose, l’ARS n’a sollicité la Réserve sanitaire que pour un appui logistique sur l’organisation de la chaîne du froid, les cabinets de médecine générale complétant les schémas vaccinaux initiés hors vaccination scolaire.
 Agrandir l'image
Agrandir l'imageCommunication
Les professionnels de santé (médecins, pharmaciens) ont été les premiers ciblés : en premier lieu les médecins traitants des patients concernés, puis tous ceux installés dans un secteur centré sur la zone épidémique. Des courriers de l’ARS et via l’Union régionale de professionnels de santé (URPS) leur ont été adressés personnellement. Des réunions ont été organisées au CH pour les équipes hospitalières et à plusieurs reprises sur site, à destination des pharmaciens et médecins libéraux.
La population-cible a été informée par différents canaux (courriers de l’ARS distribués par les écoles, par les services de PMI et les assistants maternels, réunions d’informations dans les écoles avant les séances de vaccination, spots radio, affichages et flyers à disposition dans les mairies, les pharmacies, les lieux de soins ou cabinets libéraux, communiqués de presse…). L’ARS a également mis en place une page dédiée sur son site Internet ainsi qu’un numéro vert à la mi-avril.
L’information des services de PMI, de l’Éducation nationale et du CDHS s’est faite par l’intermédiaire de leurs directions respectives, impliquées dès la première réunion d’experts dans le processus décisionnel et organisationnel.
Dès le lancement de la campagne, les maires des communes concernées ont été informés et leurs services ont été sollicités pour aider les écoles à organiser la vaccination, pour l’affichage de flyers et, si possible, la distribution de lettres dans les boîtes aux lettres de leurs administrés.
Résultats
Couverture vaccinale
Au total, 4 069 vaccins ont été administrés (2 222 premières doses, 1 840 secondes doses et 7 troisièmes doses), dont 308 chez des personnes-cibles non domiciliées dans la zone épidémique. La CV globale estimée des personnes résidant dans la zone était de 47% à une dose et 40% à deux doses, et elle variait avec l’âge (tableau 2). Les enfants de 3-11 ans avaient la CV la plus élevée (63%), suivis des 12-15 ans (36%) et des moins de 3 ans (30%). La CV était la plus basse chez les 16-24 ans (8%).
 Agrandir l'image
Agrandir l'imageLa CV obtenue dans les écoles primaires variait de 56 à 82% selon le groupe scolaire. De façon inexpliquée, la CV dans la classe fréquentée par les cas de la 2e grappe a été parmi les plus basses. Dans les établissements du second degré, la CV variait de 23 à 64%. Elle variait également selon la commune de résidence (tableau 3). La meilleure CV n’a pas été obtenue dans une commune de résidence d’un cas ni dans une commune où un centre ad hoc avait été ouvert, mais dans la commune où une pédiatre libérale avait apporté son soutien actif dans la promotion et la réalisation de la vaccination des enfants.
 Agrandir l'image
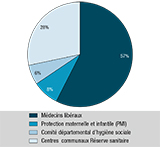
Agrandir l'imageLa majorité des vaccinations a été administrée en milieu scolaire d’une part (74%) et par les médecins libéraux d’autre part (15% des doses administrées). Hors établissements scolaires, les médecins libéraux ont contribué pour 57% des doses appliquées au travers des permanences en maison médicale de garde puis en cabinet (figure 2).
L’essentiel des vaccinations (premières doses) réalisées en dehors des centres scolaires a eu lieu dans le mois suivant le début de la campagne (figure 3).
 Agrandir l'image
Agrandir l'image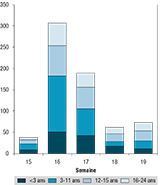 Agrandir l'image
Agrandir l'imagePharmacovigilance
Sur la période du 29 mars au 14 novembre 2016, pour 4 069 doses administrées, 152 notifications correspondant à 141 patients ont été reçues au CRPV 5, soit un taux de notifications par doses appliquées de 3,7/100 doses (IC95%: [3,2-4,4]). Les notifications ont rapporté un total de 309 effets indésirables (EI) survenus lors de la première ou de la deuxième dose. Plus de la moitié des effets survenait dans les heures suivant la vaccination et leur durée médiane était de 2 jours [0-74].
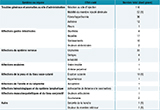
Le profil de tolérance observé était conforme aux données du RCP, avec principalement des effets locaux ou régionaux (plus de 80% des signalements) et des effets systémiques de type céphalées et fièvre (11%) (tableau 4). Les données disponibles ne permettaient pas de conclure sur une différence de tolérance entre la première et la deuxième dose. Aucun patient n’a présenté d’EI remplissant les critères de gravité selon la définition de l’Organisation mondiale de la santé. Quatre EI ont été jugés médicalement significatifs : une éruption cutanée généralisée, un cas d’impotence fonctionnelle du membre vacciné pendant 24 heures post-injection, une synovite de la hanche et une douleur du membre inférieur.
 Agrandir l'image
Agrandir l'imageDiscussion – conclusion
La CV moyenne estimée dans la population-cible était de 40%, avec de fortes variations selon l’âge et la commune de résidence. L’objectif de la campagne était de conférer une protection individuelle dans une population non-immune et non une protection collective, car l’effet du Bexsero® sur le portage pharyngé du méningocoque n’est pas démontré 6. Une étude américaine a rapporté la survenue d’un cas d’IIMB chez un sujet non vacciné dans une université où la couverture vaccinale par Bexsero® était de 89%. Ce résultat suggère donc que la souche peut continuer à circuler malgré une CV très élevée 7. De ce fait, aucun objectif chiffré en termes de CV n’avait été prédéterminé.
La CV la plus élevée a été observée chez les enfants de 3-11 ans (63%) et, dans une proportion plus faible, chez les 12-15 ans (36%). La classe d’âge des 3-11 ans correspond aux enfants scolarisés en maternelle et élémentaire pour lesquels des séances de vaccination ont été organisées au sein des établissements scolaires. Outre cette facilitation de l’accès à l’information et à la vaccination pour les familles, ces séances ont aussi été les premières à être proposées à partir de l’alerte.
Dans la classe où la deuxième grappe de cas est survenue et où l’on observe une des CV parmi les plus basses, la prophylaxie par rifampicine qui a été administrée à tous les élèves de cette classe a été évoquée comme une éventuelle explication de la faible adhésion à la recommandation vaccinale, le vaccin devenant non nécessaire. Les taux de CV les plus bas ont été observés pour les enfants de moins de 3 ans (30%) et chez les 16-24 ans (8%). Ces résultats posent question car ces deux classes d’âge sont les plus à risque d’IIM. Ces deux classes d’âge ne sont pas des populations “captives” et la diffusion de l’information jusqu’aux parents de jeunes enfants qui ne sont pas gardés en structure collective ainsi qu’aux jeunes adultes est plus difficile. Concernant les adolescents et jeunes adultes, même s’ils se montrent convaincus de l’intérêt des vaccinations, ils ont en général peu de connaissances sur les maladies qu’elles permettent d'éviter 8.
Quelles que soient les classes d’âges, les niveaux de CV obtenus sont peu élevés, évoquant des freins à la vaccination, tels que la réticence de la population française vis-à-vis des vaccins 9. L’absence de connaissance sur la durée de protection d’un vaccin récemment mis sur le marché, une primovaccination pour les moins de 24 mois de deux ou trois injections selon l’âge à l’initiation, à ajouter au calendrier vaccinal habituel, peuvent aussi contribuer à expliquer la faible adhésion des parents et de certains professionnels de santé.
La dynamique du nombre de vaccins administrés au cours du temps (hors vaccinations scolaires où les dates étaient fixées dans le cadre de l’organisation de la campagne) montre l’importance d’intervenir rapidement dès la diffusion de l’alerte. Une vaccination proposée cinq semaines après l’alerte, comme cela a été le cas dans les lycées et collèges en raison des congés scolaires, risque d’être perçue comme incohérente.
L’implication rapide des professionnels de santé du territoire est essentielle dans la dynamique de la campagne, comme relais d’information et comme effecteurs. Toutefois la non-disponibilité du vaccin en officine pour la première dose a certainement limité la possibilité des médecins traitants de vacciner leur patientèle. La participation de médecins hospitaliers (pédiatrie et infectiologie) dès la cellule d’aide à la décision pourrait faciliter le co-portage de la campagne, aux côtés de l’ARS, en direction des médecins libéraux et de la population.
En revanche, la population a peu utilisé les centres dédiés communaux armés par la Réserve sanitaire, en dépit de leur localisation au sein d’une zone épidémique de 15 km de diamètre et de leur amplitude d’ouverture. Une communication insuffisante sur l’existence de ce dispositif complémentaire ad hoc peut en être une des explications, alors que l’objectif poursuivi était d’offrir aux collégiens, lycéens et jeunes travailleurs des lieux de vaccination à proximité de leur résidence ou de leur travail dès la fin de la première semaine des vacances de printemps, sans attendre la rentrée scolaire.
Par ailleurs, l’ARS s’est adressée directement aux maires des communes et à leurs services mais n’a pas sollicité l’appui des services préfectoraux pour faciliter leur mobilisation. La plupart des communes étaient de petite taille, avec du personnel et des moyens très limités. Si l’accueil de l’ARS par les équipes municipales a été très positif, notamment lors des séances de vaccination, très peu se sont mobilisées pour faire passer l’information à leurs administrés par la distribution de courriers dans les boîtes aux lettres et/ou par un affichage dans des points stratégiques.
La mise à disposition systématique d’une fiche de pharmacovigilance incitait les professionnels ou les sujets vaccinés à déclarer les effets secondaires. Les données de pharmacovigilance montrent une bonne tolérance du vaccin, conforme aux RCP. Même si le taux de notification d’EI est relativement faible (3,7/100 doses appliquées), il est probable que la sous-déclaration concerne essentiellement les effets secondaires mineurs et que les effets les plus sérieux ont été déclarés de manière plus exhaustive.
Une étude psychosociale conduite au décours de la campagne apporte des clés de compréhension sur la réception et l’adhésion à la campagne du public, des institutions et des professionnels, et propose des pistes d’amélioration pour de futures campagnes 10.
Références
spf___internet_recherche/INV13487
Remerciements
Les auteurs remercient le Pr D. Floret, le Pr Debord, Santé publique France (I. Parent, C. De Bort, J Boudot), la Direction générale de la santé (B. Worms et C. Lazarus), le Dr C. Cros, médecin conseiller technique Éducation nationale (EN) du département du Rhône et de la métropole de Lyon, Mesdames et Messieurs les maires des 12 communes concernées, les directeurs d’établissements scolaires concernés, les personnels des équipes de vaccinateurs de l’EN, de la PMI et du Comité départemental d’hygiène sociale ainsi que les médecins libéraux de la Maison médicale de garde de Belleville, les responsables des 12 pharmacies du secteur, les directions et leurs équipes des CH de Villefranche et de Belleville, ainsi que les différents services de l’Agence régionale de santé qui ont été mis à contribution et plus particulièrement les Drs A.M. Durand et B. Morel.





