L’infection par le virus de l’hépatite Delta. Données françaises récentes
// The hepatitis Delta virus infection: recent data in France
Résumé
L’infection par le virus de l’hépatite Delta (VHD), satellite du virus de l’hépatite B (VHB), est considérée comme la forme la plus sévère de l’hépatite virale aiguë ou chronique. Elle est responsable d’hépatites fulminantes aiguës ou d’hépatites chroniques graves pouvant évoluer rapidement vers la cirrhose et le carcinome hépatocellulaire.
En dépit de données manquantes dans de nombreuses régions du monde endémiques pour le VHB, et malgré des campagnes de vaccination anti-VHB conduites dans plusieurs pays, l’infection à VHD est loin d’être une maladie en voie de disparition dans le monde, avec environ 15 à 20 millions de sujets infectés. En effet, les études récentes conduites dans différents pays d’Europe, aux États-Unis, en Australie, en Afrique, au Moyen-Orient et en Asie ont montré une prévalence de l’infection Delta (définie par le taux de portage des anticorps anti-VHD chez les patients VHB positifs) plus importante que prévue et l’existence de régions de forte endémie.
La réalité de l’infection à VHD en France est peu connue. L’objectif de cette étude est de tenter de faire un état de la situation à partir de l’analyse : (1) des données de l’étude nationale réalisée par l’Institut de veille sanitaire chez les patients nouvellement pris en charge pour une hépatite B chronique entre 2008 et 2010 ; (2) d’études réalisées chez les donneurs de sang par l’Institut national de la transfusion sanguine associé au Centre national de référence (CNR) des hépatites B, C et Delta ; (3) des différentes études conduites par le CNR associé hépatite Delta et (4) des résultats préliminaires de l’étude Deltavir, réalisée chez plus de 1 000 patients ayant présenté une infection à VHD active et dont les souches virales collectées de façon prospective de 2001 à 2013 sont conservées dans la biothèque du CNR associé hépatite Delta.
Cette analyse montre une prévalence faible de l’infection VHD en France, avec un portage des anticorps anti-VHD chez 4% des patients VHB positifs. Ces patients sont originaires principalement de pays de forte ou de moyenne endémie. Toutes ces études fournissent des données épidémiologiques, démographiques, cliniques et biologiques de l’infection Delta en France, ainsi que les caractéristiques virologiques des souches infectantes. Elles indiquent la nécessité absolue d’effectuer le dépistage des anticorps anti-VHD chez tous les patients infectés par le VHB, ainsi que la quantification de la charge virale du VHD chez les patients positifs à l’aide de techniques diagnostiques prenant en compte la grande diversité génétique du VHD.
Abstract
Infection with the hepatitis delta virus (HDV), satellite of the hepatitis B virus (HBV), is considered the most severe form of acute or chronic viral hepatitis, leading to acute fulminant or severe chronic hepatitis that may progress more rapidly to cirrhosis and hepatocellular carcinoma.
While data are lacking in many parts of endemic areas for HBV, and despite anti-HBV vaccination campaigns conducted in several countries, HDV infection is far from being a vanishing disease in the world, with about 15 to 20 million infected people. Indeed, recent studies conducted in different countries in Europe, the USA, Australia, Africa, the Middle East, Asia, showed a prevalence of Delta infection (defined by the carrier rate of anti HDV antibodies in HBV-infected individuals) greater than expected and reveal the existence of highly endemic areas.
HDV infection in France is little known. The aim of this study is to assess HDV infection according to data from: (1) the national survey data conducted by the French Institute for Public Health Surveillance among new patients treated for chronic hepatitis B between 2008 and 2010; (2) studies in blood donors by the National Institute of Blood Transfusion associated with the National Reference Centre (NRC) for hepatitis B, C and Delta (3) the various studies conducted by the NRC-associated laboratory for hepatitis Delta (HDV-NRC), and (4) preliminary results of the Deltavir study in more than 1,000 patients with an active HDV infection, whose viral strains collected prospectively from 2001 to 2013 are stored in the HDV-NRC biobank.
These studies indicate a low prevalence of HDV infection in France with a carriage rate of anti-HDV antibodies (HDV-Abs) of 4% in HBV-positive patients, patients mainly originated from high or medium endemic countries. These studies provide epidemiological, demographic, clinical and biological data about HDV infection in France as well as virological characteristics of the infecting strains. They indicate the absolute need for the screening of HDV-Abs in all HBV-infected patients and the quantification of the HDV viral load in the positive ones, using diagnostic assays that take into account the great HDV genetic diversity.
Introduction
Le virus de l’hépatite Delta (VHD) est un petit virus à ARN de 1,7kb, simple brin, de polarité négative. Ce génome est étroitement lié à deux protéines virales : la petite protéine Delta ou p24 (en raison de son poids moléculaire de 24 kDa) et la grande protéine Delta ou p27. Ces deux protéines vont former, avec l’ARN génomique, la ribonucléoprotéine Delta, qui sera enveloppée par les protéines de surface (AgHBs) du VHB auxiliaire pour former la particule virale Delta 1.
Le VHD est caractérisé, comme son virus auxiliaire le VHB, par une très grande variabilité génétique et une répartition géographique caractéristique. Le genre Deltavirus est aujourd’hui classé en 8 génotypes (HDV-1 à -8). HDV-1 est ubiquitaire et retrouvé dans tous les continents. HDV-2 et -4 sont retrouvés en Sibérie, en Asie de l’Est et du Sud, au Japon et aux Îles Miyako. L’HDV-3 a été décrit au nord de l’Amérique du Sud et dans le bassin amazonien. Les génotypes HDV-5, -6, -7 et -8 ont été caractérisés, au Centre national de référence (CNR) associé hépatite Delta, chez des patients originaires d’Afrique subsaharienne vivant en France, infectés dans leurs pays d’origine 2,3. Des études récentes conduites en Afrique confirment ces données virologiques 4,5,6,7,8.
Données épidémiologiques
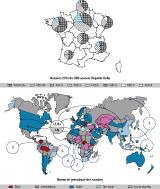
On estime aujourd’hui qu’environ 15 à 20 millions d’individus seraient infectés par le VHD dans le monde, avec des prévalences très variables selon les régions (figure). L’Afrique subsaharienne et centrale, le Bassin amazonien (Brésil, Pérou, Venezuela et Colombie), les îles du Pacifique et le Vietnam seraient des zones de forte endémie VHD, de même que la Turquie, la Mongolie, le sud de l’Italie et les républiques de l’ex-Union soviétique. L’Europe du Nord et de l’Ouest ainsi que l’Amérique du Nord et l’Australie seraient au contraire des zones de faible endémie. Des zones de moyenne endémie ou d’endémie intermédiaire ont été proposées, mais des données manquent pour beaucoup de régions du monde. Cette classification déjà ancienne repose sur le portage des anticorps anti-Delta totaux dans le sérum des patients infectés. Cependant, la détection des anticorps ne signifie pas forcément la présence et la réplication du virus. Aussi toutes ces données devront-elles être reconsidérées à l’aide d’outils diagnostiques sérologiques et moléculaires validés.
 Agrandir l'image
Agrandir l'image
Données cliniques
La transmission du VHD se fait selon les mêmes modes que ceux du VHB, son virus auxiliaire.
L’infection VHD nécessite absolument l’infection VHB concomitante. Elle peut être simultanée, on parle alors de co-infection, ou peut survenir chez un patient déjà infecté de façon chronique par le VHB, on parle alors de surinfection Delta.
La co-infection est responsable à la fois d’une hépatite aiguë B (attestée par la positivité des IgM anti-HBc) et Delta, qui peut être limitée ou au contraire fulminante, avec une prévalence de 2 à 10% selon les études contre 1‰ pour le VHB seul. L’évolution vers la chronicité est observée dans 20 à 30% des cas.
Au cours de la surinfection, l’hépatite fulminante peut survenir dans 15% des cas et l’hépatite chronique Delta dans 80%, avec aggravation des lésions hépatiques et évolution rapide (5 à 10 ans) vers la cirrhose et le carcinome hépatocellulaire (CHC) 9,10,11. Ce dernier point est toutefois l’objet de controverses 12,13,14. Des études in vitro ont pu cependant proposer des mécanismes de pathogenèse spécifique du VHD, impliquant la grande protéine Delta dans l’activation de facteurs de transcription tels STAT-3 et NF-κB et la voie du stress oxydant via la voie de la NADPH oxydase 15.
Ces données indiquent que l’infection B/Delta se traduit en règle générale par une maladie hépatique beaucoup plus grave qu’avec l’infection VHB seule.
Diagnostic
Le diagnostic VHD repose en première intention sur la recherche des anticorps totaux, principalement IgG, à l’aide des trousses commerciales disponibles qui donnent des résultats comparables. En cas de négativité, on peut parler d’absence d’infection Delta. Toutefois, en cas de persistance des signes cliniques en l’absence d’autres causes évidentes, ceux-ci peuvent être contrôlés avec un délai d’une semaine à quinze jours, ou mieux, la recherche de l’ARN Delta peut être d’emblée demandée.
Il existe aussi des trousses IgM anti-VHD. L’une des spécificités du VHD est que les anticorps IgM anti-VHD persistent au cours l’infection chronique. Cependant, les IgM anti-VHD peuvent manquer chez des patients africains ayant pourtant une réplication virale active attestée par une charge virale ARN positive 16. Dans certaines études, leur présence, même en cas de charge virale ARN négative, est une contre-indication à l’arrêt des traitements et, de ce fait, la détection des IgM peut avoir un intérêt dans la prise en charge des patients 17,18.
Il existe une trousse commerciale permettant la recherche des antigènes Delta. Ceux-ci sont fugaces dans le sérum, très vraisemblablement complexés aux anticorps qui apparaissent assez précocement. Au cours de notre expérience de plus de six années, les antigènes Delta n’ont été détectés que dans environ 3 cas pour 1 000 dans des infections avérées, et souvent chez des patients co-infectés par le VIH. Ainsi, cette recherche ne nous semble pas utile dans le diagnostic de routine de l’infection.
La recherche des ARN Delta avec, surtout, la quantification de la charge virale ARN par RT-PCR en temps réel, est le maître examen pour le diagnostic et la prise en charge des patients 17,19. La présence d’ARN Delta permet non seulement de confirmer le caractère réplicatif de l’infection, mais aussi de mesurer l’efficacité du traitement institué. Cependant, bien qu’un étalon international OMS VHD soit disponible depuis octobre 2013, il n’existe pas de kits commerciaux fiables permettant de quantifier les souches virales quel que soit leur génotype. En effet, des contrôles de qualité nationaux et internationaux organisés par le CNR associé hépatite Delta ont montré que la plupart des tests commerciaux et des techniques « maison » développés étaient incapables, par comparaison aux résultats obtenus par la méthode consensus du CNR associé hépatite Delta 19, de quantifier ou sous-estimaient de façon très importante la charge virale chez des patients infectés par des souches africaines (de génotype -1, -5, -6, -7 et -8), mais aussi parfois par des souches européennes VHD-1 20,21. Toutefois, le génotypage du VHD n’a pas d’intérêt en pratique clinique, aucune étude systématique n’ayant été conduite pour la mise en évidence d’une corrélation entre génotype et évolutivité de la maladie.
La charge virale VHB est un élément important de suivi des patients. Elle est souvent inhibée lors de la réplication du VHD. Des mécanismes moléculaires ont été proposés pour rendre compte de cette observation 22,23. La quantification de l’ADN VHB permet aussi au clinicien de faire les choix thérapeutiques par analogues de nucléos(t)ides et/ou interféron α (IFNα) pégylé en cas de co-réplication des deux virus ou de la prédominance de l’un d’entre eux.
Enfin, plus récemment, plusieurs équipes ont montré un intérêt de l’étude de la cinétique de quantification de l’antigène HBs dans le suivi des patients infectés. La diminution de l’antigène HBs serait un marqueur pronostique favorable de la résolution de l’infection VHB/VHD 24.
Traitements
Le traitement de l’hépatite repose sur une seule molécule : l’IFNα à fortes doses, sous sa forme standard autrefois et maintenant pégylée, et ce pendant au moins 18 mois. Des analogues de nucléos(t)ides anti-VHB n’ont pas montré d’efficacité sur le VHD. Ils sont utilisés en fonction de l’évaluation de la maladie VHB sous-jacente. Les taux de guérison sont estimés entre 25% et 40%, les rechutes étant souvent la règle à l’arrêt du traitement. Tout récemment, des inhibiteurs d’entrée du virus, le Myrcludex® 25 et des inhibiteurs de la prénylation (la prénylation étant un événement-clé de la morphogenèse des virions Delta) 25 ont été proposés. Ils sont en cours d’essais cliniques de phase 2.
L’infection VHD en France
L’infection VHD est encore peu étudiée en France. Cependant, plusieurs travaux réalisés ou en cours par les services cliniques, par l’Institut de veille sanitaire (InVS), chez les donneurs de sang par l’Institut national de la transfusion sanguine (INTS) (associé au CNR des hépatites B, C et Delta) ou l’analyse des données du CNR associé hépatite Delta (étude Deltavir en cours) nous permettent d’appréhender la réalité de l’infection VHD en France.
Données épidémiologiques
L’étude nationale réalisée par l’InVS sur près de 1 500 patients nouvellement pris en charge pour une hépatite B chronique entre 2008 et 2010 dans les différents pôles de référence en France (services hospitalo-universitaires) a permis d’évaluer la prévalence du portage des anticorps anti-VHD à 5,5%. Ces patients étaient âgés de 39 ans en moyenne ; il s’agissait majoritairement d’hommes (61%), nés dans une région de forte ou moyenne endémie pour le VHD (67%). Environ un tiers d’entre eux étaient nés en France métropolitaine, 13% en Europe de l’Est et du Sud et 8% en Asie. Le principal facteur de risque est la notion de contamination en pays d’endémie (naissance, voyage ou conjoint originaire de ces régions).
Une étude chez 4 500 donneurs de sang bénévoles sur 15 années (1997-2011) confirme que la France est une zone de faible endémie pour le VHD, avec une prévalence entre 1 et 2% 26.
L’étude la plus significative concernant les patients infectés par le VHD en France est celle réalisée à partir de la biothèque du CNR associé hépatite Delta, qui comporte plus de 1 000 échantillons de patients répliquant le VHD collectés de façon prospective de 2001 à 2011 (étude Deltavir soutenue par l’ANRS). Des données épidémiologiques, cliniques, biologiques et virologiques ont pu être recueillies pour 1 112 patients. Les premiers résultats de cette étude confirment que les patients VHD sont principalement des hommes (68,4%), originaires d’Afrique (59,5%), d’Europe de l’Ouest (18,5%), d’Europe centrale et de l’Est (13,7%), d’Asie (4,5%), du Moyen-Orient (2,9%) et d’Amérique du Sud (0,6%). L’âge médian est de 38 ans (IQR:30;45). Les patients africains sont plus jeunes que les patients non africains (36 versus 42 ans, p<0,001).
Données cliniques et virologiques
Sur le plan clinique, les premières données issues de l’étude Deltavir montrent que 28% des patients ont une cirrhose histologique ; 15% un épisode (ou plus) de décompensation hépatique et 2,7% des patients un CHC. Au cours de la période médiane de suivi de 4,4 ans [1,4 à 8,9], 20% des patients ont développé une cirrhose, 10% une décompensation hépatique et 6,5% un CHC, et ont donc un risque calculé sur 10 ans de développer une cirrhose, une décompensation hépatique ou un CHC respectivement de 40%, 31% et 15%. En analyse multivariée, l’âge avancé et les γGT élevées sont des facteurs de risque indépendants de développer ces complications. De plus, l’élévation des transaminases ASAT (aspartate aminotransférases) est aussi associée à la survenue de la cirrhose ; une thrombopénie <100 000/mm3 et un taux de prothrombine <60% à la décompensation hépatique aiguë, et l’obésité (indice de masse corporelle : IMC >30 kg/m2) au CHC. Il convient de souligner aussi que, dans cette cohorte de patients, la cirrhose est significativement moins fréquente chez les patients africains que chez les patients européens et asiatiques. Enfin, de façon intéressante, la charge virale VHD élevée persistante est un facteur de risque de décompensation hépatique 27.
Sur le plan virologique, la charge virale VHD médiane est de 6,17 (IQR:4,76;7,18) log10 copies/mL, sans différence selon le sexe. En revanche, une diminution significative est observée en fonction de l’âge des patients (p=0,03). De même, le niveau de réplication virale est plus faible chez les patients d’origine africaine que chez ceux originaires d’autres régions (p<0,0001). En analyse multivariée, l’âge et l’origine africaine sont associés de façon indépendante à la réplication virale. Il n’y a pas de différence de capacité réplicative des virus en fonction du génotype.
Concernant les génotypes des souches virales, hormis le génotype 4 (VHD-4) restreint à l’Asie du Sud-Est, tous les génotypes VHD sont trouvés en France. Le génotype VHD-1 (incluant les sous-génotypes -1 africain) est largement majoritaire (77,4%). Le VHD-5 représente 16,1% des souches caractérisées alors que les génotypes VHD-6, -7 et -8 sont plus rares (1,8, 3,1 et 1,2% respectivement). Des souches de génotypes -2 (Asie) et -3 (Amérique du Sud) ont été retrouvées de façon exceptionnelle (0,2% chacun). Ces différents génotypes circulent sur tout le territoire français avec des proportions différentes selon l’origine géographique des populations migrantes, impliquant la nécessité de quantifier la charge virale pour une prise en charge optimale des patients 27,28.
Conclusion
La prévalence de l’infection par le VHD en France, calculée sur la présence d’anticorps anti-VHD totaux, est faible, de l’ordre de 4%. Elle est liée principalement aux patients originaires de pays de forte ou de moyenne endémie (Afrique et Europe de l’Est surtout) vivant en France. Le VHD est responsable d’une maladie hépatique beaucoup plus grave avec une évolution vers la cirrhose, la décompensation hépatique aiguë et le CHC, et doit donc être systématiquement recherché chez tous les patients infectés par le VHB. Le diagnostic repose sur la recherche des anticorps anti-VHD totaux ; en cas de positivité, les IgM seront recherchées. Celles-ci persistent avec la réplication chronique, mais peuvent manquer chez des patients africains. Le diagnostic de l’infection chronique active réplicative repose sur la recherche de l’ARN Delta par RT-PCR qualitative, mais surtout quantitative, permettant de mesurer le niveau de réplication et l’efficacité du traitement par l’IFNα pégylé, en attendant l’avènement d’autres thérapeutiques (inhibiteurs d’entrée du virus et inhibiteurs de la prénylation). En l’absence de kits commerciaux validés, cet examen sera réalisé dans des laboratoires de référence capables de quantifier toutes les souches quel que soit leur génotype. Enfin, l’évaluation de la maladie virale due au VHB sous-jacente, avec détermination de la charge virale ADN VHB et quantification de l’AgHBs, est déterminante pour la prise en charge thérapeutique optimale des patients infectés.
Remerciements
À Ségolène Brichler, Frédéric Le Gal, Wael Mansour : Centre national de référence associé hépatite Delta, Laboratoire de bactériologie, virologie, hygiène ; AP-HP, Hôpital Avicenne, Bobigny ; Sylvie Chevret : DBIM, AP-HP Hôpital Saint-Louis, Paris ; Dominique Roulot : Unité d’Hépatologie, AP-HP, Hôpital Avicenne, Bobigny ; Françoise Roudot-Thoraval : Département de santé publique, AP-HP, Hôpital Mondor, Créteil ; Syria Laperche : Institut national de la transfusion sanguine, Paris ; au Centre national de référence des hépatites B, C et Delta ; au Groupe Deltavir.




