Leptospirose à Mayotte : apports de la surveillance épidémiologique, 2008-2015
// Leptospirosis in Mayotte: contribution of epidemiological surveillance, 2008-2015
Résumé
Les premiers cas de leptospirose dans l’archipel des Comores et à Mayotte ont été rapportés au début des années 1980. De 1998 à 2008, une vingtaine de cas par an, en moyenne, étaient rapportés pour Mayotte par le Centre national de référence de la leptospirose (Institut Pasteur, Paris). Une surveillance spécifique de la maladie a été mise en place en 2008, d’abord par un simple recueil des cas déclarés par le Centre hospitalier de Mayotte et de leurs caractéristiques administratives puis, à partir de 2010, par une investigation épidémiologique des cas.
De 2008 à 2015, 808 cas de leptospirose (100 cas par an en moyenne, soit une incidence annuelle moyenne de 47 cas pour 100 000 habitants) ont été rapportés, dont 203 hospitalisés. Entre 2012 et 2015, 13 personnes ont été hospitalisées en réanimation, soit 10% des cas hospitalisés. Des cas sont rapportés tout au long de l’année, mais majoritairement durant la saison des pluies, de janvier à mai. L’incidence varie selon les années mais aussi selon les communes, en fonction de la pluviométrie et des activités humaines. La leptospirose à Mayotte est une maladie à la morbidité élevée, touchant deux fois plus les hommes que les femmes et avec 20% de moins de 15 ans. Cependant, les formes graves et les décès sont rares (taux de létalité moyen 0,9%). La grande majorité des cas recensés sur l’île est liée à des pratiques agricoles ou de jardinage et d’élevage à domicile, ou à des loisirs en eau douce (pêche, baignade en rivière ou bassins), ainsi qu’à la marche pieds nus ou sans chaussures fermées. Il existe probablement une exposition intra ou péridomiciliaire liée à un habitat dégradé (RR=1,5 [1,4-1,8]). Des expositions professionnelles sont retrouvées dans 4 cas sur 10, et 1 cas sur 10 est uniquement d’origine professionnelle. Les professions à risque retrouvées sont celles classiquement décrites : agriculteurs, ouvriers du bâtiment, éboueurs et militaires. La plupart des cas sont isolés, sans lien entre eux.
À Mayotte, l’information et la vigilance des personnels de santé vis-à-vis de cette maladie sont en partie à l’origine de sa faible létalité. Si l’amélioration de l’habitat, de la gestion des eaux usées et des eaux pluviales, de la gestion des déchets et de l’accès à l’eau sont autant d’éléments pour le contrôle de la leptospirose dans l’avenir, il est nécessaire de mieux informer la population sur les modes de contamination pour réduire les expositions, ainsi que sur la nécessité de consulter rapidement en cas de fièvre afin de diminuer la sévérité de la maladie. Un travail de prévention est également à mener auprès des professions à risque, notamment les agriculteurs et les éleveurs.
Abstract
The first cases of leptospirosis in the Comoros archipelago and in Mayotte were reported in the early 1980s. From 1998 to 2008, 20 cases per year on average were reported for Mayotte by the National Reference Centre for Leptospirosis (Pasteur Institute of Paris). A specific surveillance of the disease was implemented in 2008, starting with a simple collection of cases reported by the Mayotte Hospital Centre (CHM) and their administrative characteristics, followed in 2010, by an epidemiological investigation of cases.
From 2008 to 2015, 808 cases of leptospirosis (100 cases per year on average, corresponding to an average annual incidence of 47 cases per 100,000 inhabitants) were reported, 203 of whom were hospitalized. From 2012 to 2015, 13 patients were hospitalized in intensive care, representing 10% of all hospitalized cases. Cases are reported throughout the year, but mostly during the rainy season, from January to May. The incidence varies from one year to the other and also from one municipality to the other, depending on rainfalls and human activities. Leptospirosis in Mayotte is a disease with high morbidity, affecting twice as many men as women, and with 20% of cases under 15 years. However, severe forms and deaths are rare (0.9% mean case fatality rate). The vast majority of cases recorded on the island are related to farming or gardening practices, domestic farming practices or to freshwater recreation activities (fishing, swimming in rivers or ponds), walking barefoot or without closed shoes. An intra– or peri-residential exposure associated with degraded habitat (RR=1.5 [1.4-1.8]) is much likely. Occupational exposures are found in 4 out of 10 cases, and 1 in 10 cases only has an occupational origin. Occupations at risk are those which are traditionally described: farmers, construction workers, garbage collectors and the military. Most cases are isolated and unrelated.
In Mayotte, the information and vigilance of the health personnel regarding this disease are partly responsible for its low lethality. While the improvement of habitat, wastewater and rainwater management, and access to water are all factors contributing to the control of leptospirosis in the future, it is necessary to better inform the population about the modes of contamination to reduce exposures and the need to quickly seek medical assistance in order to reduce the severity of the disease. Preventive work is also needed for high-risk occupations, particularly farmers and livestock keepers.
Introduction
L’île de Mayotte, 101e département français, est située dans l’archipel des Comores, dans l’Océan Indien, entre Madagascar et la côte orientale de l’Afrique. Le climat y est tropical et humide, avec une saison chaude et pluvieuse (de décembre à mars) et une saison sèche (de juin à septembre) séparées par deux intersaisons. Sa population a atteint 212 645 habitants en 2012, avec un taux de croissance annuel de 2,7% entre 2007 et 2012 1. L’immigration légale et illégale y est importante et, au recensement de 2012, 40% des habitants étaient d’origine étrangère. La population de Mayotte est jeune (46% de moins de 15 ans) et croît régulièrement du fait du taux de natalité élevé et de l’immigration. Cette situation ne facilite pas le rattrapage du retard accumulé par le département en termes d’assainissement, d’accès à l’eau et de qualité du logement. Ainsi, en 2013, 37% de la population vivait dans des logements en tôle. Malgré les importants progrès réalisés, 28% de la population n’avait pas accès à l’eau courante (contre 75% en 2002) et 52% des logements n’avaient ni baignoire ni douche 2.
Peu de données sont disponibles sur l’historique de la leptospirose dans l’archipel des Comores et à Mayotte. Une première étude hospitalière rétrospective (1984-1989) portant sur 42 cas à Mayotte avait souligné l’importance des formes sévères et estimé l’incidence annuelle de cette zoonose à 3,8 cas pour 100 000 habitants, avec une prédominance du sérogroupe Icterohaemorrhagiae 3. Une deuxième étude rétrospective hospitalière (2002-2003) rapportait 13 cas, essentiellement des formes graves, dont un tiers de formes pulmonaires, avec une létalité de 23% et une incidence estimée à 6 cas pour 100 000 habitants 4. En 2016, une troisième étude rétrospective hospitalière, menée dans le service de réanimation du Centre hospitalier de Mayotte (CHM) et portant sur la période 2009-2014, a retrouvé 34 formes graves prises en charge, dont 3 décès (létalité en réanimation : 8,8%). Un tiers des patients présentaient des signes d’insuffisance respiratoire et deux tiers une oligo-anurie nécessitant une épuration extra-rénale 5. De 1998 à 2008, le Centre national de référence (CNR) de la leptospirose à l’Institut Pasteur de Paris a reçu en moyenne 23 souches par an (16 à 37 cas annuels) en provenance de Mayotte, soit une incidence annuelle moyenne de 15 cas pour 100 000 habitants (9 à 28 cas pour 100 000 habitants) 6. À Mayotte, le sérogroupe Mini est majoritaire et représentait l’essentiel des souches de 2007 à 2015. Le sérogroupe Icterohaemorrhagiae, qui représentait 6% des tests de micro-agglutination microscopique (MAT) de 2003 à 2008, n’a plus jamais été retrouvé depuis 2008. Ces dernières années, les tests sérologiques et les investigations moléculaires ont confirmé l’absence du sérogroupe Icterohaemorrhagiae et la prédominance d’une grande diversité de souches spécifiques (dont l’espèce L. mayottensis), tant dans les réservoirs animaux que chez l’Homme à Mayotte 7,8,9,10,11 (voir l’article de P. Tortosa et coll. dans le même numéro). En 2011, une enquête a estimé à 16,5% (IC95%: [13,6-19,7]) laséroprévalence de la leptospirose à Mayotte chez les plus de 5 ans 12. Elle était plus élevée chez les agriculteurs (47,6%) et les personnes en contact avec des zébus et/ou des chèvres (34,8%). Le sérogroupe majoritaire était Mini (74,5%) et le sérogroupe Icterohaemorrhagiae était retrouvé chez seulement 2,5% des sujets porteurs d’anticorps anti-leptospires.
Depuis 2008, une surveillance spécifique de la leptospirose a progressivement été mise en place à Mayotte par l’Agence régionale de santé Océan Indien (ARS OI) 13. Nous présentons ici les résultats de huit années de cette surveillance (2008-2015).
Matériel et méthodes
Tous les cas de leptospirose confirmés par amplification génomique (PCR) ou sérologie (Elisa IgM et/ou MAT) contractés à Mayotte par des résidents mahorais doivent être rapportés à la plateforme de veille et d’urgences sanitaires de l’ARS OI. Les cas contractés hors de Mayotte ou survenus chez des touristes ne sont pas pris en compte. Depuis 2008, la surveillance de la leptospirose à Mayotte est basée essentiellement sur la déclaration, par le laboratoire du CHM, des cas biologiquement confirmés.
Depuis 2010, le suivi de la leptospirose est intégré à un dispositif de surveillance des syndromes dengue-like pour toutes les consultations réalisées au CHM. Tout patient pour lequel est décrit un syndrome dengue-like (fièvre d’apparition brutale avec au moins un des symptômes suivants, en l’absence de tout autre point d’appel infectieux : douleurs musculo-articulaires, manifestations hémorragiques, céphalées frontales, asthénie, douleur rétro-orbitaire, éruption maculo-papuleuse) fait l’objet d’une recherche systématique par PCR ou sérologie portant sur trois arboviroses (dengue, chikungunya et fièvre de la vallée du Rift) et sur la leptospirose. Pour chaque cas confirmé, les données suivantes sont systématiquement collectées au niveau hospitalier : âge, sexe, commune de résidence, notion d’hospitalisation et évolution (guérison, décès).
À partir de fin 2009, une investigation à domicile a été progressivement mise en place autour de chaque cas confirmé de leptospirose. Au moyen d’un questionnaire standardisé, des informations ont été collectées sur les données cliniques et les facteurs de risque de contamination : type d’habitation, présence d’animaux, environnement rural ou urbain, activités à risque (agriculture, activités aquatiques, profession à risque, etc.). L’objectif était de proposer des mesures correctrices et d’adapter les messages de prévention. L’investigation à domicile a été systématisée en 2010. Depuis la mise en place de la surveillance, le questionnaire a été modifié à plusieurs reprises. Ainsi, les questions sur les manifestations cliniques et sur la survenue d’inondations au domicile ont été supprimées car les réponses étaient le plus souvent manquantes. Des informations ont été rajoutées : depuis 2012, la notion d’un séjour en réanimation et, depuis 2015, la notion d’un voyage dans les quatre semaines précédant la date de début des signes, la fréquence de la marche pieds nus ou sans chaussures fermées, la présence de volailles ou de lémuriens dans l’entourage des cas et la disponibilité de l’eau courante à domicile.
Les données du Programme de médicalisation des systèmes d’information (PMSI) et du CNR ont été utilisées pour évaluer l’exhaustivité du système de surveillance de la leptospirose à Mayotte. Ainsi, une extraction des données du PMSI du CHM a été réalisée pour la période 2008-2015 (dossiers avec un des codes suivants en diagnostic principal : A270, A278, A279). Le nombre de cas hospitalisés, le nombre de cas pris en charge en réanimation et le nombre de décès survenus ont été colligés. Les nombres de cas annuels diagnostiqués par le CNR de la leptospirose ont été extraits de ses rapports annuels de 1998 à 2015 et utilisés pour calculer des taux d’incidence annuelle. Les taux d’accroissement de la population fournis par l’Insee (Institut national de la statistique et des études économiques) ont été utilisés pour estimer la population annuelle entre deux recensements. Les données de pluviométrie ont été fournies par Météo France.
Les données ont été analysées à l’aide du logiciel Epi Info™7.1.2.0. Les proportions ont été comparées à l’aide du test du Chi2 et les données quantitatives à l’aide du test de Student ou du test de Kruskall-Wallis en cas d’inégalité des variances.
Résultats
Surveillance spécifique
De 2008 à 2015, 808 cas de leptospirose ont été rapportés à Mayotte dans le cadre la surveillance épidémiologique spécifique, avec une moyenne annuelle de 100 cas par an (min 40 ; max 172). Ceci représente une incidence annuelle moyenne de 47 cas pour 100 000 habitants (min 21 ; max 81) (figure 1).
 Agrandir l'image
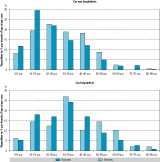
Agrandir l'imageLa distribution mensuelle des cas de leptospirose suit la pluviométrie, avec un décalage de trois mois entre le début des pluies et l’apparition des premiers cas de l’épidémie saisonnière (figure 2). À partir de la mise en place effective d’un formulaire d’investigation en 2010, 675 cas sur 686 rapportés ont été enregistrés dans une base de données (98%) et 401 ont été investigués (soit en moyenne 59%, variant de 40 à 80% selon les années).
Au cours de cette période, la majorité des cas de leptospirose à Mayotte (70%) n’a pas été hospitalisée. Parmi les 30% hospitalisés (203 cas), la prise en charge en service de réanimation n’a été systématiquement rapportée que depuis 2012. Treize personnes (3% des cas de leptospirose à Mayotte de 2012 à 2015) ont été hospitalisées en service de réanimation, soit 10% des cas hospitalisés pour leptospirose de 2012 à 2015 (4 à 16% selon les années). De 2010 à 2015, 6 décès ont été enregistrés, soit une létalité de 0,9% sur l’ensemble des cas.
 Agrandir l'image
Agrandir l'imageLa répartition des cas par tranche d’âge et par sexe parmi les cas hospitalisés et non hospitalisés est donnée dans la figure 3. Les femmes représentaient 31% des cas de leptospirose déclarés de 2010 à 2015. Elles étaient plus jeunes que les hommes (28 ans versus 32 ans ; p=0,005), mais la part des moins de 15 ans (25%) était identique chez les hommes et les femmes. Le taux d’hospitalisation était le même quel que soit le sexe. Les cas hospitalisés étaient significativement plus âgés globalement (35 vs 27 ans, p<10-5) et ce quel que soit le sexe : 37 vs 30 ans chez les femmes (p=0,01) et 34 vs 26 ans chez les hommes (p<10-5). La part des hospitalisations était près de deux fois plus importante chez les plus de 15 ans : 26% vs 15% (risque relatif, RR=1,7 [1,2-2,5]).
 Agrandir l'image
Agrandir l'imageRépartition géographique
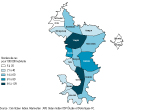
De 2010 à 2015, la commune de résidence des cas était connue pour 537 cas (79%). L’incidence moyenne annuelle de 2010 à 2015 variait, selon les communes, de 5 cas pour 100 000 habitants à Pamandzi à 126 cas pour 100 000 habitants à Chirongui (figure 4). Elle variait au sein d’une même commune selon les années, sans qu’il soit possible d’identifier de communes particulièrement à forte incidence. Ainsi, au niveau de la commune de Bandraboua, l’incidence annuelle a varié, de 2010 à 2015, de 0 à plus de 100 cas pour 100 000 habitants selon les années.
 Agrandir l'image
Agrandir l'imageExpositions liées à l’environnement
Des données sur l’environnement et les activités ou expositions à risque étaient disponibles pour 401 cas et sont présentées dans le tableau.
 Agrandir l'image
Agrandir l'imagePlus de la moitié des cas (56%) vivaient en milieu rural ou semi-urbain. La plupart habitaient des logements en tôle (60%) ou en dur (38%). La part de patients vivant dans des logements en tôle était près de deux fois plus élevée chez les patients atteints de leptospirose qu’en population générale (60% vs 37% ; p<10-7 ; RR=1,5 [1,4-1,8]).
Des rats étaient présents dans l’environnement de 85% des patients. D’autres animaux étaient retrouvés dans l’entourage des cas : animaux de rente (ovins, caprins, bovins) dans 44% des cas, animaux de compagnie (chiens, chats) dans 19% des cas, volailles dans 13% des cas et/ou lémuriens (makis) dans 5% des cas. La présence de volailles ou de lémuriens est possiblement sous-estimée. En effet en 2015, année où la présence de ces animaux a été recherchée par deux questions spécifiques, des volailles et des lémuriens ont été retrouvés, respectivement, autour de 69 et 34% des cas.
Une accumulation de déchets dans leur environnement était retrouvée dans 52% des cas.
Enfin, de 2010 à 2012, la survenue d’inondations était rapportée par 25% des sujets enquêtés.
Activités à risque
Une seule possibilité de contamination était retrouvée pour 59% des patients (activité agricole seule pour 36%, activité aquatique seule pour 22%, exposition professionnelle à risque seule, hors agriculture, pour 1%). Plusieurs possibilités de contamination étaient retrouvées pour 32% des cas (activité agricole et exposition aquatique cumulées dans 26% des cas). Une exposition professionnelle à risque était retrouvée pour 171 cas (43%), dont 88% d’agriculteurs ou éleveurs, 8% de travailleurs du bâtiment, 2% de militaires et 2% d’éboueurs/dératiseurs. Au total, 11% des cas étaient formellement liés à une contamination professionnelle, aucune autre exposition n’ayant été retrouvée. Dans 9% des cas, aucune activité à risque n’était retrouvée, en dehors de l’évolution dans un milieu potentiellement contaminé par la présence de réservoirs animaux. En 2015, année d’introduction du questionnement spécifique, la marche pieds nus ou sans chaussures fermées était retrouvée comme mode de contamination possible pour un tiers des patients et comme seule exposition à risque pour 7 cas (8%).
La plupart des sujets ne se protégeaient pas lors des activités à risque. En effet, 86% ne portait aucun moyen de protection lors des activités agricoles et 14% avait une protection partielle (bottes ou gants). Lors du ramassage ou de la manipulation de déchets, 80% ne portait aucun moyen de protection et 20% une protection partielle (bottes ou gants).
Données du PMSI
De 2008 à 2015, 274 patients ont été hospitalisés à Mayotte pour une leptospirose, soit en moyenne 34 cas par an (min 7 ; max 36). Parmi eux, 29 personnes (11% des cas hospitalisés) ont été admises en réanimation, soit en moyenne 3,6 cas par an (min 1 ; max 5). Depuis 2008, 6 décès directement ou indirectement liés à l’infection sont survenus, ce qui correspond à moins d’un décès par an en moyenne (min 0 ; max 2) et à une létalité de 3,7% parmi les cas hospitalisés.
Données du CNR
Avant la mise en place de la surveillance en 2008, le nombre moyen de cas confirmés par le CNR était de 23/an de 1998 à 2008 vs 109/an de 2009 à 2015. Le taux d’incidence annuel moyen rapporté était de 15 cas pour 100 000 habitants de 1998 à 2008 contre 54 cas pour 100 000 habitants de 2009 à 2015.
L’évolution du nombre de cas déclarés à la surveillance, du nombre de cas rapportés au CNR et du nombre de cas hospitalisés selon la surveillance et selon le PMSI est présentée figure 5.
 Agrandir l'image
Agrandir l'imageDiscussion
Avec une incidence moyenne annuelle estimée à 100 cas pour 100 000 habitants, Mayotte fait partie des zones de haute endémicité. Des cas peuvent y être rapportés toute l’année, mais la majorité survient lors de la saison des pluies, de janvier à mai. Le nombre de cas rapportés depuis la mise en place de la surveillance a varié selon les années. Ces variations sont dues à la montée en puissance de la surveillance épidémiologique (multiplication par deux en moyenne du nombre de cas rapportés depuis 2008), aux variations de la pluviométrie et à l’effort de dépistage (mise en place du diagnostic moléculaire, multiplication par cinq du nombre de souches envoyées au CNR). Dans l’île de Futuna (Pacifique Sud), la mise en place d’une surveillance spécifique de la leptospirose avait entrainé une multiplication par huit de son incidence annuelle moyenne mesurée, entre les périodes pré– et post-surveillance 14. À Mayotte, l’apparition des cas suit l’évolution de la pluviométrie avec un décalage de trois mois : le pic de cas en avril suit le pic de pluviométrie de janvier. T. Lernout et coll., qui avaient déjà mis en évidence ce phénomène à Mayotte avec une corrélation statistiquement significative, expliquent ce décalage par le détrempage des terrains après les pics de pluviométrie qui favoriserait le maintien dans le milieu des leptospires pathogènes 13. Selon cette étude, l’importance des pics saisonniers est davantage liée au nombre de mois consécutifs avec de fortes pluies qu’au total de pluviométrie. Si l’on compare la pluviométrie des trois premiers mois de l’année depuis la mise en place de la surveillance (en excluant l’année 2008 où les données de surveillance ou du CNR sous-estiment le nombre de cas rapportés, notamment lors de l’épidémie saisonnière), la pluviométrie lors des deux années à plus haute incidence (2011 et 2014) est constamment supérieure à 250 mm de pluie par mois et ne diminue pas au cours des trois premiers mois de l’année. Néanmoins, ces deux pics d’incidence ont été observés lors d’épidémies de dengue 13,15. Or, la recherche d’une leptospirose étant intégrée au dispositif de surveillance des syndromes dengue-like à Mayotte, l’augmentation des consultations pour syndrome dengue-like a entrainé ces deux années une augmentation du nombre de PCR et de sérologies de la leptospirose réalisées. Cette augmentation du dépistage peut donc aussi expliquer les incidences élevées enregistrées au cours de ces deux années. Les données de la surveillance épidémiologique sont superposables à celles du CNR à partir de 2009 en termes d’incidence et celles du PMSI sont superposables aux données recueillies par le système de surveillance sur les cas hospitalisés (nombre de cas, hospitalisation en réanimation et décès ; données non présentées).
L’exhaustivité de la surveillance de la leptospirose à Mayotte peut être considérée comme bonne par comparaison aux données extérieures. Depuis 2010, si on excepte l’année 2011 (plus de 80% de cas investigués), seuls 50% des cas en moyenne ont bénéficié d’une enquête. Ceci est dû en partie à la difficulté à retrouver certains patients à Mayotte par défaut d’adresse, de téléphone ou du fait de coordonnées fournies erronées (volontairement ou non), au manque de personnel entre 2012 et 2015 et au surplus de charge de travail occasionné par l’épidémie de dengue de 2013-2014 15.
Le risque de contracter une leptospirose est géographiquement hétérogène à Mayotte. Depuis 2010, des cas ont été rapportés dans l’ensemble de l’île, mais les taux d’incidence annuelle moyens varient selon les communes de 5 cas pour 100 000 habitants à 126 cas pour 100 000 habitants. Seule la commune de résidence étant prise en compte, il est possible que l’attribution d’un cas à une commune se fasse par excès, notamment pour les cas ayant été exposés en dehors de leur lieu de résidence lors de leur activité professionnelle. Ainsi, il est probable que des cas rattachés au milieu urbain, notamment à Mamoudzou et en Petite Terre, soient liés à une activité agricole dans d’autres communes.
Si le nombre de cas rapportés chaque année est élevé, le nombre de décès (moins d’un décès par an depuis 2010) et la létalité (0,9%) sont faibles. La plupart des cas ne sont pas hospitalisés mais pris en charge en ambulatoire, et les hospitalisations en réanimation sont rares (3%). La rareté apparente des formes sévères pourrait s’expliquer par la prédominance de souches endémiques de pathogénicité modérée ainsi que par un diagnostic et une prise en charge médicale précoces dans les centres de santé, notamment la prescription d’une antibiothérapie dès la suspicion clinique. À Futuna, malgré une incidence élevée (800 cas pour 100 000 habitants) et la prédominance du sérogroupe Icterohaemorrhagiae, la situation est identique, avec une létalité à 0,5% 14. La rareté des formes sévères et des décès y est attribuée à la précocité de l’évocation du diagnostic et de la prise en charge. Les données cliniques pour répondre à ces hypothèses sont parcellaires à Mayotte. En effet, il n’existe pas de dossiers cliniques pour les patients non hospitalisés vus dans les centres de santé, l’ensemble des informations étant noté dans leur carnet de consultation. De plus, les patients ne reviennent pas automatiquement consulter et l’évolution n’est pas forcément connue. La leptospirose est considérée habituellement comme responsable de formes moins sévères chez les femmes et les moins de 15 ans 16,17. À Mayotte, si le taux d’hospitalisation est identique chez les hommes et les femmes, les moins de 15 ans, qui représentent près d’un tiers des cas, sont deux fois moins souvent hospitalisés que les plus de 15 ans. La jeunesse de la population peut ainsi en partie expliquer le faible taux d’hospitalisation. Pour les cas hospitalisés, il n’existe pas de recueil systématisé des informations cliniques au niveau du dispositif de surveillance. Pour les formes vues en ambulatoire, qui constituent la majorité des cas, une étude prospective pourrait répondre à la question, en proposant le remplissage d’une fiche clinique pour chaque suspicion de leptospirose vue en centre de santé et en mettant en place une deuxième consultation pour les cas confirmés afin d’en renseigner l’évolution clinique.
Contrairement aux îles voisines des Seychelles et de La Réunion, où les hommes adultes représentent 95% des personnes atteintes, les femmes et les jeunes sont une part importante des cas de leptospirose diagnostiqués à Mayotte 18,19. Cette observation peut s’expliquer par plusieurs facteurs. La population est très jeune (46% de moins de 15 ans). Outre leur implication dans les tâches agricoles, les femmes et les enfants sont également exposés à la leptospirose via la fréquentation des rivières pour la baignade pour les plus jeunes et les activités domestiques pour les plus âgées, lessive notamment, du fait de l’absence, pour une partie de la population, d’un accès régulier à l’eau courante 2. Ces données sont concordantes avec celles de l’enquête de séroprévalence de 2011, qui retrouvait une prévalence importante chez les femmes (14% contre 20% pour les hommes) et une exposition importante des moins de 15 ans, puisque 12% des 5 à 15 ans étaient porteurs d’anticorps (Ac) anti-leptospires contre 16 à 30% des plus de 15 ans, selon les tranches d’âge 12.
La surveillance retrouve les caractéristiques environnementales favorables à la contamination qui ont été identifiées lors de l’enquête de séroprévalence : présence de rats près du domicile, vie en milieu rural, contact avec des bovins ou des chèvres 12. Les personnes vivant dans des logements en tôle sont près de deux fois plus représentées parmi les cas de leptospirose (RR=1,5 [1,4-1,8]). L’association habitat précaire – leptospirose a déjà été décrite 16,20,21. Une urbanisation non planifiée, avec un accès limité à l’eau et des systèmes de drainage des eaux et de gestion des déchets non adaptés, favorise la présence de boues, la prolifération des rats et donc la contamination et le maintien dans l’environnement de leptospires pathogènes et, possiblement, une contamination intradomiciliaire et péridomiciliaire 20,21,22,23,24. La contamination de jeunes enfants (de 2010 à 2015 à Mayotte, les moins de 5 ans représentaient 1,2% des cas de leptospirose) peut s’expliquer par cette exposition intra ou péridomiciliaire, de même que celles des patients n’ayant d’autre facteur de risque retrouvé que la marche pieds nus ou sans chaussures fermées. Lors de l’étude de séroprévalence, les sujets vivant dans une maison avec un sol en dur (béton ou carrelage) étaient deux fois moins porteurs d’Ac anti-leptospires 12.
Dans cette étude, la proximité d’un point d’eau, le contact avec l’eau de la rivière, la baignade et la lessive en rivière (séroprévalence de 20%) étaient significativement associés à la présence d’Ac anti-leptospires, ainsi que le fait d’être agriculteur (séroprévalence de 48%) ou sans emploi (séroprévalence de 21%). Les modes de contamination majeurs identifiés par la surveillance sont les activités agricoles (agriculture, élevage), les activités aquatiques (baignade, lessive) et les activités professionnelles et habitus exposant au contact avec de la boue (métier du bâtiment, marche pieds nus). Les expositions sont souvent multiples et il est possible de rattacher une contamination à un seul type d’exposition dans seulement 6 cas sur 10. Des expositions professionnelles ont été retrouvées dans 4 cas sur 10 et 1 cas sur 10 est uniquement d’origine professionnelle. Les professions à risque retrouvées sont celles classiquement décrites : agriculteurs, ouvriers du bâtiment, éboueurs et militaires 25.
Au cours des années de surveillance, les questionnaires ont évolué. Ces modifications résultent de l’évolution des connaissances (résultats de l’enquête de séroprévalence de 2011) et de choix pragmatiques (suppression des données cliniques se révélant impossibles à collecter par exemple). Néanmoins, malgré les difficultés à investiguer l’ensemble des cas et ces modifications successives, les données de surveillance permettent de mieux connaitre la situation de la leptospirose à Mayotte. Comme dans la plupart des îles tropicales, la leptospirose à Mayotte est une pathologie endémique à recrudescence saisonnière de janvier à mai. La majorité des cas sont vus en deuxième partie de saison des pluies, de mars à mai. Si l’incidence y est comparable à celle des zones de haute endémicité comme les Seychelles, la Nouvelle-Calédonie ou la Polynésie française, la létalité est en revanche trois fois plus faible 19,26,27. La situation de Mayotte en termes d’épidémiologie est comparable avec celle de Futuna, qui associe incidence très élevée (844 cas pour 100 000 habitants) et faible létalité (0,5%) 14. Si, dans les îles du Sud-Ouest de l’Océan Indien, la situation de la leptospirose est bien documentée, notamment aux Seychelles, à La Réunion et à Maurice, peu de données existent sur les souches de leptospires et sur l’incidence de la leptospirose à Madagascar et dans les autres îles de l’archipel des Comores, en l’absence d’outils diagnostiques et de système de surveillance 18,19,28,29,30. Le système de surveillance à Mayotte a permis, depuis sa mise en place, d’identifier des cas aigus de leptospirose (confirmés par PCR) en provenance de Madagascar et des Comores, notamment Anjouan et Moheli 8. L’absence de déclaration de cas de leptospirose dans le reste de l’archipel des Comores n’est peut-être pas due seulement aux faibles possibilités diagnostiques et à l’absence de surveillance, mais aussi à un profil épidémiologique comparable à celui de Mayotte (polymorphisme clinique, faible part de formes sévères et faible létalité). Cette hypothèse est confortée par une étude sérologique réalisée aux Comores, qui retrouvait un taux de positivité au MAT de 3% à 10% selon les îles sans détection du sérogroupe Icterohaemorrhagiae 31. Le sérogroupe Icterohaemorrhagiae a été identifié par le passé aux Comores de même qu’à Mayotte, mais ne semble plus y être présent, tant au niveau des cas humains que des réservoirs animaux 3,32. Une transition, passée inaperçue du fait de l’absence de surveillance, s’est peut être produite par le passé, aboutissant à l’absence actuelle de ce sérogroupe. Ceci pourrait expliquer l’important taux de létalité hospitalière rapporté dans les années 1990 et 2000 à Mayotte contre le taux actuel de 0,9% 3,4. Une autre explication possible est un sous-diagnostic, dans les années 1990 et 2000, des formes moins sévères de leptospirose, qui aurait amené à surestimer la part des formes graves et des décès.
La leptospirose est une maladie de la pauvreté, liée à des conditions de vie entrainant une exposition élevée à un environnement contaminé par les leptospires, mais aussi une maladie professionnelle et, de plus en plus souvent, liée à la pratique de certains loisirs (activités aquatiques, raids, courses nature) 33,34. À Mayotte, l’amélioration de l’habitat, de la gestion des eaux usées, des eaux pluviales, de la gestion des déchets et de l’accès à l’eau est un élément clé pour le contrôle de la leptospirose dans l’avenir 18. À l’heure actuelle, en l’absence de possibilité de vaccination et avec une chimioprophylaxie limitée à des situations particulières, peu d’outils sont disponibles pour y limiter le poids de la leptospirose en termes de morbidité, sévérité et létalité 32,35,36. L’information et la vigilance des personnels de santé ont montré leur importance pour réduire les formes sévères de la leptospirose et sont sans doute en partie à l’origine de la faible létalité à Mayotte 14,37. Un élément important est l’information et l’éducation de la population sur les modes de contamination, pour réduire les expositions, et sur la nécessité de consulter rapidement en cas de fièvre, afin de diminuer la sévérité de la maladie 14,37. Par exemple, la marche pieds nus, identifiée comme un mode majeur de contamination à La Réunion dans les années 1970, n’y est plus qu’un mode de contamination anecdotique 18. Il apparait nécessaire de réaliser à Mayotte un travail de prévention auprès des professions à risque, notamment les agriculteurs et les éleveurs qui représentent une grande part des cas. La généralisation des équipements de protection personnels (gants, bottes, vêtements longs) permettrait sans doute d’éviter un grand nombre de cas, même si leur acceptabilité par les professionnels reste à évaluer 38,39.
Remerciements
À l’ensemble des déclarants (cliniciens hospitaliers ou de ville, biologistes médicaux hospitaliers ou de ville), aux personnels de la CVAGS de Mayotte pour leur aide dans la surveillance et pour la réalisation des enquêtes et au service statistique de la DSP de l’ARS OI pour la cartographie.
Références
_aux_recommandations_pour_la_prevention_de_la_leptospirose_en_cas_d_activite_professionnelle_a_risque.pdf




