Surveillance des infections humaines par hantavirus en France métropolitaine, 2012-2016
// Surveillance of human hantavirus infections in metropolitan France, 2012-2016
Résumé
Les infections par les hantavirus chez l’homme font l’objet d’une surveillance en France, en particulier en métropole, depuis une trentaine d’années. Cette surveillance associait sur la période 2012-2016 un réseau d’une quinzaine de laboratoires de biologie médicale, le Centre national de référence (CNR) des Hantavirus et Santé publique France. Les données de surveillance ont été obtenues par l’analyse des fiches de renseignements accompagnant les échantillons des cas diagnostiqués par les laboratoires du réseau et confirmés par le CNR.
La situation observée était proche de celles rapportées pour les périodes précédentes : une centaine de cas, la plupart hospitalisés, était dénombrée en moyenne annuellement (incidence de 0,15 cas pour 100 000 habitants) avec de fortes variations annuelles. La population active était toujours la plus touchée (médiane d’âge de 40 ans) et les hommes étaient les plus concernés (75% des cas). Les cas étaient détectés toute l’année, avec des pics de détection à la fin du printemps ou à l’automne. La majorité des cas étaient dus au virus Puumala, mais le fait marquant sur la période était la détection de cas d’infection par les virus Seoul et Tula et la nature des expositions à ces virus. La distribution géographique des cas, concentrée sur le quart nord-est de la France, a connu une extension très limitée dans sa périphérie. Cependant, cette incidence et cette distribution géographique pourraient être sous-estimées du fait de l’utilisation de tests de diagnostic sérologique trop spécifiques et de la faible demande de diagnostic pour des patients non hospitalisés ou en dehors de la zone d’endémie connue.
Abstract
Surveillance of human hantavirus infection has been carried out for about 30 years in mainland France. From 2012-2016, a network of 15 clinical laboratories, the National Reference Center (NRC) for Hantavirus and the French Public Health Agency (Santé publique France) were involved in the surveillance. Data were obtained from the analysis of the information sheet records of the hantavirus cases diagnosed by the laboratory network and confirmed by the NRC.
The global situation was similar as the ones observed in the previous periods: an average of about one hundred cases, mostly hospitalized, was reported annually (incidence of 0.15 case per 100,000 inhabitants) with high annual variations. Active people were more concerned (median age 40 years), and were mostly males (75% of the cases). Cases were detected all year round with peaks of detection at the end of spring and at fall. Most of the cases were due to Puumala virus, but interestingly Seoul and Tula viruses were also detected, underlying other high-risk behavior. The geographic distribution of the cases in the North-Eastern quarter of France had a limited peripheral extension. However, this incidence and this geographic distribution are probably under-estimated because of the use of too specific serological diagnostic tests, and the low request of laboratory tests outside the hantavirus endemic area or for outpatients.
Introduction
Les hantavirus, virus enveloppés à ARN simple brin de polarité négative (genre Orthohantavirus, famille des Hantaviridae) ont pour hôtes naturels des rongeurs, des musaraignes, des taupes et des chauves-souris. Certains des hantavirus associés aux rongeurs sont transmissibles à l’homme. La transmission du virus s’effectue essentiellement via l’inhalation d’excreta ou de sécrétions contaminés de rongeurs infectés. Ils provoquent alors deux types de syndromes : soit une fièvre hémorragique avec syndrome rénal (FHSR) plus ou moins sévère, causée principalement par des hantavirus européens et asiatiques, soit un syndrome cardiopulmonaire sévère, causé essentiellement par des hantavirus américains. Le traitement de ces maladies est symptomatique. Des vaccins contre certains virus sont disponibles seulement dans quelques pays asiatiques. La prévention de l’infection consiste essentiellement à limiter les contacts avec les rongeurs, leurs sécrétions et excrétions ou à contrôler les populations de rongeurs 1.
Quatre espèces d’hantavirus zoonotiques circulent sur le continent européen : le virus Puumala (PUUV), le virus Seoul (SEOV), le virus Dobrava-Belgrade (DOBV) et le virus Tula (TULV). Ces quatre virus sont responsables d’une FHSR. PUUV, virus responsable du plus grand nombre de cas avec une létalité très faible, circule en Europe du Nord et de l’Ouest. DOBV circule dans la région des Balkans et l’Europe centrale et il peut être à l’origine d’atteintes humaines graves (taux de létalité pouvant atteindre 10%). Les cas d’infection par SEOV ont une distribution géographique mondiale, en lien avec celle de son réservoir principal, le rat brun (Rattus norvegicus), mais ces cas sont très sporadiques. Les infections par TULV sont exceptionnelles et mal connues 1.
Les infections par hantavirus sont associées en France métropolitaine au quart nord-est du pays, où les premiers cas ont été historiquement détectés dans les années 1980. Les principales zones d’endémie sont le nord des Ardennes, l’Avesnois, le centre de l’Aisne, le sud de l’Oise et le massif du Jura. Ces infections sont généralement attribuées par usage à PUUV, dont le réservoir est le campagnol roussâtre (Myodes glareolus), une espèce forestière de rongeurs. On dénombre, sur la période 2003-2011, une centaine de cas en moyenne détectés annuellement avec des années épidémiques (≥ 20%) ou inter-épidémiques (≤ 20%), un pic saisonnier étant généralement observé à la fin du printemps mais également à l’automne, le tout en rapport avec la dynamique des populations des rongeurs sous l’influence importante des conditions environnementales. La population active (âge médian des cas de 40 ans), plutôt masculine (sexe-ratio H/F de 3,6), est la plus touchée, ce qui est en lien avec la nature des expositions aux déjections de rongeurs forestiers infectés 2,3.
Dans le cadre du suivi de la situation des infections par les hantavirus chez l’homme en France métropolitaine, nous présentons ici les données de surveillance du Centre national de référence (CNR) des Hantavirus pour la période 2012-2016.
Système de surveillance
En France métropolitaine, la surveillance des infections par les hantavirus est réalisée par le CNR des Hantavirus en lien avec Santé publique France et les laboratoires qui effectuent le diagnostic de première intention d’une infection par hantavirus. Ces laboratoires de biologie médicale spécialisée ou hospitaliers (au nombre de 15 fin 2016), utilisent des tests commerciaux sérologiques permettant la détection des anticorps de type IgM ou/et IgG dirigés contre un ou plusieurs hantavirus, anticorps apparaissant très rapidement après le début de la maladie (tableau 1). Certaines des trousses utilisées ne permettent pas la détection de tous les hantavirus zoonotiques circulant en Europe. Ces laboratoires se trouvent pour la plupart dans le quart nord-est de la France, zone d’endémie de l’infection humaine par PUUV, mais les laboratoires reçoivent des prélèvements de tout l’hexagone et au-delà. Les coûts de ces actes ne sont pas remboursés par l’Assurance maladie.
 Agrandir l'image
Agrandir l'imageCes laboratoires adressent au CNR, à des fins de confirmation et de surveillance, des prélèvements de sérum ou plasma présentant un résultat positif, mais également ceux avec un résultat limite ou négatif peu compatible avec la présentation clinique. Le CNR contribue également à ce diagnostic de première intention en recevant des prélèvements directement de centres hospitaliers.
Le CNR effectue sur tous ces prélèvements une recherche d’IgM et d’IgG anti-hantavirus par test Elisa et d’immunoglobulines anti-hantavirus par immunofluorescence (IF) avec des antigènes natifs de PUUV, DOBV, SEOV et/ou Sin Nombre (SNV), le choix des antigènes testés dépendant du lieu d’exposition des patients (en cas de défaut de renseignement, seuls les antigènes PUUV et SEOV sont testés). Ces antigènes, du fait des réactions sérologiques croisées, permettent de détecter une infection par un des hantavirus zoonotiques. Le CNR recherche également l’ARN de PUUV ou d’hantavirus (par RT-PCR temps réel et RT-PCR Nichée respectivement), en complément de diagnostic et dans le cadre de la surveillance. Les prélèvements privilégiés pour cette recherche d’ARN sont ceux effectués dans les 10 premiers jours de la maladie, soit contenant des IgM dirigées contre les hantavirus, soit présentant un intérêt diagnostique (discordance entre les résultats de sérologie du CNR et ceux des laboratoires de première intention), clinique (forme grave) et/ou épidémiologique (lieu d’exposition). La plupart de ces prélèvements sont reçus après conservation pendant plusieurs jours à des températures non conformes pour des tests moléculaires (demande initiale pour diagnostic sérologique). Une feuille de renseignements cliniques, biologiques et épidémiologiques accompagne le prélèvement, permettant le choix de ces antigènes et l’interprétation des résultats, ainsi qu’à des fins de surveillance. Le type d’habitat (rural, maison isolée), la profession et les activités récentes donnant lieu à une exposition ainsi que la commune d’exposition rapportées par le patient y sont en particulier précisées 4.
Un patient sera classé comme cas confirmé d’infection récente par un hantavirus (CCIRH) si, dans un prélèvement isolé, les IgM et les IgG anti-hantavirus sont présentes, et/ou si l’ARN d’un hantavirus est détecté ou si, dans un deuxième prélèvement, l’apparition des IgG et/ou IgM anti-hantavirus est constatée.
Résultats
Demandes de diagnostic
Moins de 2 000 patients ont été prélevés annuellement sur la période 2012-2016, les demandes de diagnostic étant plus faibles lors des années inter-épidémiques 2013 et 2016, identifiées par un faible nombre de CCIRH (tableau 2). Il existe surtout une forte disparité dans l’origine géographique des demandes, celles-ci provenant pour plus de 80% du quart nord-est de la France, zone d’endémie définie par la présence de CCIRH sur la période 2003-2016.
2012-2016
 Agrandir l'image
Agrandir l'imageLe volume d’activité du CNR a suivi cette dynamique, avec un nombre plus faible d’échantillons reçus pendant les périodes inter-épidémiques mais aussi un pourcentage de confirmation plus élevé en période épidémique. Les feuilles de renseignements ont été reçues spontanément pour plus de la moitié des cas et après relance téléphonique pour le reste. La plupart des patients concernés étaient des patients hospitalisés (tableau 3).
 Agrandir l'image
Agrandir l'imageCas confirmés d’infection récente
Un total de 470 CCIRH a été détecté pour la période 2012-2016 (tableau 2). Ce nombre exclut du reste de l’analyse 7 patients prélevés en 2011, 4 résidant et exposés à l’étranger, ainsi que 4 résidant en France et exposés à l’étranger (Finlande, Belgique et Luxembourg). Les trois quarts des 470 patients (n=355) étaient des hommes. Leur âge médian était de 39,5 ans et celui des femmes de 42 ans. Onze mineurs (2,3%) étaient concernés. La moyenne d’une centaine de cas détectés annuellement sur la période de référence 2003-2011 a été largement dépassée en 2012 (+64%) et 2015 (+32%). Le nombre de détections a été bien en deçà de cette moyenne en 2013 (-86%) et 2016 (-44%). Le pic saisonnier classique de fin du printemps a été observé pour les années épidémiques. Il était décalé à l’été pour les autres années. Le pic d’automne a été observé de manière plus ou moins intense chaque année (figure 1).
 Agrandir l'image
Agrandir l'imageLes techniques de diagnostic moléculaire ont permis d’identifier l’espèce d’hantavirus en cause chez 234 des 470 patients. Comme attendu, PUUV a été détecté dans la grande majorité des cas (n=228) mais, de manière plus surprenante, TULV a été détecté chez 1 patient et SEOV chez 5. Un cas d’infection récente a également été attribué sérologiquement à SEOV, avec confirmation d’une exposition à des rats bruns infectés par SEOV.
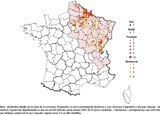
La distribution géographique des 470 cas selon les départements est présentée figure 2. Les données se fondent 1/ sur la commune d’exposition (n=318) puis, si elle n’est pas indiquée, 2/ sur la commune de résidence du patient (n=147) et, si les deux sont inconnues, 3/ sur la commune du lieu de prélèvement (n=5). Au cours de la période, on observe une extension de la zone d’endémie de PUUV, certes limitée, avec la détection d’un cas confirmé d’infection par PUUV dans le Loiret et d’un autre en Isère. Les cas d’infection par SEOV et TULV ont été détectés également dans cette zone d’endémie. Les traditionnels départements d’endémie les plus touchés sont retrouvés (Ardennes et Avesnois, Aisne, Nord, Franche-Comté et Oise) (figure 2, tableau 4). Les patients sont globalement des personnes résidant en zone d’endémie. La commune d’exposition et celle de résidence sont disponibles à la fois pour 301 des 470 cas : 280 (93,0%) résidaient dans le département où ils ont été exposés, 19 (6,3%) dans un département différent de celui de l’exposition (mais les deux sont en zone d’endémie) et 2 (0,7%), exposés dans la zone d’endémie, résidaient en dehors de cette zone. Des cas groupés (au plus 3) dans l’espace (même commune) et le temps (même mois) ont été observés dans les départements de l’Aisne, des Ardennes et du Bas-Rhin.
 Agrandir l'image
Agrandir l'image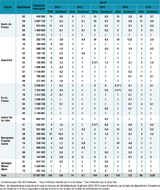 Agrandir l'image
Agrandir l'imageDiscussion – conclusion
Plusieurs éléments de l’endémie à hantavirus sont restés inchangés au cours de ces cinq dernières années. La population active est toujours la plus touchée, et en particulier les hommes. Les périodes épidémiques restent séparées par une année inter-épidémique, en lien avec la dynamique des populations de rongeurs. Les pics de détection des cas se situent toujours globalement à la fin du printemps et à la fin de l’automne. Une centaine de cas sont dénombrés en moyenne annuellement (incidence de 0,34% pour la zone d’endémie). Néanmoins, cette incidence est sans doute sous-estimée. Il s’agit, pour la très grande majorité des cas, de patients hospitalisés. Étant donné leur coût, non pris en charge par l’Assurance maladie, les examens biologiques sont très peu demandés pour des patients non hospitalisés et la maladie reste sous-diagnostiquée, au moins dans sa forme bénigne pour laquelle nous n’avons aucune idée de son incidence.
La distribution géographique des cas est légèrement modifiée, avec une extension dans la périphérie de la zone d’endémie et qui reste très limitée 5. L’absence de détection de cas en dehors du nord-est de la France reste une énigme. Néanmoins, il existe un biais dans l’origine géographique des demandes d’examens : en effet, plus de 80% des demandes proviennent de la zone d’endémie. La maladie resterait alors méconnue ou son diagnostic de laboratoire ne serait pas évoqué en dehors de cette zone, car elle est réputée pour ne pas y sévir. Un parallèle peut être fait avec la leptospirose, maladie proche cliniquement et qui partage un même réservoir (le rat brun Rattus norvegicus) avec l’infection par SEOV. Les demandes d’examens pour la leptospirose sont beaucoup plus nombreuses et mieux réparties sur l’ensemble de la France métropolitaine. Il en est de même pour les cas de leptospirose détectés. Ainsi, à titre d’exemple, deux laboratoires de biologie médicale spécialisée traitant les deux tiers des demandes ont examiné les prélèvements de 7 490 patients en 2015 et 8 097 en 2016, dont 38,4% et 35,6% dans la zone d’endémie de PUUV (représentant environ un tiers du territoire et de la population) ; un total de 509 et 644 cas de leptospirose ont été détectés en 2015 et 2016 par ces deux laboratoires, dont 38,5% et 34,5% dans la zone d’endémie de PUUV (données Santé publique France). La sous-demande de diagnostic d’hantaviroses pourrait expliquer la distribution géographique de cas observée et contribuer aussi à la sous-estimation de l’incidence de la maladie. Le diagnostic de laboratoire d’une hantavirose devrait être plus souvent évoqué quand une leptospirose non ictérique est suspectée. D’autre part, il faut garder à l’esprit que même si le réservoir de PUUV, le campagnol roussâtre, est présent partout sur le territoire métropolitain excepté le littoral méditerranéen, on ne sait toujours pas s’il existe des populations de rongeurs infectées éloignées de la zone d’endémie. L’absence de détection de cas humains d’infection par ce virus en dehors de cette zone (quand ils sont recherchés) pourrait s’expliquer par l’absence d’infection des rongeurs. Il a cependant été montré récemment que des rongeurs infectés par PUUV pouvaient être trouvés en périphérie de la zone d’endémie 6. Aucun cas humain n’a été détecté dans cette région (Est du Loiret), mais il faut souligner qu’aucune demande n’a concerné cette région pendant la période 2012-2016.
D’autres raisons pourraient expliquer l’absence de cas humains en présence de rongeurs infectés : exposition humaine limitée, excrétion virale des rongeurs faible, conditions environnementales défavorables aux pullulations de rongeurs et à la survie du virus dans le milieu extérieur, etc. Autant d’axes de recherches à développer.
Un fait marquant de la période reste l’identification des hantavirus responsables de ces infections. La grande majorité des cas sont dus, comme attendu, à PUUV. Néanmoins, il faut souligner la mise en évidence de cas humains d’infection par SEOV et TULV. Il s’agit des premiers cas d’infection par SEOV confirmés virologiquement en Europe (même si d’autres cas avaient été confirmés sérologiquement auparavant en Europe et en France en particulier). Quatre de ces cinq cas ainsi qu’un autre cas confirmé seulement par sérologie ont été détaillés par ailleurs 7,8,9. L’étude de ces cas a permis de souligner le rôle des rats bruns (Rattus norvegicus) domestiques dans la transmission de SEOV, la méconnaissance des propriétaires sur les risques zoonotiques associés à la manipulation de ces rats et l’absence de suivi sanitaire des rats commercialisés, hors animaux de laboratoire 9. Le cas d’infection par TULV est le premier rapporté chez un patient immunocompétent, ce qui met fortement en question sa non pathogénicité pour l’homme. L’exploration de ce cas a montré également que le risque d’infection par un hantavirus ne se limitait pas à la fréquentation du milieu forestier ou péri-forestier, le campagnol des champs (Microtus arvalis) étant le principal hôte de ce virus 10. L’incidence des infections par ces deux virus est très faible et les cas restent détectés dans la zone d’endémie. Néanmoins, la maladie due à ces virus est sans doute sous-diagnostiquée en dehors de la zone d’endémie en raison de la faible demande d’examens ainsi que les capacités techniques des laboratoires à identifier ces hantavirus. En effet, dans la zone d’endémie, le test rapide permettant la détection des IgM dirigées contre PUUV utilisé par certains laboratoires ne permet pas de détecter des infections par SEOV 9. Dans le cas de forte suspicion d’infection par ce dernier (contexte d’exposition semblable à celui de la leptospirose), il faut privilégier l’usage de tests permettant de le détecter.
Un autre hantavirus a été décrit en France métropolitaine. Il s’agit du virus Nova, associé à la taupe européenne (Talpa europaea). Ce virus, décrit dans d’autres pays européens, n’a pas encore été retrouvé chez l’homme 11. Nous ne l’avons pas détecté avec notre technique de détection moléculaire pan-hantavirus dans les échantillons testés de patients présentant pour la plupart une fièvre à syndrome rénal. Un autre type de syndrome pourrait être provoqué par ce virus, qui pourrait expliquer ce résultat négatif. Un des réservoirs de DOBV, le mulot à collier (Apodemus flavicollis) est présent en France. Cependant, aucune infection par ce virus n’a encore été retrouvée chez ce mulot sur le territoire et aucun cas humain autochtone n’a été détecté. De nouveaux hantavirus ont été décrits en Europe chez des espèces de rongeurs, musaraignes ou chauves-souris présentes en France : le virus Tatenale chez le campagnol agreste (Microtus agrestis) au Royaume-Uni, les virus Seewis, Asikkala et Boginia chez la musaraigne carrelet (Sorex araneus), la musaraigne pigmée (Sorex minutus) et la musaraigne aquatique (Neomys fodiens), le virus Brno chez la noctule commune (Nyctalus noctula) 12,13,14,15,16. Ces virus n’ont pas encore été détectés chez l’homme mais c’est un point de vigilance à souligner, en particulier en cas d’exposition patente à ces animaux. Enfin, les territoires français d’outre-mer sont au moins concernés par deux hantavirus : le virus Thailand à Mayotte, associé au rat noir ubiquiste Rattus rattus, dont la preuve de la pathogénicité n’est pas faite, et le virus Maripa en Guyane, associé à des espèces de rongeurs endémiques sud-américains et responsable chez l’homme d’un syndrome cardiopulmonaire sévère 17,18.
L’infection par un hantavirus chez l’homme en France métropolitaine peut provoquer des signes cliniques suffisamment graves pour conduire à l’hospitalisation du patient. Il est donc essentiel que le diagnostic d’hantavirose soit évoqué en cas d’activités à risque, même en dehors de la zone d’endémie, et que des mesures de prévention soient relayées, s’agissant essentiellement d’éviter les expositions aux rongeurs et à leurs déjections.
Remerciements
À Pierre Rollin (Viral Special Pathogens Branch, Centers for Disease Control and Prevention, Atlanta, États-Unis) pour la fourniture de certains réactifs utilisés par le CNR des Hantavirus. Le CNR des Hantavirus reçoit un support financier de Santé publique France.




