Bilan évolutif des RCP-hépatite C de 2015 à 2019 dans un centre de référence en Alsace
// Assessment of the evolution of hepatitis C specialist multidisciplinary coordination meeting from 2015 to 2019 in a reference center in Alsace, France
Résumé
Le but de cette étude a été d’analyser, en fonction de l’évolution des réunions de concertation pluridisciplinaire (RCP), les modifications des caractéristiques et de la prise en charge thérapeutique des patients ayant une mono-infection par le virus de l’hépatite C (VHC) traitée par les antiviraux à action directe, à l’échelon du territoire alsacien. Les modifications ont été étudiées au cours de cinq périodes successives entre janvier 2015 et décembre 2019 chez 1 753 patients. L’âge des patients et la proportion de ceux nés en France a diminué régulièrement (p<0,001). La fréquence de la contamination par usage de drogues a varié entre 27,43% et 41,66% (p<0,001). La fréquence de la fibrose avancée a chuté de 86,80% à 30,45% entre les deux premières périodes, avec un plateau inférieur à 40% durant les périodes suivantes (p<0,001). Parmi les structures de prise en charge, la part du Centre hospitalier universitaire (CHU) a été prédominante durant toutes les périodes, la part des centres hospitaliers généraux a diminué de moitié et le périmètre de prise en charge s’est élargi progressivement aux centres d’addictologie et aux réseaux de médecins généralistes (p<0,001). Au total, les caractéristiques et la prise en charge de l’hépatite C ont été modifiées entre 2015 et 2019 en fonction de l’évolution des RCP.
Abstract
The purpose of this study was to analyze changes in the characteristics and in the therapeutic care of patients with HCV mono-infection who were treated with direct-acting antivirals (DAAs) according to the evolution of Specialist Multidisciplinary Coordination Meeting (SMCM) in the Alsatian territory. The changes were studied over five successive periods between January 2015 and December 2019 in a sample of 1,753 patients. The age of patients and the proportion of those born in France decreased steadily (p<0.001). The frequency of contamination by drug use varied between 27.43% and 41.66% (p<0.001). The frequency of advanced fibrosis dropped from 86.80% to 30.45% between the first two periods with a plateau of less than 40% during the following periods (p<0.001). Among the patient care management center, the involvement of the University Hospital center was predominant during all the periods, the share of general hospitals has halved, and the scope of management was gradually extended to addictology centers and general practitioner networks (p<0.001). In total, the characteristics and management of hepatitis C were modified between 2015 and 2019 according to the evolution of SMCM.
Introduction
En France l’élimination du virus de l’hépatite C (VHC) à l’horizon 2025 figure parmi les mesures phares du Plan priorité prévention 2018-2022 qui s’inscrit dans le cadre de la Stratégie nationale de santé 1. L’Organisation mondiale de la santé (OMS) a également fixé cet objectif pour 2030 2.
Les réunions de concertation pluridisciplinaire (RCP) ont été instaurées en France en décembre 2014 au sein des services experts de lutte contre les hépatites virales avec l’arrivée des antiviraux à action directe (AAD) 3. Elles ont permis d’encadrer la prescription et la délivrance de ces nouveaux traitements et d’optimiser l’organisation du suivi des patients traités, en veillant à l’égalité de leur mise à disposition sur l’ensemble du territoire. Initialement, les AAD étaient prescrits par un médecin hospitalier hépato-gastro-entérologue, infectiologue ou interniste et étaient délivrés par une pharmacie à usage intérieur d’un établissement de santé. Les indications étaient restrictives et concernaient l’hépatite chronique C chez l’adulte, avec une fibrose avancée F3 ou F4 ou une fibrose F2 sévère (fonction de l’état clinique et de l’évolutivité de la fibrose), et l’hépatite chronique C associée à une infection VIH ou une cryoglobulinémie mixte systémique et symptomatique ou à un lymphome B, quel que soit le stade de fibrose 3.
Les décisions thérapeutiques émises par la RCP ont été évolutives par la suite jusqu’en 2019 en fonction des indications et des modalités de prescription et de délivrance des AAD. En juillet 2016, le traitement était élargi au stade F2 de fibrose 4. En août 2017, le traitement était étendu à tous les stades de fibrose et les RCP étaient limitées aux cas complexes avec fibrose avancée F3-F4 et/ou comorbidité 5. En mars 2018, les AAD pouvaient également être délivrés par les pharmacies d’officine 6. Enfin, en mai 2019, la prescription des AAD pangénotypiques devenait universelle avec la possibilité, en particulier pour le médecin généraliste, de les prescrire dans le cadre d’une prise en charge simplifiée de l’hépatite C, c’est-à-dire en l’absence de fibrose avancée, de co-infection VIH ou par le virus de l’hépatite B, d’insuffisance rénale sévère, de transplantation d’organe et de comorbidité mal contrôlée (consommation excessive d’alcool, diabète et obésité) 7. Le but de cette étude a été d’analyser rétrospectivement, à l’échelon du territoire alsacien, entre 2015 et 2019, les modifications des caractéristiques et de la prise en charge thérapeutique des patients ayant une hépatite chronique C en fonction de l’évolution des RCP.
Patients et méthodes
Tous les patients inclus dans cette étude étaient mono-infectés par le VHC. L’indication d’un traitement par les AAD a été retenue pour chaque patient durant une période de 8 à 24 semaines selon les schémas successifs recommandés par l’Association française pour l’étude du foie (AFEF) entre janvier 2015 et février 2019 8. Il s’agissait d’un primo-traitement ou d’un retraitement chez des patients ayant eu une résistance ou une rechute à un traitement à base d’interféron. La RCP était organisée à l’échelon du territoire alsacien par le Service expert de lutte contre les hépatites virales d’Alsace (Selhva) rattaché aux Hôpitaux universitaires de Strasbourg (HUS). Les fiches de synthèse établies à partir du dossier de chaque patient, selon le modèle de la lettre d’instruction de décembre 2014 3, ont permis l’exploitation des données en prenant garde au respect de la confidentialité des informations. Les fiches ont été adaptées en fonction de l’évolution des connaissances sur l’hépatite C et des schémas thérapeutiques 8,9. Les données concernant la réponse virologique soutenue, qui correspond à la guérison virologique, ont été exploitées postérieurement dans la mesure où cette réponse est évaluée 12 semaines après la fin du traitement (RVS 12). Le résultat de la PCR ARN-VHC a été communiqué au Selhva par le médecin spécialiste prescripteur ou par le médecin généraliste référent, en respectant la confidentialité des informations.
Les caractéristiques des patients ont été étudiées rétrospectivement entre janvier 2015 et décembre 2019 en distinguant cinq périodes successives en fonction de l’évolution des RCP : P1 de janvier 2015 à juin 2016, P2 de juillet 2016 à juillet 2017, P3 d’août 2017 à février 2018, P4 de mars 2018 à avril 2019 et P5 de mai 2019 à décembre 2019. Il s’agissait des variables suivantes : a) démographiques : âge, sexe et pays de naissance ; b) épidémiologiques : mode de contamination, les usagers de drogues correspondant à des personnes ayant injecté ou sniffé au moins une fois dans leur vie, selon les critères retenus dans l’enquête française ANRS-Coquelicot 10 et génotype viral ; c) cliniques et paracliniques : stade de fibrose évalué dans la majorité des cas par un FibroScan® avec, pour la fibrose avancée (stades F3-F4), une valeur d’élasticité ≥10 kP 8, carcinome hépatocellulaire surajouté à la cirrhose, antécédent de transplantation d’organe (foie et/ou rein), cryoglobulinémie symptomatique, valeur de l’indice de masse corporelle IMC en kg/m2, comorbidités associées (obésité définie par un IMC ≥30 kg/m2, diabète de type 2, consommation d’alcool à risque, supérieure à 10 verres standard déclarés/semaine sans dépasser 2 verres standard/jour 11, et affection psychiatrique) ; d) mode de vie : pour l’alcool, absence de consommation ou consommation occasionnelle, consommation régulière déclarée inférieure ou supérieure à 10 verres standard/semaine, consommation journalière de tabac et de cannabis sans précision du nombre de cigarettes ou de joints.
Les modalités de prise en charge thérapeutique des patients ont également été étudiées rétrospectivement en fonction des cinq périodes. Les structures de prise en charge étaient : le centre hospitalo-universitaire de Strasbourg (HUS), avec le service d’hépato-gastroentérologie en lien avec le Selhva, le pôle de médecine interne, la Permanence d’accès aux soins de santé et l’Unité sanitaire de niveau 1, les centres hospitaliers généraux (CHG) de Mulhouse, Colmar, Sélestat, Saverne et Haguenau, les centres de prévention ou de soin en addictologie et réseaux de santé de médecine générale orientés vers les addictions ou la précarité, avec en particulier le réseau des microstructures médicales. Il s’agissait également de l’éducation thérapeutique du patient (ETP), accessible uniquement aux patients des HUS avec un programme coordonné par une infirmière entourée d’une équipe pluridisciplinaire (comprenant notamment un médecin psychiatre-addictologue et une assistante sociale) et l’aide d’une association de patients (SOS Hépatites Alsace-Lorraine) ; du primo-traitement ou du retraitement par les AAD après échec d’un traitement à base d’interféron ; du type d’AAD pangénotypiques ou non ; du traitement de substitution aux opiacés (TSO) pour les usagers de drogues et des interactions médicamenteuses avec les AAD. Enfin, la RVS 12 a été évaluée selon les modalités décrites ci-dessus.
L’ensemble des fiches de synthèse, conservées sur le serveur des HUS, ont été rassemblées par le Selhva dans un tableau Excel et anonymisées pour l’analyse statistique. Un avis favorable du Comité d’éthique de la Faculté de médecine de Strasbourg a été obtenu le 17 décembre 2020 (CE-2020-171). Le traitement des données a été enregistré sur le registre des HUS le 22 janvier 2021 (fiche de registre réf 21-009).
L’analyse statistique a été confiée au groupe Méthode en recherche clinique du pôle de santé publique au travail des HUS. Le logiciel utilisé a été R Studio. Les variables catégorielles/binaires ont été exprimées en fréquence avec un intervalle de confiance à 95% (IC95%) et les variables continues en médiane [IQR]. Les tests de comparaison entre les différentes périodes d’étude ont été le test du Chi2 pour les variables catégorielles/binaires et le test de Kruskal-Wallis pour les variables continues.
Résultats
La répartition des 1 753 patients inclus dans l’étude en fonction des cinq périodes est indiquée sur la figure 1. Le nombre de patients variait entre 729 pour la période P2 (41,6%) et 84 pour la période P5 (4,8%).
 Agrandir l'image
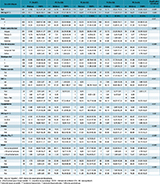
Agrandir l'imageLes caractéristiques de l’hépatite C en fonction des cinq périodes sont figurées dans le (tableau 1). L’âge médian a diminué régulièrement, de 57 ans durant P1 à 51,7 ans durant P5 (p<0,001). La proportion d’hommes a varié entre 55,91% et 72,61% (p<0,01). La proportion des patients nés en France a diminué régulièrement de 87,85% à 69,04% entre P1 et P5 (p<0,001). À l’inverse, la proportion des patients originaires des pays d’Europe de l’Est a augmenté régulièrement, de 10,79% durant P1 à 27,38% durant P5 (p<0,001). La fréquence de la contamination par usage de drogues a été fluctuante, entre 27,43% durant P2 et 41,66% durant P5, alors que la fréquence de la contamination nosocomiale/transfusion sanguine a diminué de 19,79% à 3,57% entre P1 et P5. La fréquence du mode inconnu de contamination a toujours été supérieure à 50%, sauf durant P1 (p<0,001). La répartition des génotypes n’a pas varié de façon significative au cours du temps, le génotype 1 étant toujours prédominant. La fréquence de la fibrose avancée a chuté de 86,80% durant P1 à 30,45% durant P2, avec un plateau inférieur à 40% durant les périodes ultérieures (p<0,001) (figure 2). La fréquence du carcinome hépatocellulaire a diminué de 3,59% à 0% entre P1 et P3, puis a augmenté jusqu’à 7,84% durant P4 (p<0,01). La proportion des patients transplantés du foie et/ou du rein a fluctué au cours du temps, avec une fréquence totale toujours inférieure à 6% (p=0,02). La fréquence de la cryoglobulinémie symptomatique a d’abord diminué de 10,68% à 5,83% entre P1 et P3, puis est remontée jusqu’à 9,52% durant P5 (p<0,01). La valeur médiane de l’IMC a varié entre 23,92 et 25,10 kg/m2 (p=0,001). La fréquence de l’obésité a diminué de moitié entre P1 et P3 pour remonter à son niveau initial durant P5 (p=0,02). La fréquence du diabète a chuté de 17,24% à 9,05% entre P1 et P2 pour remonter aux environs de 12% durant les périodes ultérieures (p<0,001). La proportion de consommateurs excessifs d’alcool a varié entre 4,57% durant P4 et 16,66% durant P3 (p<0,001). La fréquence d’une comorbidité psychiatrique a été relativement stable aux environs de 15% durant les trois premières périodes, a diminué à 11,11%% durant P4 puis est remontée à 20,23% durant P5 (p<0,001). La fréquence de la consommation de tabac et de cannabis a augmenté régulièrement au cours du temps (p<0,001).
 Agrandir l'image
Agrandir l'imageau cours des cinq périodes successives de RCP. Alsace, janvier 2015-décembre 2019 (voir détails tableau 1)
 Agrandir l'image
Agrandir l'imageLes modalités de la prise en charge thérapeutique des patients en fonction des cinq périodes sont figurées dans le tableau 2. Parmi les structures de prise en charge, la part du CHU a été prédominante durant toutes les périodes, variant entre 40,83% et 54,76%, alors que la part des CHG a diminué de moitié entre P1 et P5 (figure 3). La part des centres d’addictologie a augmenté, de 1,35% durant P1 à 16,34% durant P4, et celle des réseaux de médecine générale a été maximale durant P3 atteignant 24,17% (p<0,001) (figure 3). Le recours à l’ETP a diminué régulièrement, de 49,30% durant P1 à 6,52% durant P5 (p<0,001). La fréquence d’un primo-traitement a augmenté de 54,12% durant P1 à 74,07% durant P2 avant de diminuer jusqu’à 60,71% durant P5 (p<0,001). La fréquence du traitement par les AAD pangénotypiques a augmenté de 10,83% à 96,43% de P2 à P5 (p<0,001). La fréquence des interactions médicamenteuses avec les AAD a diminué de 16,34% durant P1 à 7,50% durant P3 pour revenir à son niveau initial durant P5 (p=0,001). La fréquence du TSO a augmenté de 42,63% à 69,05% entre P1 et P3, puis est descendue jusqu’à 57,14% durant P5 (p<0,001). Le taux de RVS 12 est proche de 94% au cours des différentes périodes.
en fonction des cinq périodes successives de RCP. Alsace, janvier 2015-décembre 2019
 Agrandir l'image
Agrandir l'image Agrandir l'image
Agrandir l'imageDiscussion
Cette étude met en évidence, entre 2015 et 2019, d’une part une nette diminution du nombre de dossiers soumis en RCP et, d’autre part, des variations significatives des caractéristiques et des modalités de prise en charge thérapeutique de l’hépatite C, à l’exception du génotype et de la RVS 12.
Le nombre de dossiers soumis en RCP a diminué d’un facteur 8 entre 2015 et 2019. La soumission a été maximale durant la seconde période de l’étude, entre juillet 2016 et juillet 2017, avec l’extension du traitement par les AAD au stade F2 de fibrose. Une réduction a été observée ultérieurement avec la limitation des RCP aux cas complexes, même si le traitement a été étendu à tous les stades de fibrose. Dans notre expérience, le tiers des cas complexes relevaient d’une fibrose avancée F3-F4. Les autres cas regroupaient principalement les comorbidités mal contrôlées, les affections psychiatriques, en particulier chez les usagers de drogues, et les hépatites C chez les personnes migrantes en situation de précarité. La proportion des patients n’ayant pas nécessité de RCP n’a pas été évaluée dans notre étude et le nombre de patients ayant bénéficié d’une prise en charge simplifiée de l’hépatite C à partir de mai 2019 est inconnu. De ce fait, les RCP ne reflètent plus du tout l’épidémiologie des patients traités pour une hépatite C.
Parmi les caractéristiques de l’hépatite C, le stade de fibrose a été un facteur déterminant dans l’évolution des RCP en France 3,4,5,7,8,12. Dans cette étude, la fibrose a été évaluée par le FibroScan® dans la majorité des cas, en l’absence de signes de cirrhose. Cette technique était accessible au CHU et dans deux CHG avec des appareils fixes, et dans les autres centres hospitaliers généraux et la plupart des centres d’addictologie dans le cadre d’un programme de recherche clinique avec des appareils mobiles mutualisés. L’objectif principal du FibroScan® était d’individualiser les stades avancés de fibrose, sans distinction entre les stades F3 et F4 8. Durant P1, une priorité a été accordée aux formes les plus sévères d’hépatite chronique C avec une fibrose avancée dans plus de 80% des cas 3. L’âge des patients, qui constitue un paramètre connu de progression de la fibrose hépatique, était également le plus élevé 13,14. L’âge plus élevé peut également être lié à l’ancienneté de l’infection virale C, les patients ayant une fibrose avancée, notamment une cirrhose, étant souvent plus âgés que les patients avec moindre fibrose. L’ouverture des RCP au stade F2 de fibrose peut expliquer la diminution de fréquence aux environs de 30% des stades avancés de fibrose durant P2 4. L’intensité de la diminution est probablement liée à l’importance du réservoir de patients en attente des nouveaux traitements, qu’il s’agisse d’un primo-traitement ou d’un retraitement. Par la suite, la fréquence de la fibrose avancée a été relativement stationnaire dans la mesure où les RCP étaient limitées aux cas complexes d’hépatite chronique C, avec notamment ce critère 5,7,8. Parmi les comorbidités, les cinétiques d’évolution de l’obésité et du diabète ont été semblables, avec une diminution de fréquence durant les premières périodes contemporaine de celle de la fibrose avancée, évoquant une relation possible. En effet, l’obésité et le diabète sont connus pour favoriser la progression de la fibrose 12. Ultérieurement, la fréquence de ces deux comorbidités a augmenté dans la mesure où les RCP étaient limitées aux cas complexes d’hépatite chronique C, avec notamment une comorbidité mal contrôlée 5,7,8. L’interprétation de l’évolution de la consommation d’alcool, y compris excessive, est limitée par le caractère déclaratif de cette dernière 15. La cinétique d’évolution d’une comorbidité psychiatrique est voisine de celle observée pour les usagers de drogues, suggérant une possible corrélation entre ces deux facteurs. Les fréquences les plus élevées (10%) de la cryoglobulinémie symptomatique ont été observées au début et à la fin de l’étude. Au début, elle constituait une indication de traitement par les AAD, indépendamment du stade de fibrose 3 et à la fin, elle s’intégrait dans les formes complexes d’hépatite C 8. La fréquence plus élevée du carcinome hépatocellulaire durant les dernières périodes de l’étude correspond également à la sélection des formes complexes. Même si les variations de fréquence étaient significatives au cours du temps pour les antécédents de transplantation hépatique et/ou rénale, la proportion des patients est restée très faible avec une valeur toujours inférieure à 6%.
Dans le cadre des RCP la prise en charge thérapeutique de l’hépatite C a d’abord été hospitalière, car elle concernait les formes les plus graves de la maladie, en attente de nouveaux traitements. La place du CHU a été prépondérante durant les cinq périodes de l’étude, son rôle de centre de référence étant renforcé par la présence du Selhva et la possibilité de recourir à l’ETP dans le cadre d’une autorisation par l’Agence régionale de santé 16. Par la suite, le périmètre de prise en charge s’est élargi aux centres d’addictologie et aux réseaux de médecine générale orientés vers les addictions et la précarité. Cette extension a coïncidé avec l’accès au traitement pour tous les stades de fibrose 5 et avec l’ouverture de la délivrance des AAD aux pharmacies d’officine 6. Les usagers de drogues ayant une fibrose avancée et/ou une comorbidité ont alors accédé plus facilement au traitement antiviral, d’autant plus qu’ils étaient substitués, le TSO étant également délivré en pharmacie d’officine 17. Cependant, la part des centres d’addictologie et des réseaux de médecine générale dans la prise en charge de l’hépatite C est ici sous-estimée car elle ne tient pas compte du parcours simplifié de soin 7,8. Ce dernier permet au médecin addictologue ou au médecin généraliste, quel que soit son mode d’exercice, de prendre en charge les cas simples d’hépatite C et de prescrire les AAD pangénotypiques, sans nécessité d’un passage en RCP. La diminution de la part des CHG dans la prise en charge de l’hépatite C à partir de P3 peut être liée à une appropriation de la prescription des AAD par les médecins de ces centres dès lors qu’ils n’avaient plus l’obligation de passer par la RCP du CHU. La fréquence du recours à l’ETP a diminué au cours du temps en raison de la simplification des schémas thérapeutiques et de la bonne tolérance des AAD par rapport à l’interféron 12. Le raccourcissement de la durée du traitement à 8 ou 12 semaines avec les AAD pangénotypiques a également contribué à cette diminution 6. Néanmoins, le recours à l’ETP était restreint au CHU. De plus, durant P5, le recours à l’ETP a été limité aux patients les plus vulnérables en raison d’une diminution des ressources en personnel pour cette activité.
Les autres variations paraissent indépendantes de l’évolution des RCP. La répartition selon le sexe fait apparaitre une prédominance masculine durant les cinq périodes d’étude. Durant la période P2, la proportion des femmes était la plus élevée (44,1%). Cette augmentation pourrait être liée à l’ouverture des AAD au stade F2 de fibrose, dans la mesure où le sexe masculin est un facteur indépendant reconnu de progression de la fibrose 13,14. Cette augmentation pourrait également expliquer la plus faible proportion d’usagers de drogues durant P2. Les autres variations significatives concernaient la répartition selon le pays d’origine avec, pour les usagers de drogues et les migrants, un accès au traitement souvent difficile en raison du délai d’obtention des droits sociaux 18, les consommations de tabac et de cannabis, dont l’évaluation n’a été que qualitative avec une proportion importante de données manquantes durant les deux premières périodes, et les interactions médicamenteuses avec les AAD, dont la fréquence dépend des pathologies associées à l’hépatite C 8,12.
Au total, la plupart des modifications des caractéristiques et de la prise en charge thérapeutique de l’hépatite C ont été consécutives à l’évolution des RCP entre 2015 et 2019. La fréquence des stades avancés de fibrose a diminué au cours du temps alors que la prise en charge thérapeutique par des centres de soins primaires a augmenté, même si la part du CHU avec le centre de référence est restée majoritaire. Au regard des objectifs du Plan priorité prévention 2018-2022 1, les RCP ont permis une prise en charge globale médico-psycho-sociale de l’hépatite C, particulièrement utile chez les personnes en situation de vulnérabilité sociale, contribuant ainsi à réduire les inégalités de santé. Elles ont contribué à renforcer la coopération entre la ville et l’hôpital. Elles ont permis d’optimiser la coordination et la qualité de la prise en charge de l’hépatite C en impliquant une équipe pluridisciplinaire, particulièrement utile en cas de comorbidité(s) associée(s). Enfin, elles ont permis aux services experts d’optimiser leur mission de formation auprès de l’ensemble des professionnels de santé et du secteur médico-social en favorisant les échanges, et leur mission de veille épidémiologique à l’échelon d’un territoire. Dans notre expérience, les réseaux de santé de médecine générale constituent le meilleur relais pour assurer le déploiement de la prise en charge simplifiée de l’hépatite C.
Remerciements
Les auteurs remercient les médecins des différentes structures de prise en charge ayant participé aux RCP, l’équipe de SOS Hépatites Alsace-Lorraine pour son aide logistique et les infirmières du Selhva (Anne-Élisabeth Bury et Carine Wiedemer) pour leur collaboration quotidienne.
Liens d’intérêt
Les auteurs déclarent ne pas avoir de liens d’intérêt au regard du contenu de l’article.
Références
publications/global-hepatitis-report2017/en/
files/u122/Lettre_d_instruction_hepatite_C_NAAD_29_dec_2014.pdf
themes/alcool-sante/definition-reperes-consommation
Citer cet article
publiquefrance.fr/beh/2021/9/2021_9_1.html




