Recommandations sanitaires pour les voyageurs, 2015
(à l’attention des professionnels de santé)
// Health recommendations for travellers, 2015 (for health professionals)
Avis du Haut Conseil de la santé publique du 24 avril 2015
Introduction à la pathologie du voyage
Les voyageurs, quelles que soient leur destination et les conditions du voyage, sont fréquemment victimes de problèmes de santé. Le taux de voyageurs malades varie de 15% à 70% selon les études, en fonction du type de voyageurs, des destinations et des conditions de séjour. La diarrhée est toujours le plus fréquent des problèmes de santé en voyage, avec les affections des voies aériennes supérieures, les dermatoses et la fièvre. Les études les plus récentes montrent aussi l’émergence de pathologies non infectieuses : mal d’altitude, mal des transports, traumatismes et blessures, d’origine accidentelle mais aussi intentionnelle.
Le risque de décès par mois de voyage a été estimé à 1 pour 100 000 (1 pour 10 000 pour les personnes impliquées dans des opérations humanitaires). Les causes de mortalité en voyage sont, dans la moitié des cas environ, cardiovasculaires. Les autres causes de décès, plus en rapport avec le voyage, se partagent entre accidents de la voie publique, noyades, homicides et suicides. Les infections ne rendent compte que de 1 à 3% des décès. Les causes de rapatriement sanitaire sont proches de celles de la mortalité en voyage : traumatiques (accidents, loisirs, agressions), vasculaires (cardiaques et neurologiques) et psychiatriques.
Si les étiologies infectieuses des décès ou des pathologies graves, imposant une évacuation sanitaire, sont peu fréquentes, c’est en grande partie parce que les recommandations qui suivent permettent de les éviter.
Les voyageurs ayant été hospitalisés au cours de leur voyage ou rapatriés sanitaires présentent un risque de portage de bactéries multirésistantes (BMR) qui doit faire l’objet d’un dépistage en cas d’hospitalisation dans une structure de soins.
Ces recommandations ont été élaborées par le Comité des maladies liées aux voyages et des maladies d’importation (CMVI) et approuvées par le Haut Conseil de la santé publique (HCSP) lors de la séance du 24 avril 2015 de la Commission spécialisée maladies transmissibles. Elles tiennent compte des données du Centre national de référence (CNR) du paludisme, du CNR des arboviroses, de l’Institut de veille sanitaire (InVS) et de l’Agence nationale de sécurité des médicaments et des produits de santé (ANSM), pour les vaccins et médicaments.
Les recommandations figurant dans ce document ne peuvent prendre en compte l’évolution des risques et l’émergence de nouvelles maladies infectieuses. Les recommandations aux voyageurs sont donc susceptibles d’être modifiées en fonction de l’évolution de la situation internationale. Pour être informé de ces mises à jour, il est conseillé de consulter un des sites suivants :
- http://www.sante.gouv.fr/
- http://www.invs.sante.fr/
- http://www.who.int/en/
- http://emergency.cdc.gov/
1. Vaccinations
Un grand nombre de maladies liées aux voyages peuvent être prévenues par une vaccination.
Le programme de vaccination à établir pour chaque voyageur doit tenir compte de :
- l’évaluation des risques réels encourus par le voyageur, qui varient en fonction :
- du contexte épidémiologique international ;
- de la situation sanitaire et du niveau d’hygiène de la zone visitée ;
- des conditions du séjour (saison, activités sur place, modalités d’hébergement et durée) ;
- des facteurs de risque individuels, notamment l’âge et les antécédents médicaux ;
- du statut vaccinal antérieur ;
- l’obligation administrative de présenter un certificat de vaccination pour entrer dans certains pays, soit dans le cadre du Règlement sanitaire international (vaccination contre la fièvre jaune), soit du fait d’une exigence particulière du pays d’accueil (vaccination contre les infections invasives à méningocoques pour les pèlerinages en Arabie Saoudite).
La mise à jour des vaccinations recommandées en France dans le calendrier vaccinal 1, que ce soit pour les adultes ou les enfants, est la première étape de ce programme, sachant que certaines des infections visées peuvent être endémiques dans le pays de destination. Cette mise à jour est particulièrement importante pour la vaccination contre la diphtérie, le tétanos, la poliomyélite (Cf. encadré ci-après) et la coqueluche, ainsi que pour la rougeole.
Poliomyélite
La vaccination antipoliomyélitique fait l’objet de recommandations particulières concernant 10 pays où une circulation active de virus polio sauvages est observée actuellement, à savoir : l’Afghanistan, le Cameroun, l’Ethiopie, la Guinée équatoriale, l’Irak, Israël, le Nigeria, le Pakistan, la Somalie et la Syrie 2,3.
Voyage d’une durée inférieure à 4 semaines dans l’un des 10 pays cités :
- Si vaccin polio seul ou combiné administré il y a moins de 1 an : rien à faire
- Si vaccin polio reçu il y a plus de 1 an et si vaccination contre diphtérie-tétanos à jour : administrer une dose de vaccin poliomyélitique inactivé injectable (Imovax Polio®)
- Si vaccin polio reçu il y a plus de 1 an et vaccination contre diphtérie-tétanos non à jour : administrer une dose de vaccin dTP, DTCP ou dTCP selon l’âge et les recommandations en vigueur
Voyage d’une durée supérieure à 4 semaines dans l’un des 10 pays cités :
Vérifier la date du retour :
- Si retour dans moins de 12 mois : administrer une dose de vaccin polio seul ou combiné (comme précédemment)
- Si retour dans plus de 12 mois : informer le voyageur de l’exigence possible par le pays d’accueil d’un rappel de vaccination antipoliomyélitique, à faire pendant le séjour (au maximum un an avant le retour).
Afin de faciliter la lecture, les vaccinations sont présentées par ordre alphabétique.
1.1 Choléra
Dans tous les cas, une prévention efficace est assurée par des règles d’hygiène simples appliquées à l’alimentation (Cf. chapitre 4 Diarrhée).
La vaccination anticholérique n’est recommandée que pour les personnels devant intervenir auprès de malades, en situation d’épidémie.
1.2 Encéphalite japonaise
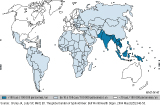
La vaccination contre l’encéphalite japonaise n’est pas recommandée systématiquement pour tous les voyageurs qui se rendent en Asie ou en Océanie 4 ;
Cette vaccination est recommandée avec le vaccin Ixiaro® pour les personnes âgées de 2 mois et plus, dans les circonstances suivantes :
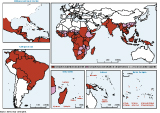
- séjour (quelle qu’en soit la durée) avec exposition importante en milieu extérieur (1), dans une région endémique (Carte 1), plus particulièrement dans les zones rurales (2) ;
- expatriation dans un pays situé dans la zone de circulation du virus (3) ;
- toute autre situation jugée à risque par le médecin vaccinateur.
Encéphalite japonaise – Schéma vaccinal
Adultes
- Deux injections de 0,5 ml à J0 et J28.
- Rappel 12-24 mois après la primo-vaccination, avant une réexposition éventuelle au virus de l’encéphalite japonaise.
- Les adultes à risque continu d’infection par le virus de l’encéphalite japonaise doivent recevoir une injection de rappel 12 mois après la primo-vaccination.
Enfants et adolescents âgés de 3 à 18 ans
- Deux injections de 0,5 ml à J0 et J28. Le rappel n’est pas recommandé pour les enfants âgés de moins de 18 ans.
Enfants âgés de 2 mois à 3 ans
- Deux injections de 0,25 ml (1/2 dose) à J0 et J28.
Le vaccin de l’encéphalite japonaise utilisé en France est produit à partir d’un virus inactivé.
NB. Une vaccination commencée avec Ixiaro® ne peut pas être poursuivie avec un vaccin différent : si le schéma vaccinal complet (primo-vaccination et rappel) ne peut pas être réalisé avant le départ, il convient donc de s’assurer de la disponibilité de ce vaccin (souche SA 14-14-2 inactivée) dans le pays de destination.
 Agrandir l’image
Agrandir l’image
1.3 Encéphalite à tiques
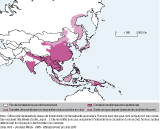
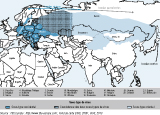
La vaccination contre l’encéphalite à tiques est recommandée pour les voyageurs devant séjourner en zone rurale ou boisée dans les régions d’endémie (Europe centrale, orientale et septentrionale, nord de l’Asie centrale, nord de la Chine, nord du Japon) du printemps à l’automne 5 (Carte 2).
Encéphalite à tiques – Schéma vaccinal
Deux vaccins, préparés à partir de deux souches différentes (Ticovac® et Encepur®), sont disponibles en France.
Schéma classique
- Ticovac® : trois injections à M0, entre M1 et M3, puis entre M5 et M12.
Il existe une présentation pédiatrique utilisable chez les enfants âgés de 1 à 15 ans révolus. - Encepur® (utilisable à partir de l’âge de 12 ans) : trois injections à M0, entre M1 et M3, puis entre M9 et M12.
Pour les deux vaccins, le 1er rappel est à faire 3 ans après la 3e dose, avant une réexposition éventuelle au virus de l’encéphalite à tiques.
Schéma accéléré
Si une immunisation rapide est nécessaire, deux schémas accélérés peuvent être utilisés, selon la spécialité :
- Ticovac® : deux injections à J0 et J14 (3e dose 5 à 12 mois après la 2e)
- Encepur® : trois injections à J0, J7 et J21 (auquel cas le 1er rappel doit être administré 12 à 18 mois après la primo-vaccination).
Les deux vaccins de l’encéphalite à tiques sont produits à partir d’un virus inactivé.
 Agrandir l’image
Agrandir l’image
1.4 Fièvre jaune
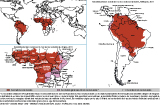
La vaccination contre la fièvre jaune est indispensable pour un séjour dans une zone endémique (régions intertropicales d’Afrique et d’Amérique du Sud (Carte 3), même en l’absence d’obligation administrative.
Cette vaccination est obligatoire pour les résidents du département de la Guyane.
Le vaccin de la fièvre jaune (ou vaccin amaril) est disponible uniquement dans les Centres de vaccination antiamarile désignés par les Agences régionales de santé 6.
 Agrandir l’image
Agrandir l’image
Cas particuliers
Enfants
La vaccination est recommandée à partir de l’âge de 9 mois pour les enfants se rendant dans une zone à risque. Exceptionnellement, elle peut être effectuée dès l’âge de 6 mois si le nourrisson doit séjourner en milieu rural ou en forêt ou si une épidémie sévit dans la région visitée.
Femmes enceintes
Comme il s’agit d’un vaccin vivant, la vaccination contre la fièvre jaune est en principe déconseillée chez une femme enceinte. Cependant, en raison de la gravité de la maladie, elle peut être réalisée quel que soit le stade de la grossesse, si le voyage dans une zone d’endémie amarile ne peut être différé.
Femmes allaitantes
En raison du passage dans le lait maternel du virus vaccinal pendant la virémie post-vaccinale, il paraît souhaitable d’attendre que le nourrisson ait atteint l’âge de 6 mois pour vacciner une mère qui allaite. Si la vaccination est impérative, notamment en cas de voyage ne pouvant être différé dans une zone à haut risque, l’allaitement doit être suspendu et peut être repris deux semaines après la vaccination.
Donneurs de sang
Le don de sang doit être suspendu pendant la phase de virémie post-vaccinale ; il peut être repris quatre semaines après l’administration du vaccin.
Personnes immunodéprimées
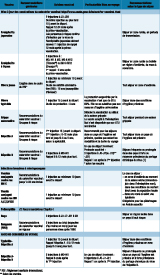
Le vaccin amaril est en principe contre-indiqué en cas de déficit immunitaire congénital ou acquis. Il peut toutefois être administré dans certaines circonstances (Tableau 1).
Dans les cas de thymectomie ou d’irradiation du thymus : si ces interventions étaient motivées par un dysfonctionnement du thymus, la contre-indication au vaccin amaril est définitive.
En revanche, les personnes dont le thymus a été irradié indirectement lors du traitement d’une autre maladie (en particulier cancer du sein), peuvent être vaccinées contre la fièvre jaune 7.
Chez les patients drépanocytaires traités par hydroxycarbamide (Hydrea®, Syklos®), le vaccin amaril n’est pas contre-indiqué.
Lorsqu’une autre vaccination avec un vaccin viral vivant est envisagée (en particulier rougeole), un délai minimum de 28 jours entre les deux vaccinations doit être respecté si celles-ci ne sont pas réalisées simultanément. Cependant, en cas de départ imminent en zone d’endémie amarile, les deux vaccins peuvent être administrés à n’importe quel intervalle.
Lorsque la vaccination ne peut pas être réalisée, les voyages en zone d’endémicité amarile sont formellement déconseillés.
Si nécessaire, un certificat de contre-indication à la vaccination anti amarile (4) peut être délivré par le médecin d’un Centre de vaccination antiamarile ou par le médecin traitant (5).
Fièvre jaune – Schéma vaccinal
Une injection au moins 10 jours avant le départ.
Durée de validité : 10 ans *.
Le vaccin amaril est produit à partir d’un virus vivant atténué.
D’exceptionnels effets indésirables graves du vaccin amaril ont été observés. Une information est accessible sur le site de la Société de médecine des voyages (feuille d’information Stamaril®) : http://www.medecine-voyages.fr/publications/ficheinfovaccinStamaril.pdf
* En juillet 2013, l’Organisation mondiale de la santé (OMS), suivant l’avis du Groupe stratégique consultatif d’experts sur la vaccination (SAGE), a déclaré qu’une dose unique de vaccin amaril était suffisante pour conférer une immunité protectrice pour toute la vie 8. Cependant, le Haut Conseil de la santé publique ne recommande pas pour le moment la suppression des rappels décennaux pour les personnes résidant en Guyane ou celles de la métropole qui doivent s’y rendre 9. Au-delà des divergences sur la question de l’utilité des rappels décennaux de vaccination contre la fièvre jaune, deux points sont à souligner :
- le Règlement sanitaire international (RSI) a été modifié en mai 2014, les pays ont jusqu’à juin 2016 pour la mise en œuvre ;
- chez les personnes ayant un facteur de moindre réponse à la vaccination au moment de leurs primo-vaccination (immunodépression modérée ne contre indiquant pas le vaccin amaril, femmes enceintes, enfants âgés de moins de 2 ans, personnes âgées de plus de 60 ans), la durée de protection conférée par le vaccin amaril ne peut pas pour le moment être considérée comme supérieure à 10 ans.
 Agrandir l’image
Agrandir l’image
1.5 Fièvre typhoïde
La vaccination contre la fièvre typhoïde est recommandée pour les voyageurs devant effectuer un séjour prolongé ou dans de mauvaises conditions dans des pays où l’hygiène est précaire et la maladie endémique, particulièrement dans le sous-continent indien (Carte 4).
Ce vaccin n’assurant qu’une protection de 50 à 65%, il ne se substitue pas aux mesures de précaution vis-à-vis de l’eau et des aliments, ni au lavage des mains.
Fièvre typhoïde – Schéma vaccinal
Le vaccin peut être administré à partir de l’âge de 2 ans.
Une injection, 15 jours avant le départ.
Durée de protection : 3 ans.
Les vaccins typhoïdiques disponibles en France sont composés d’un polyoside capsulaire de S. Typhi.
1.6 Grippe saisonnière
La vaccination contre la grippe saisonnière est recommandée 1 :
- pour toutes les personnes âgées de 65 ans et plus et pour tous les adultes, adolescents et enfants (à partir de l’âge de 6 mois) faisant l’objet de recommandations dans le calendrier vaccinal en vigueur, qui participent à un voyage, notamment en groupe ou en bateau de croisière ;
- pour le personnel navigant des bateaux de croisière et des avions, ainsi que pour le personnel de l’industrie des voyages (guides) accompagnant les groupes de voyageurs.
Le vaccin adapté à l’hémisphère sud n’est à ce jour disponible que sur autorisation temporaire d’utilisation (ATU) nominative.
Grippe – Schéma vaccinal
- Une injection, à renouveler chaque année.
- Pour les enfants âgés de 6 à 35 mois inclus : deux doses de 0,25 ml à 1 mois d’intervalle en primo-vaccination.
- Pour les enfants âgés de 3 à 9 ans inclus n’ayant pas été vaccinés auparavant : deux doses de 0,50 ml à 1 mois d’intervalle.
Le vaccin grippal disponible en France est produit à partir de virus inactivés.
1.7 Hépatite A
La vaccination est recommandée à partir de l’âge de 1 an 10 pour tous les voyageurs devant séjourner dans un pays où l’hygiène est précaire, quelles que soient les conditions du séjour. Elle est particulièrement recommandée chez les personnes souffrant d’une maladie chronique du foie ou de mucoviscidose.
Un examen sérologique préalable (recherche d’IgG) a un intérêt pour les personnes ayant des antécédents d’ictère, ayant passé leur enfance en zone d’endémie ou nées avant 1945.
Hépatite A – Schéma vaccinal
- Une injection, au moins 15 jours avant le départ.
- Un rappel 6 à 12 mois plus tard ; cette seconde dose peut être administrée jusqu’à 3 ans ou 5 ans après la première injection, selon la spécialité.
La durée de protection est d’au moins 10 ans.
Il existe deux vaccins pédiatriques, dosés à 80 U (Avaxim®) et 720 U (Havrix®), utilisables de 1 à 15 ans révolus.
Le vaccin de l’hépatite A est produit à partir d’un virus inactivé.
1.8 Hépatite B
Cette vaccination est recommandée pour des séjours fréquents ou prolongés dans les pays à forte ou moyenne prévalence du portage chronique du virus 1.
La recherche d’une infection occulte par le virus de l’hépatite B devrait être proposée avant la vaccination chez les personnes appartenant à des groupes à risque d’hépatite B : personnes originaires de pays où la prévalence de l’Ag HBs est supérieure à 2%, comportements sexuels à risque, entourage familial de porteurs de l’Ag HBs, usagers de drogue intraveineuse 11.
Le vaccin de l’hépatite B peut être administré dès la naissance en cas de séjour prévu dans un pays de forte ou de moyenne endémie.
Hépatite B – Schéma vaccinal
Deux injections espacées d’1 mois et une 3e injection 6 mois après la première.
Cas particulier (Voir Tableaux 3 et 4)
Chez l’adulte, si une immunisation rapide est nécessaire, un schéma adapté incluant trois injections rapprochées sur 21 jours (J0-J7-J21 avec EngerixB20®, J0-J10-J21 avec GenhevacB Pasteur®) et une 4e injection 1 an plus tard doit être proposée.
Ce schéma accéléré n’est pas applicable chez l’enfant.
Le vaccin de l’hépatite B est composé de l’antigène HBs obtenu par recombinaison génétique.
1.9 Infections invasives à méningocoques
La vaccination contre les infections invasives à méningocoque est recommandée :
- aux personnes se rendant dans une zone d’endémie, notamment la « ceinture de la méningite » en Afrique subsaharienne : zones de savane et Sahel, d’ouest en est, du Sénégal à l’Ethiopie, au moment de la saison sèche, favorable à la transmission du méningocoque (habituellement hiver et printemps) ou dans toute autre zone où sévit une épidémie, dans des conditions de contact étroit et prolongé avec la population locale :
- pour les nourrissons âgés de 6 à 12 mois en cas d’épidémie due au méningocoque de sérogroupe A : avec le vaccin méningococcique A+C ;
- pour les nourrissons âgés de 2 à 12 mois, en cas d’épidémie due au méningocoque de sérogroupe C : avec le vaccin méningococcique C conjugué 12 ;
- pour les personnes âgées de 12 mois et plus, avec un vaccin polyosidique conjugué A,C,Y,W135.
- aux personnes se rendant dans une zone d’endémie pour y exercer une activité dans le secteur de la santé ou auprès des réfugiés, quelle que soit la saison : avec un vaccin polyosidique conjugué A,C,Y,W135.
Les vaccins disponibles en France figurent dans le tableau 2.
L’actualité des épidémies d’infections invasives à méningocoques est consultable sur le site Internet de l’OMS à l’adresse : http://www.who.int/csr/don/archive/disease/meningococcal_disease/fr/
La vaccination contre les infections invasives à méningocoques avec un vaccin tétravalent A,C,Y,W135 est obligatoire pour l’obtention des visas pour le pèlerinage en Arabie saoudite (cf. § 8.6).
Infections invasives à méningocoques – Schéma vaccinal
Pour les adultes, une injection quel que soit le vaccin utilisé (cf. Tableau 4) au moins 10 jours avant le départ. Pour les nourrissons, se référer au Tableau 3.
Durée de protection : elle reste à préciser pour les vaccins conjugués.
Les vaccins méningococciques sont composés de polyosides capsulaires du germe, conjugués ou non à une protéine.
Il existe également un vaccin exclusivement protéique, dont les indications ne concernent pas spécifiquement les voyageurs (cf. Avis du HCSP relatif à l’utilisation du vaccin Bexsero® (6)).
1.10 Rage
La vaccination contre la rage est recommandée pour les voyageurs devant effectuer un séjour prolongé ou aventureux et en situation d’isolement dans des zones à haut risque (Asie, Afrique y compris l’Afrique du Nord, Amérique du Sud).
Elle est recommandée en particulier chez les jeunes enfants dès qu’ils marchent. En effet, ceux-ci ont un risque plus élevé d’exposition par morsure et/ou par contact mineur passé inaperçu (léchage sur peau excoriée, griffure…).
La vaccination préventive ne dispense pas d’un traitement curatif (deux injections de rappel à J0 et J3), qui doit être mis en œuvre le plus tôt possible en cas d’exposition avérée ou suspectée, mais elle simplifie le traitement et dispense du recours aux immunoglobulines, qui ne sont pas toujours disponibles dans les pays en développement.
Rage – Schéma vaccinal en pré-exposition
Trois injections à J0, J7, J21 ou J28.
Il n’y a pas de rappels systématiques à prévoir en pré-exposition pour les voyageurs ayant complété cette série primaire d’injections mais, en cas d’exposition avérée ou suspectée, deux injections de rappel espacées de 3 jours devront être faites impérativement et le plus tôt possible 13.
Les vaccins rabiques à usage humain sont produits à partir du virus inactivé.
1.11 Rougeole
La vaccination contre la rougeole est recommandée dans le calendrier vaccinal en vigueur 1 aux âges de 12 mois (1ère dose) et 16-18 mois (2e dose). Cependant, pour les nourrissons qui doivent voyager, cette vaccination peut être pratiquée dès l’âge de 6 mois, avec une dose de vaccin rougeoleux monovalent entre les âges de 6 et 11 mois révolus. Les enfants ayant reçu le vaccin rougeoleux monovalent devront recevoir ultérieurement les deux doses de vaccin trivalent (RRO), conformément au calendrier vaccinal. Lorsque la vaccination contre la fièvre jaune est nécessaire, un délai minimum de 28 jours doit être respecté si elle n’est pas réalisée simultanément ; cependant, en cas de départ imminent en zone d’endémie amarile, les deux vaccins peuvent être administrés à n’importe quel intervalle.
Rougeole – Schéma vaccinal
- Une injection avec le vaccin monovalent entre les âges de 6 et 11 mois et deux injections du vaccin trivalent rougeole, rubéole, oreillons, la 1ère à l’âge de 12 mois, la 2e entre les âges de 16 et 18 mois (avec un intervalle d’au moins 1 mois entre les deux doses).
- Pour les personnes nées à partir de 1980 et âgées de plus de 12 mois : deux injections au total de vaccin trivalent quels que soient les antécédents vis-à-vis des trois maladies 1.
- Pour les personnes nées avant 1980, sans antécédent de rougeole ou de vaccination complète et se rendant dans un pays de circulation virale intense, l’administration d’une dose de vaccin monovalent peut se discuter.
Le vaccin rougeoleux, de même que les vaccins ourlien et rubéolique inclus dans la présentation trivalente, sont produits à partir de virus vivants atténués.
1.12 Tuberculose
La vaccination par le BCG est recommandée pour les enfants dès la naissance, en cas de séjours fréquents ou supérieurs à un mois dans les pays à forte incidence tuberculeuse. Elle peut être réalisée jusqu’à l’âge de 15 ans.
Les zones géographiques à forte incidence tuberculeuse sont, selon les estimations de l’OMS :
- le continent africain dans son ensemble ;
- le continent asiatique dans son ensemble, y compris les pays du Proche et du Moyen-Orient ;
- les pays d’Amérique centrale et du Sud ;
- les pays d’Europe centrale et de l’Est y compris les pays de l’ex-URSS, et dans l’Union européenne, la Bulgarie, l’Estonie, la Hongrie, la Lettonie, la Lituanie, la Pologne, le Portugal et la Roumanie.
La vaccination par le BCG est strictement contre-indiquée chez les patients infectés par le VIH, quel que soit le taux de CD4.
Tuberculose – Schéma vaccinal
- De la naissance à l’âge de 2 mois révolus : 0,05 ml de BCG par voie intradermique sans IDR préalable.
- De 3 à 12 mois : 0,05 ml de BCG par voie intradermique après IDR négative.
- Après l’âge de 1 an : 0,1 ml de BCG après IDR négative.
Le BCG est un vaccin vivant atténué.
Pharmacovigilance
Les professionnels de santé doivent déclarer immédiatement tout effet indésirable suspecté d’être dû à un médicament et porté à leur connaissance au Centre régional de pharmacovigilance dont ils dépendent géographiquement.
Les patients et les associations agréées de patients peuvent également signaler tout effet indésirable à leur Centre régional de pharmacovigilance.
Pour plus d’information, consulter la rubrique « Déclarer un effet indésirable » sur le site Internet de l’ANSM : http://ansm.sante.fr.
Comment déclarer : http://ansm.sante.fr/Declarer-un-effet-indesirable/Comment-declarer-un-effet-indesirable/Declarer-un-effet-indesirable-mode-d-emploi/(offset)/0
2. Paludisme
2.1 Données épidémiologiques
Pour l’année 2014, un total de 2 299 cas de paludisme a été déclaré au Centre national de référence (CNR) du Paludisme par les correspondants du réseau métropolitain. Deux cas sont des paludismes présumés autochtones, aéroportuaires. Le nombre de cas de paludisme d’importation a été estimé à environ 4 370 cas pour l’ensemble de la France métropolitaine (représentativité du réseau 2014 : 52,0%, stable par rapport à 2013). À déclarants constants, une augmentation significative des cas, d’environ 8% par rapport à 2013, est observée. Comme pour les dernières années, les pays de contamination sont toujours majoritairement situés en Afrique subsaharienne (96,1%). Les cas ont été observés principalement chez des sujets d’origine africaine (76,5%), résidant en France ou arrivant d’Afrique, et ils sont dus en majorité à l’espèce Plasmodium falciparum (86,0%), stable par rapport à 2013. Un accès à Plasmodium knowlesi a été diagnostiqué chez un voyageur au retour de Sumatra (Indonésie) (séjour en forêt au contact des singes), traité avec succès par la chloroquine.
Il n’y a eu en 2014 qu’un seul cas de paludisme d’importation au retour des Comores contre 53 cas rapportés en 2013 (45 en 2012). Pour les principaux pays de contamination, la tendance à l’augmentation des cas en provenance de la Côte d’Ivoire (n=638, +22%) et du Cameroun (n=402, +14%) par rapport à 2013 se poursuit. Les cas en provenance du Mali sont en diminution modérée de 10%, essentiellement du fait d’une diminution des cas chez les militaires (10 cas en 2014 versus 39 cas en 2013). Les cas en provenance de République centrafricaine augmentent cette année de 69% en lien avec une très forte augmentation des cas chez les militaires (104 cas en 2014 versus 21 en 2013).
Le nombre et la proportion des formes graves, 311 (13,5%), sont en augmentation par rapport à l’année 2013 (267 soit 12,6%). Un total de 11 décès a été déclaré, soit une létalité de 0,48% sur l’ensemble des cas et de 3,7% sur les formes graves ; ces chiffres sont stables par rapport à ceux de 2013. Le traitement par artésunate intraveineux, recommandé par le Haut Conseil de la santé publique en 2013, est maintenant le traitement le plus prescrit (73% des cas).
Au final, l’année 2014 confirme la tendance à l’augmentation des cas de paludisme importés en France métropolitaine observée en 2013. On note cette année une poursuite de l’augmentation des cas en provenance de Côte d’Ivoire et du Cameroun, essentiellement en lien avec les sujets d’origine africaine en visite dans leur famille. La légère diminution du nombre de cas en provenance du Mali et la nette augmentation des cas en provenance de République centrafricaine sont en lien avec les opérations militaires en cours dans ces pays. Concernant les Comores, le nombre de cas atteint son plus bas niveau depuis la mise en place de cette surveillance (1985). Pour les autres pays, les variations observées ne sont pas significatives. Les sujets d’origine africaine sont toujours très majoritaires dans la distribution des cas de paludisme importés. Le nombre de cas graves continue d’augmenter sans que l’on observe d’augmentation concomitante de la létalité.
Les données sur l’évolution des chimiorésistances aux antipaludiques en 2014 sont sans particularité par rapport aux années antérieures, justifiant les recommandations de chimioprophylaxie du paludisme, en adéquation avec les recommandations internationales. Les rares cas de chimiorésistance à la méfloquine et les quelques échecs thérapeutiques à l’atovaquone-proguanil et à l’artéméther-luméfantrine en traitement curatif incitent à recommander des contrôles post-thérapeutiques tardifs (J28) pour ces médicaments à longue demi-vie d’élimination. Le non respect des recommandations de prévention est à l’origine de la plupart des cas de paludisme d’importation étudiés.
Un avis émis par le HCSP en février 2013 a recommandé l’artésunate injectable comme traitement de première intention des formes graves du paludisme chez l’enfant et l’adulte. Ce traitement est disponible dans le cadre d’une ATU nominative délivrée par l’ANSM.
2.2 Chimioprophylaxie
2.2.1 Principes
Aucun moyen préventif n’assure à lui seul une protection totale. Il convient donc d’insister sur la nécessité de l’observance simultanée d’une protection contre les piqûres de moustiques (cf. § 3.1) associée à la chimioprophylaxie.
Toute fièvre au retour des tropiques, quels que soient les symptômes associés, doit être considérée a priori comme pouvant être d’origine palustre et nécessite une consultation en urgence. Environ 3% des paludismes à P. falciparum sont encore observés au-delà des habituels deux mois suivant le retour.
Le choix d’une chimioprophylaxie doit tenir compte :
- des zones visitées, selon les résistances aux médicaments antipaludiques (Tableau 5) ;
- de l’intensité de la transmission ;
- des conditions, de la durée et de la période du séjour ;
- de l’âge et du poids du voyageur ;
- de ses antécédents pathologiques ;
- d’une possible interaction avec d’autres médicaments ;
- d’une précédente intolérance à un antipaludique ;
- d’une grossesse en cours ou envisagée ;
- de l’évaluation de l’observance en fonction des modalités de prise ;
- des capacités financières du voyageur.
 Agrandir l’image
Agrandir l’image
Quel que soit l’antipaludique choisi, il ne peut être délivré que sur ordonnance, en conseillant sa prise au cours d’un repas. La prophylaxie doit être poursuivie après la sortie de la zone d’endémie pour une durée variable selon le médicament prescrit. Aucun produit n’étant toujours parfaitement toléré, il peut être admissible, pour des personnes autonomes et bien informées, pour des séjours inférieurs à sept jours, dans une zone à très faible transmission et correctement médicalisée, d’avoir recours à la seule protection contre les moustiques.
La chimioprophylaxie vise essentiellement à prévenir les risques d’infection à Plasmodium falciparum (Afrique surtout, Amérique et Asie forestières), l’évolution pouvant être fatale. De plus, les résistances de cette espèce à certains antipaludiques sont fréquentes.
Plasmodium vivax (Asie, Amérique, Afrique de l’Est) et Plasmodium ovale (Afrique de l’Ouest) provoquent des accès palustres d’évolution généralement bénigne. La chimioprophylaxie prévient l’accès primaire mais pas les rechutes, pouvant survenir dans les deux ou trois années qui suivent l’infection. Seule une cure de primaquine prescrite dès le premier accès préviendra ces rechutes. La primaquine est accessible avec autorisation temporaire d’utilisation (ATU) nominative délivrée par l’ANSM sur demande des cliniciens. De rares cas de résistance de Plasmodium vivax à la chloroquine ont été signalés dans quelques pays d’Asie et d’Océanie.
Plasmodium malariae est plus rarement observé. L’évolution de l’infection est bénigne, mais l’accès survient parfois plusieurs années après le séjour.
Des cas de paludisme dus à un parasite du singe, Plasmodium knowlesi, ont été signalés assez fréquemment depuis 2004 chez l’homme, dans les zones forestières d’Asie (Bornéo, Malaisie péninsulaire, Philippines (île de Palawan), Singapour, Myanmar, Thaïlande, Cambodge, Vietnam), avec un risque d’accès grave, voire de décès. Douze cas ont été identifiés depuis 2008 chez des voyageurs en Europe (8 dont 1 en France), aux USA, en Australie et en Nouvelle-Zélande. Il a été récemment montré que ce plasmodium a une sensibilité réduite à la méfloquine et une sensibilité modérée et variable à la chloroquine.
2.2.2 Schémas prophylactiques (Tableau 6)
• Chloroquine (Nivaquine® 100 mg et Nivaquine® sirop 25 mg/5 ml) :
- pour une personne pesant au moins 50 kg, la posologie est d’un comprimé chaque jour ;
- pour une personne de moins de 50 kg et chez les enfants, la posologie est de 1,5 mg/kg/jour.
La chloroquine peut être administrée aux femmes enceintes.
La prise est à débuter le jour de l’arrivée dans la zone à risque, et à poursuivre quatre semaines après avoir quitté la zone d’endémie.
• Association chloroquine et proguanil :
- soit un comprimé de Nivaquine® 100 (chloroquine) et deux comprimés de Paludrine® 100 (proguanil) chaque jour, en une seule prise au cours d’un repas ;
- soit l’association fixe chloroquine base 100 mg + proguanil 200 mg : Savarine® un comprimé par jour ou Nopalu® une gélule par jour, pour une personne pesant au moins 50 kg.
Savarine® ou Nopalu® n’ayant pas de présentation adaptée à l’enfant, la chloroquine à la dose de 1,5 mg/kg/j et le proguanil à 3 mg/kg/j (à partir de 9 kg) sont prescrits séparément chez les sujets de moins de 50 kg.
La chloroquine, le proguanil, la Savarine® et le Nopalu® peuvent être administrés aux femmes enceintes.
La prise est à débuter le jour de l’arrivée dans la zone à risque, et à poursuivre quatre semaines après l’avoir quittée.
• Association atovaquone (250 mg) - proguanil (100 mg) :
- pour les personnes pesant plus de 40 kg, la posologie est d’un comprimé par jour, au cours d’un repas ;
- pour les enfants pesant de 11 à 40 kg, l’association est disponible en comprimés pédiatriques (atovaquone : 62,5 mg, proguanil : 25 mg), permettant l’administration de ce médicament en prophylaxie ;
- pour les enfants de 5 kg à moins de 11 kg, en l’absence de formes pharmaceutiques adaptées disponibles à ce jour, l’association peut être utilisée en prophylaxie hors autorisation de mise sur le marché, en coupant les comprimés ;
- pour la femme enceinte, l’association peut être prescrite en cas de séjour inévitable dans les zones où cette association est recommandée.
Le suivi de grossesses exposées à l’association atovaquone-proguanil est insuffisant à ce stade pour exclure formellement tout risque malformatif ou fœtotoxique.
La prise est à débuter le jour d’arrivée en zone à risque et doit être poursuivie une semaine après la sortie de cette zone. La durée d’administration continue de l’atovaquone-proguanil dans cette indication devra être limitée à trois mois, faute de disposer à ce jour d’un recul suffisant en prophylaxie prolongée.
• Méfloquine (Lariam® 250 mg) :
- pour une personne pesant plus de 45 kg, la posologie est d’un comprimé une fois par semaine ;
- pour les enfants, la chimioprophylaxie obéit aux mêmes règles que pour l’adulte, à la dose de 5 mg/kg/semaine. Cependant, le produit n’existe que sous forme de comprimé quadrisécable qui ne permet d’adapter la prophylaxie que chez les sujets de plus de 15 kg. En France, la méfloquine n’a pas d’AMM en chimioprophylaxie du paludisme pour les enfants pesant moins de 15 kg. Cependant, l’OMS permet son utilisation à partir d’un poids de 5 kg et les recommandations américaines de 2014 recommandent une dose de 5 mg/kg/semaine pour un poids ≤9 kg et d’un quart de comprimé par semaine pour un poids compris entre 9 et 19 kg.
- pour la femme enceinte, la méfloquine peut être prescrite en cas de séjour inévitable dans les zones où cette association est recommandée ; l’analyse d’un nombre élevé de grossesses exposées n’a relevé aucun effet malformatif ou fœtotoxique particulier dû à ce médicament administré en prophylaxie.
Le traitement est à débuter au moins 10 jours avant l’arrivée dans la zone à risque pour apprécier la tolérance de deux prises. Sauf si ce médicament a déjà été utilisé antérieurement et était bien toléré, il est même préférable, dans la mesure du possible, d’effectuer trois prises avant le départ afin de pouvoir détecter un éventuel effet secondaire survenant plus tardivement.
L’apparition sous traitement de troubles neuropsychiques tels qu’une anxiété aiguë, un syndrome dépressif, une agitation, une confusion mentale, des idées suicidaires ou même des troubles mineurs tels qu’une tristesse inexpliquée, des céphalées, des vertiges ou des troubles du sommeil (cauchemars), doit conduire à l’interruption immédiate de cette prophylaxie et à une consultation médicale. Le voyageur doit être informé de la survenue possible de ces effets secondaires.
En juillet 2013, l’information sur le profil de risque de la méfloquine a été actualisée, avec un renforcement des informations concernant les troubles neuropsychiatriques dans le résumé des caractéristiques du produit, la mise en place d’une brochure destinée aux professionnels de santé ainsi qu’une carte de surveillance patient afin de minimiser le risque de ces effets indésirables neuropsychiatriques.
La prise de méfloquine doit être poursuivie trois semaines après avoir quitté la zone d’endémie, soit trois prises.
En cas de contre-indication ou d’effet indésirable de la méfloquine entraînant l’arrêt du traitement, peuvent être proposées : - l’association atovaquone+proguanil ;
- la doxycycline (au-delà de l’âge de 8 ans et en l’absence de grossesse en cours) ;
- l’association chloroquine-proguanil (Nivaquine® + Paludrine® ou Savarine® ou Nopalu®) en dépit de sa moindre efficacité ; il conviendra alors de renforcer les mesures de protection contre les piqûres de moustiques.
• Doxycycline (monohydrate de doxycycline : Doxypalu® comprimés à 50 ou 100 mg, Granudoxy®Gé comprimés sécables à 100 mg ; hyclate de doxycycline : Doxy® Gé 100 et Doxy® Gé 50 comprimés) :
- pour les sujets de plus de 40 kg, la posologie est de 100 mg/jour ;
- pour les sujets de moins de 40 kg, la posologie est de 50 mg/jour.
La doxycycline est contre-indiquée avant l’âge de 8 ans, déconseillée pendant le premier trimestre de la grossesse et contre-indiquée à partir du deuxième trimestre (elle expose l’enfant à naître au risque de coloration des dents de lait). Elle peut entraîner une photodermatose par phototoxicité si les précautions d’emploi ne sont pas respectées. Il est conseillé une prise le soir au cours du repas, au moins 1 h avant le coucher et le recours à une protection solaire adaptée.
La prise est à débuter le jour de l’arrivée dans la zone à risque et à poursuivre quatre semaines après l’avoir quittée. L’observance journalière est impérative, compte-tenu de la courte demi-vie de la molécule dans le sang. En cas de contre-indication et en fonction de la zone d’endémie concernée, les alternatives sont : méfloquine, atovaquone+proguanil, choroquine+proguanil (voir ci-dessus).
 Agrandir l’image
Agrandir l’image
Pharmacovigilance
Les professionnels de santé doivent déclarer immédiatement tout effet indésirable suspecté d’être dû à un médicament et porté à leur connaissance au Centre régional de pharmacovigilance dont ils dépendent géographiquement.
Les patients et les associations agréées de patients peuvent également signaler tout effet indésirable à leur Centre régional de pharmacovigilance.
Pour plus d’information, consulter la rubrique « Déclarer un effet indésirable » sur le site Internet de l’ANSM : http://ansm.sante.fr.
Comment déclarer : http://ansm.sante.fr/Declarer-un-effet-indesirable/Comment-declarer-un-effet-indesirable/Declarer-un-effet-indesirable-mode-d-emploi/(offset)/0
2.2.3 Chimioprophylaxie selon les zones
Les recommandations de chimioprophylaxie par zones sont indiquées dans le tableau 5.
Cas particuliers
- Courts séjours en zone de faible risque
Pour un court séjour (inférieur à sept jours : durée minimum d’incubation du paludisme à P. falciparum) en zone de faible risque de transmission, la chimioprophylaxie n’est pas indispensable, à condition de respecter scrupuleusement les règles de protection anti-moustiques et d’être en mesure, durant les mois qui suivent le retour, de consulter en urgence en cas de fièvre, en signalant la notion de voyage en zone d’endémie palustre. - Variabilité des niveaux de transmission selon les régions des pays
Il n’y a pas de transmission du paludisme dans les grandes villes du Proche et du Moyen-Orient, du reste de l’Asie (excepté en Inde) et d’Amérique du Sud (excepté en Amazonie). Le paludisme ne se transmet habituellement pas au-dessus de 1 500 mètres d’altitude en Afrique et de 2 500 mètres en Amérique ou en Asie.
L’identification du pays de destination est insuffisante ; il faut aussi tenir compte de la région visitée (Tableau 5), des conditions de séjour et de la saison.
2.3 Séjours de longue durée (plus de trois mois) 15
La prévention du paludisme doit faire l’objet d’une information approfondie. Il est utile de remettre au patient un document rédigé. Il est nécessaire d’insister sur la protection contre les piqûres de moustiques (répulsifs, moustiquaire, etc., cf. § 3.1 et 3.2). Lors du premier séjour, la chimioprophylaxie adaptée au niveau de résistance devrait être poursuivie au moins pendant les six premiers mois. Au-delà de cette durée et si la poursuite d’une prise continue pendant plusieurs années pose des problèmes d’observance, la chimioprophylaxie peut être modulée avec l’aide des médecins référents locaux. Une prise intermittente durant la saison des pluies ou lors de certains déplacements en zone rurale peut par exemple être envisagée. Dans tous les cas, il est indispensable que la prise en charge rapide d’une fièvre par le médecin référent puisse être assurée. Il convient de prévenir les intéressés de la persistance du risque d’accès grave lors des retours de zone d’endémie, surtout pendant les deux premiers mois.
2.4 Séjours itératifs de courte durée
Certains professionnels sont amenés à faire des séjours brefs et répétés pendant plusieurs années, voire toute leur carrière (navigants, ingénieurs et techniciens pétroliers ou miniers, commerciaux divers). Dans ces cas, une chimioprophylaxie antipaludique prolongée est inappropriée, voire contre-indiquée. Le médecin du travail de ces entreprises doit jouer un rôle essentiel d’information personnalisée, répétée annuellement, portant sur la prévention des piqûres de moustiques et l’incitation à consulter en urgence un médecin référent en cas de fièvre. La remise d’un document d’information sur les pays à risque, mis à jour tous les ans, s’impose. L’établissement, à l’initiative de la médecine du travail, d’une carte personnelle, nominative, jointe en permanence aux papiers d’identité, indiquant les voyages professionnels répétés en zone tropicale et le risque de paludisme, est nécessaire. Cette carte comportera un numéro de téléphone d’urgence d’un contact professionnel capable d’informer sur les déplacements récents. La prescription d’un traitement présomptif (voir ci-après § 2.5) est envisageable chez ces personnes.
2.5 Traitement présomptif
Un traitement antipaludique sans avis médical pendant le séjour doit rester l’exception et ne s’impose qu’en l’absence de possibilité de prise en charge médicale dans les 12 heures suivant l’apparition de la fièvre. Il doit toujours être l’application de la prescription d’un médecin, consulté avant le départ. La possession d’un médicament destiné à un traitement dit « de réserve » en zone d’endémie palustre peut se justifier lors d’un séjour de plus d’une semaine avec déplacements en zone très isolée, mais aussi dans des circonstances qui incitent, après avis d’un médecin référent, à ne plus poursuivre la chimioprophylaxie antipaludique, telles que les voyages fréquents et répétés (voir ci-dessus § 2.4) ou après six mois d’expatriation. Les tests de diagnostic rapide disponibles sur le marché ne sont pas recommandés pour l’autodiagnostic, plusieurs études ayant montré que la majorité des voyageurs ne sont pas en mesure de conserver ni de réaliser correctement ces tests ou d’en interpréter les résultats. Les molécules utilisables pour ce traitement de réserve sont les associations atovaquone-proguanil, artéméther-luméfantrine ou dihydroartémisinine-pipéraquine, en tenant compte pour cette dernière association du risque d’allongement de l’espace QTc sous traitement (Tableau 7).
 Agrandir l’image
Agrandir l’image
Si le voyageur est amené à prendre de lui-même un tel traitement, il doit être informé de la nécessité de consulter, de toute façon, un médecin dès que possible. Dans le cas où une consultation médicale et une recherche parasitologique sont possibles dans l’immédiat, mieux vaut y recourir. L’halofantrine (Halfan®) ne doit pas être prescrite dans le cadre de l’auto-traitement par le voyageur d’une fièvre suspectée de cause palustre, en raison de sa cardiotoxicité potentielle.
Le voyageur doit être informé des risques liés à l’achat de spécialités hors de France, en raison du grand nombre de contrefaçons circulant dans les pays en développement et des risques liés à l’achat de médicaments sur Internet, dont ni l’origine, ni la composition ne sont garantis. Il doit également être mis en garde sur l’utilisation de sa propre initiative d’autres antipaludiques, non disponibles en France, aisément accessibles dans certains pays d’endémie, notamment les produits qui contiennent des dérivés de l’artémisinine et qui ne doivent pas être pris en monothérapie. Le fait de disposer d’un médicament de réserve ne dispense pas le voyageur de suivre les conseils prodigués en matière de chimioprophylaxie ou de protection contre les moustiques.
Compte tenu des risques liés à un mésusage d’un traitement de réserve chez les enfants, il n’est pas recommandé de voyager avec des enfants dans une zone où une consultation médicale serait impossible dans un délai maximal de 12 heures.
Un traitement de réserve ne doit jamais être pris au retour en France.
3. Risques liés aux arthropodes
Les risques liés aux insectes et autres arthropodes sont principalement des risques de transmission de maladies parfois très graves, voire mortelles, et sont à évaluer en fonction de la destination et des conditions de séjour. De façon générale, pour les voyages vers des destinations à climat chaud ou tropical, il est recommandé de :
- se protéger contre les piqûres d’insectes, notamment avec des répulsifs sur les parties non couvertes (voir encadré ci-après sur les répulsifs cutanés) ;
- dormir la nuit sous une moustiquaire imprégnée d’insecticide si possible (correctement installée et en s’assurant de l’intégrité du maillage) ;
- porter des vêtements légers et couvrants (manches longues, pantalons et chaussures fermées) ;
- utiliser des vêtements imprégnés d’insecticides en cas de risques importants.
Dans les habitations, la climatisation diminue les risques de piqûres, des insecticides en bombes ou en diffuseurs électriques ainsi que les raquettes électriques pourront être utilisés en mesure d’appoint. À l’extérieur et dans les vérandas, les serpentins fumigènes peuvent constituer des répulsifs efficaces.
3.1 Risques liés aux moustiques
Les moustiques sont vecteurs de nombreux agents pathogènes tels que des virus et des parasites et sont également responsables de fortes nuisances (voir sites du ministère des Affaires sociales, de la Santé http://www.sante.gouv.fr et de l’Institut de veille sanitaire http://www.invs.sante.fr). Il est donc recommandé de se protéger contre leurs piqûres avec un type de protection adapté au risque de maladie (Tableau 8). Il est également recommandé de ne pas favoriser la multiplication des moustiques en laissant de l’eau dans des récipients.
3.1.1 Moustiques qui piquent plutôt la nuit et peuvent transmettre le paludisme, certaines arboviroses (Virus du Nil occidental, Encéphalites américaines, Encéphalite japonaise) et des filarioses
Ces moustiques appartiennent aux genres Anopheles et Culex. Les anophèles piquent habituellement entre le coucher et le lever du soleil et les Culex piquent surtout la nuit. Mais ces comportements ne sont pas toujours aussi stricts. Il est donc recommandé d’éviter les piqûres la nuit et de se protéger le jour. Ces moustiques se rencontrent dans toutes les zones tropicales d’Afrique, d’Amérique et d’Asie et aussi dans des zones plus tempérées, notamment aux États-Unis, en Asie et parfois en Europe.
3.1.2 Moustiques qui piquent plutôt le jour et peuvent transmettre des arboviroses (dengue, chikungunya, zika…) et des filarioses
Ces moustiques appartiennent au genre Aedes et piquent habituellement le jour. La dengue sévit sur un mode endémo-épidémique sur tous les continents, dans l’ensemble des zones tropicales, mais des épidémies peuvent aussi émerger dans des zones plus tempérées comme à Madère en 2012. Le virus chikungunya est responsable d’épidémies survenant principalement dans le sous-continent indien, en Asie du Sud-Est, en Afrique et dans les îles de l’Océan Indien. Le virus circule dans les Caraïbes depuis fin 2013 et s’est propagé en 2014 sur le continent américain. De même, dans le Pacifique, des épidémies ont été rapportées en Polynésie française (pour la première fois), en Nouvelle-Calédonie et aux Îles Cook, Samoa et Kiribati (Carte 5). Depuis 2013, le virus Zika est responsable d’épidémies dans la région Pacifique (Cf. chapitre 11).
Les moustiques du genre Aedes transmettent également les filarioses lymphatiques en Océanie. La meilleure protection contre les piqûres de ces moustiques est l’application de répulsifs cutanés sur les parties non couvertes du corps et l’utilisation de vêtements couvrants, voire imprégnés d’insecticides (Cf. encadré ci-après sur les répulsifs cutanés et Tableaux 9 et 10).
Les répulsifs cutanés
Dans la stratégie de protection contre les vecteurs, les répulsifs sont nécessaires en fonction des risques (Tableau 8), de la même façon que l’utilisation de la moustiquaire. La surveillance et l’entretien intra- et péri-domiciliaire contre les gîtes sont également indispensables quand cela est possible. La tenue vestimentaire peut être un complément pour une meilleure protection.
Les répulsifs cutanés sont composés d’une substance active qui éloigne les insectes sans les tuer et sont à appliquer sur toutes les parties du corps non couvertes. Il faut privilégier l’application le matin et le soir, périodes d’activité maximum des insectes vecteurs.
La durée de la protection varie de 4 à 8 heures selon la nature et la concentration de la substance active ainsi que des conditions d’utilisation (sudation, température et humidité ambiantes…).
L’application doit être renouvelée après une baignade.
En cas d’utilisation de crème solaire, l’application de répulsif doit avoir lieu après un délai d’au moins 20 minutes. La crème solaire doit toujours être appliquée avant le répulsif.
Ces produits sont à employer avec précaution, ils ne doivent pas être ingérés, ni appliqués sur les muqueuses ou sur des lésions cutanées étendues.
Chez l’enfant et la femme enceinte leur utilisation doit respecter un mode d’emploi précis (Tableau 9).
Chez l’enfant, l’application ne doit pas être faite sur les mains.
Chez la femme allaitante, leur utilisation est possible en respectant les mêmes précautions que chez les autres adultes et en veillant à la non-application au niveau du sein ainsi qu’au lavage des mains avant la mise au sein.
3.1.3 Moustiques responsables de fortes nuisances
Les nuisances provoquées par des populations abondantes et agressives de certains moustiques existent dans tous les pays du monde, de l’équateur au cercle polaire. En effet, les moustiques des pays nordiques peuvent se montrer très agressifs durant la courte période estivale. Il est donc recommandé de s’en protéger avec des vêtements imprégnés d’insecticides et des répulsifs cutanés.
Enfin, il faut éviter la surinfection des piqûres par grattage, en particulier chez l’enfant, en utilisant, si nécessaire (et sur avis médical), un dermocorticoïde associé à un anti-histaminique en cas de prurit intense.
 Agrandir l’image
Agrandir l’image
 Agrandir l’image
Agrandir l’image
 Agrandir l’image
Agrandir l’image
3.2 Prévention contre les piqûres de moustiques
Pour se protéger des moustiques qui piquent la nuit, la meilleure protection est l’utilisation d’une moustiquaire imprégnée d’insecticide pour dormir. Il est fortement recommandé d’éviter de sortir la nuit, même un court moment, sans protection anti-moustiques, et a fortiori de dormir la nuit à la belle étoile, sans moustiquaire imprégnée, surtout dans les zones fortement impaludées.
La moustiquaire imprégnée d’insecticide assure la meilleure protection contre les piqûres de moustiques nocturnes par son effet à la fois insecticide et insectifuge. Elle est disponible en pharmacie ou dans des magasins spécialisés. Il est possible d’imprégner soi-même une moustiquaire avec un kit d’imprégnation vendu également en pharmacie. Le seul produit disponible est la perméthrine. En cas d’imprégnation par trempage de moustiquaire, la rémanence du produit varie de un à trois mois et ne résiste généralement pas à plus de trois lavages. Il existe maintenant des moustiquaires imprégnées industriellement, dont certaines à longue durée d’efficacité, résistantes à des lavages successifs (Tableau 11).
Pour se protéger des piqûres de moustique en soirée ou en journée, l’usage de répulsifs cutanés est fortement recommandé (Cf. Encadré sur les répulsifs cutanés et Tableaux 8 & 9). Les vêtements et les toiles de tente peuvent également être imprégnés par spray ou trempage dans la perméthrine, disponible en pharmacie ou dans les magasins spécialisés du voyage (Tableau 10).
Pour les enfants avant l’âge de la marche, l’utilisation de moustiquaires, de préférence imprégnées de perméthrine, sur les berceaux et les poussettes, reste la méthode la plus efficace.
Par contre, il est fortement recommandé de ne pas utiliser :
- les bracelets anti-insectes pour se protéger des moustiques et des tiques ;
- les huiles essentielles dont la durée d’efficacité, généralement inférieure à 20 minutes, est insuffisante ;
- les appareils sonores à ultrasons, la vitamine B1, l’homéopathie, les rubans, papiers et autocollants gluants sans insecticide 16.
3.3 Risques liés aux autres insectes piqueurs (phlébotomes, mouches, punaises, poux et puces)
Les risques liés aux insectes piqueurs autres que les moustiques, sont également à prendre en compte pour toutes les destinations. Ces risques sont particulièrement importants pour des séjours en zone rurale et/ou dans des conditions de confort sommaire. Les insectes vecteurs de maladies, leurs zones de risques et les protections adaptées sont reportés dans le Tableau 12. Le voyageur devra se garder de ramener chez lui des punaises de lit, insecte susceptible de voyager dans les bagages et nuisance ré-émergente dans le monde (Cf. § 11.7)
 Agrandir l’image
Agrandir l’image
3.4 Risques liés aux autres arthropodes
3.4.1 Tiques
Les tiques sont des arthropodes hématophages qui absorbent le sang de leurs hôtes et peuvent transmettre des virus et bactéries responsables de maladies telles que les borrélioses (la maladie de Lyme 17 en Europe et en Amérique du Nord), des encéphalites, des fièvres hémorragiques et certaines rickettsioses.
Un vaccin existe contre la méningo-encéphalite à tiques, mais la seule prévention contre les autres infections transmises par les tiques reste la couverture vestimentaire et l’application de répulsifs cutanés sur les parties découvertes. Pour les tiques, les données de la littérature laissent penser que le DEET est actif, les autres répulsifs ayant été moins étudiés.
Les tiques s’accrochent sur un hôte de passage (animal ou être humain) qui circule dans leur milieu naturel. Il est donc impératif, après toute promenade en milieu rural et particulièrement en forêt dans les régions infestées, de bien s’examiner et d’examiner ses enfants pour rechercher la présence éventuelle de tiques sur le corps et sur le cuir chevelu afin de les ôter très rapidement. Pour cela, un tire-tique ou une pince à épiler peuvent être utilisés : la tique doit être saisie délicatement et retirée sans forcer en lui imprimant un mouvement de rotation, afin d’éviter que son appareil buccal ne se casse dans la plaie ; cette plaie doit ensuite être désinfectée.
3.4.2 Acariens microscopiques
Les acariens microscopiques, du type aoûtats, peuvent infester la peau lors de promenades en milieu naturel, en particulier en zone tropicale, et provoquer de fortes démangeaisons. Pour s’en protéger il est recommandé d’utiliser des répulsifs cutanés. En Asie, l’un de ces acariens microscopiques transmet le typhus des broussailles.
3.4.3 Arthropodes venimeux
Les risques liés aux autres arthropodes piqueurs tels que les araignées, les scolopendres, les scorpions, et à certains insectes sociaux (guêpes, frelons, abeilles…) entrent dans la catégorie des envenimations (manifestations locales et/ou générales induites par la pénétration dans l’organisme d’une substance toxique). Toute piqûre qui entraîne des troubles importants (fièvre, nausées, douleur vive, gonflement, etc.) nécessite une consultation au service des urgences le plus proche si le déplacement est possible, ou l’appel des secours si le déplacement n’est pas possible.
Prévention
En cas de bivouac, il est recommandé de protéger ses affaires personnelles (vêtements, chaussures, etc.) en les rangeant dans un sac ou un bidon en plastique étanche et bien fermé, contenant des boules insecticides.
4. Diarrhée du voyageur et autres risques liés à l’alimentation
La diarrhée affecte fréquemment les voyageurs, son taux d’attaque pouvant dépasser 50% pour un séjour de trois semaines. Il s’agit généralement d’un épisode aigu bénin, spontanément résolutif en un à trois jours, mais qui peut être parfois grave. Elle est plus souvent liée à la consommation d’aliments solides que de boissons.
Parmi les étiologies, sont retrouvées les infections virales (rotavirus, norovirus…), bactériennes (Escherichia coli entérotoxinogène, Salmonella enterica non typhi, Shigella spp, Campylobacter spp, Yersinia enterocolitica, Vibrio cholerae,…) ou parasitaires (Giardia intestinalis, Cryptosporidium spp, Isospora belli, Cyclospora cayatanensis, Entamoeba histolytica,…).
Une consultation médicale est recommandée systématiquement chez l’enfant âgé de moins de 2 ans et aux autres âges dans les formes moyennes ou sévères, fébriles ou avec selles glairo-sanglantes, ou prolongées au-delà de 48 heures ou en cas de vomissements incoercibles.
4.1 Prévention
4.1.1 Hygiène
La prévention repose avant tout sur les mesures d’hygiène.
- Se laver souvent les mains, avant les repas et avant toute manipulation d’aliments, et après passage aux toilettes. En l’absence d’eau et de savon, un gel ou une solution hydroalcoolique peuvent être utilisés (attention au risque de photosensibilité).
- Ne consommer que de l’eau en bouteille capsulée (bouteille ouverte devant soi), ou à défaut rendue potable par ébullition (1 minute à gros bouillons), ou par la combinaison d’une filtration (filtre portatif) suivie d’une désinfection [produits à base de DCCNa (dichloroisocyanurate de sodium), ou hypochlorite de sodium].
- Ne pas consommer l’eau en sachet.
- Éviter les glaçons.
- Éviter les jus de fruits frais préparés de façon artisanale.
- Éviter de consommer de la nourriture vendue dans la rue sauf si elle est bien cuite et le récipient encore fumant. Les buffets froids des restaurants peuvent également comporter des risques.
- Le lait doit être pasteurisé ou bouilli et la chaîne du froid assurée.
- Peler les fruits soi-même.
- Éviter les crudités, les coquillages, les plats réchauffés.
- Éviter les sorbets et les crèmes glacées.
- Bien cuire les œufs, les viandes, les poissons et les crustacés.
- Se renseigner localement sur les risques de toxicité des poissons de mer (ciguatera).
4.1.2 Prophylaxie médicamenteuse
La prévention médicamenteuse n’est pas indiquée en dehors de situations particulières (maladies inflammatoires chroniques de l’intestin notamment) et après avis spécialisé.
4.2 Traitement
Dans tous les cas, les mesures pour éviter ou corriger la déshydratation sont essentielles au traitement. Il est important de boire abondamment (liquides salés et sucrés en alternance) et, en particulier chez les jeunes enfants et les personnes âgées, d’utiliser des sels de réhydratation orale (sachets à diluer) à administrer à volonté et par petites doses successives en cas de vomissements.
Les parents de jeunes enfants doivent pouvoir reconnaître les premiers signes de la déshydratation et connaître les mesures nécessaires pour la prévenir :
- utiliser rapidement les solutés de réhydratation orale (SRO) ;
- réalimenter précocement l’enfant en assurant les apports caloriques nécessaires.
Les parents doivent être avertis de la nécessité de consulter rapidement.
4.2.1 Traitement symptomatique
Les anti-diarrhéiques ne sont pas recommandés en première intention chez les personnes présentant une diarrhée glairo-sanglante et/ou associée à une fièvre importante.
- La prise d’un anti-diarrhéique antisécrétoire (racecadotril) peut atténuer la symptomatologie clinique. Le racecadotril est contre-indiqué chez la femme qui allaite.
- L’usage d’un anti-diarrhéique moteur (lopéramide sous forme de chlorhydrate ou sous forme d’oxyde de lopéramide monohydraté) est à restreindre au cas survenant dans des circonstances particulières (accès difficile aux sanitaires) en respectant les contre-indications, dont les enfants âgés de moins de 2 ans.
- Les pansements intestinaux ne sont pas indiqués dans la diarrhée.
4.2.2 Antibiothérapie
En l’absence de possibilités de consultation rapide et de diagnostic étiologique, une antibiothérapie empirique (avec une fluoroquinolone ou l’azithromycine) est indiquée dans les formes moyennes ou sévères, fébriles ou avec selles glairo-sanglantes (syndrome dysentérique) (Cf. schémas posologiques pour l’adulte et l’enfant dans le Tableau 13). Partout sauf en Asie, la préférence sera donnée chez l’adulte à une fluoroquinolone (ofloxacine ou ciprofloxacine), mais il convient de respecter les contre-indications et les précautions d’utilisation.
Cette classe d’antibiotiques comporte en particulier un risque de tendinopathie, accru chez les sportifs, et de photosensibilisation. Il est important d’informer les patients de ces effets indésirables potentiels et des symptômes qui doivent les alerter.
- Les fluoroquinolones sont contre-indiquées pendant toute la durée de la grossesse (à l’exception de la ciprofloxacine qui peut éventuellement être prescrite, mais avec prudence) et chez la femme allaitante.
- Chez l’enfant et l‘adolescent, en raison du risque de survenue d’arthropathies graves, leur utilisation doit être réservée pour des cas cliniques sévères et là encore, seule la ciprofloxacine est autorisée, car c’est la mieux connue en pédiatrie.
- En Asie, en raison d’un niveau élevé de résistance des shigelles, des salmonelles et de Campylobacter aux fluoroquinolones, c’est l’azithromycine qui est recommandée (hors AMM) en première intention.
- Chez l’adulte, cette molécule représente également une alternative en cas de contre-indication aux fluoroquinolones.
- Par précaution, on évitera de prescrire l’azithromycine au premier trimestre de la grossesse, en raison du manque de données.
- Chez l’enfant et l’adolescent, l’azithromycine peut être utilisée dans les diarrhées suspectées bactériennes, en complément de la réhydratation.
NB. En raison d’un effet potentiel sur le rythme cardiaque (troubles de la repolarisation), la prudence est de mise chez les patients à risque d’allongement de l’intervalle QT, ou chez ceux qui présentent une maladie cardiaque sous-jacente.
 Agrandir l’image
Agrandir l’image
5. Transports
5.1 Accidents de la voie publique
Les accidents (de la circulation ou non) représentent une des principales causes de rapatriement sanitaire et de mortalité. Dans toute la mesure du possible, les règles de prévention (port de la ceinture de sécurité, port du casque si l’on circule à deux-roues et utilisation de sièges auto pour les enfants en bas âge) doivent être respectées. Il faut éviter de conduire soi-même (prendre un chauffeur) et se montrer particulièrement prudent si l’on doit conduire de nuit.
5.2 Transports aériens
- Conseils généraux
- Emporter les médicaments en cabine (dans le respect de la réglementation régissant le transport des produits et matériels). Garder les médicaments délivrés sur ordonnance dans leur emballage ou récipient d’origine, accompagnés d’une lettre d’un médecin certifiant que le passager en a besoin, notamment si les médicaments doivent être administrés sous forme injectable.
- Prendre un avis médical spécialisé avant le départ pour les personnes atteintes de certaines affections chroniques (cf. § 8.4).
- Tenir compte du décalage horaire pour la prise de certains médicaments (contraceptifs oraux, anticoagulants, insuline...).
- Prévention des thromboses veineuses profondes liées à un voyage aérien 18
Le transport aérien apparaît comme un facteur de risque de thrombose veineuse, multipliant le risque par deux. Certains voyageurs peuvent aussi avoir un facteur de risque indépendant : âge, antécédents personnels ou familiaux de thrombose veineuse ou d’embolie pulmonaire, thrombophilie, contraception œstro-progestative ou œstrogénothérapie de substitution hormonale, obésité, varices, intervention chirurgicale récente concernant notamment l’abdomen, le bassin ou les membres inférieurs, tabagisme, grossesse. Les mesures suivantes peuvent être recommandées à titre préventif : - tous les voyageurs doivent s’hydrater régulièrement au cours du vol, bouger fréquemment leurs jambes, se déplacer dans l’avion et suivre les programmes d’exercices proposés en cours de vol, réalisables sans quitter sa place ;
- la présence d’au moins un facteur de risque de thrombose justifie le port d’une contention élastique (mi-cuisse plus confortable que sous le genou) de classe 2 (pression à la cheville de 15 à 30 mmHg) ; cette mesure devrait même concerner tous les voyageurs qui ne déambulent pas régulièrement à bord, plus particulièrement pour tous les voyages de plus de 6 heures ;
- les héparines de bas poids moléculaire ou le fondaparinux (inhibiteur du facteur X) n’ont pas d’indication validée mais sont parfois prescrits hors AMM à dose prophylactique chez les sujets pour lesquels la contention n’est pas possible ou en cas de risque très élevé. La prise d’aspirine ne prévient pas les thromboses veineuses.
- Contre-indications à un voyage aérien
Les contre-indications aux voyages aériens sont résumées dans l’encadré ci-après.
Contre-indications aux voyages aériens
(Recommandations de l’Organisation mondiale de la santé) 18.
Les voyages aériens sont normalement contre-indiqués dans les cas suivants :
- nouveau-nés âgés de moins de 48 heures ;
- femmes enceintes après la 36e semaine de grossesse (après la 32e semaine en cas de grossesse multiple) ;
- personnes souffrant d’une des maladies suivantes, sur avis médical :
- angor (angine de poitrine) ou douleurs thoraciques au repos ;
- maladie transmissible évolutive ;
- mal de décompression après la plongée ;
- augmentation de la pression intracrânienne en raison d’une hémorragie, d’un traumatisme ou d’une infection ;
- infection des sinus, de l’oreille ou du nez, particulièrement si la trompe d’Eustache est bouchée ;
- infarctus du myocarde ou accident vasculaire cérébral récent (le délai à respecter dépendra de la gravité de la pathologie et de la durée du voyage) ;
- intervention chirurgicale récente ou traumatisme récent comportant un risque de flatulence (en particulier traumatisme abdominal ou intervention gastro-intestinale) ;
- traumatisme cranio-facial ou oculaire, opération du cerveau ou opération de l’œil avec pénétration oculaire ;
- maladie respiratoire chronique sévère, difficulté à respirer au repos ou pneumothorax non résorbé ;
- drépanocytose ;
- trouble psychotique, sauf s’il est totalement maîtrisé.
La liste ci-dessus n’est pas exhaustive et l’aptitude à voyager doit être décidée au cas par cas. Un avis médical est indispensable.
Par ailleurs, il ne faut pas voyager en avion dans les 24 h qui suivent une plongée avec bouteille.
- Prévention des effets du décalage horaire
Quelques mesures hygiéno-diététiques peuvent atténuer les effets du décalage horaire 19.
Dans les jours précédant l’arrivée, si c’est possible, il faut décaler l’heure du coucher dans le même sens que celle de la destination d’arrivée. Pendant le voyage en avion, mieux vaut de ne pas boire alcools, diurétiques ou caféine, et profiter du vol pour faire une sieste si le vol se fait vers l’ouest. Après l’arrivée, faire une courte sieste (20-30 minutes) ; s’exposer à la lumière.
La mélatonine aide à resynchroniser le rythme veille/sommeil avec le cycle jour/nuit et est bénéfique dans les situations pathologiques associées aux troubles du rythme circadien. Son usage a ainsi été étendu à la prévention et au traitement du décalage horaire. Dans ce cas, elle est prise les jours suivant l'arrivée, dans la matinée pour les vols vers l’ouest et au coucher pour les vols vers l’est. Les doses habituellement utilisées vont de 0,5 à 2 mg/j. Les doses supérieures à 5 mg sont associées à un effet hypnotique 20.
Néanmoins, le HCSP ne recommande pas l’utilisation de mélatonine pour corriger les effets du décalage horaire.
5.3 Transports maritimes
Les problèmes de santé les plus fréquents sont le mal de mer, les infections respiratoires, les traumatismes et les affections gastro-intestinales.
Il est indispensable que les passagers prévoient un stock de fournitures médicales suffisant pour les longues périodes passées loin de leur domicile, en particulier pour les séjours passés en mer. Les médicaments délivrés sur ordonnance doivent être transportés dans leur emballage ou récipient d’origine, accompagnés d’une lettre d’un médecin certifiant que le passager en a besoin.
Les situations de confinement liées à la vie à bord et la multiplication des escales favorisent l’éclosion d’épidémies parmi les passagers et les membres d’équipage, pouvant toucher un pourcentage important d’entre eux.
Il convient de recommander aux voyageurs maritimes ainsi qu’aux personnels des compagnies maritimes, en plus des vaccinations liées aux conditions épidémiologiques des pays visités, de se vacciner contre les maladies à potentiel épidémique, notamment la grippe et l’hépatite A.
5.4 Mal des transports
Le mal des transports est plus fréquent en bateau mais peut aussi se voir en voiture et dans les autres modes de transports. Les enfants âgés de 2 à 12 ans sont plus à risque de mal des transports que les nourrissons, les adolescents ou les adultes. Les antécédents de migraine sont un facteur favorisant.
En prévention, les antihistaminiques de première génération (sédatifs) (dimenhydrinate, chlorphéniramine) peuvent être utilisés. La scopolamine est plus adaptée mais elle calme les nausées et pas les vomissements, elle a des contre-indications chez l’adulte et n’est pas bien évaluée en pédiatrie. Le gingembre peut être efficace dans les nausées et vomissements.
6. Environnement
6.1 Excursions et randonnées en altitude (supérieure à 2 500 mètres)
Les excursions et randonnées en altitude doivent faire l’objet d’un avis médical spécialisé avant le départ. La haute altitude est déconseillée pour les enfants âgés de moins de 7 ans.
6.1.1 Risques
Les troubles observés à haute altitude sont liés à l’hypoxie, consécutive à la baisse de pression partielle en oxygène. Ils surviennent d’autant plus fréquemment que l’ascension est plus rapide, d’où la règle à respecter : « ne pas monter trop vite, trop haut ». Il faut quelques jours à l’organisme pour s’adapter à ces conditions environnementales particulières ; un défaut d’acclimatation se traduira par le mal aigu des montagnes, dont les manifestations sont des céphalées, une insomnie, une anorexie, des nausées, des œdèmes. Avant 3 ans les signes sont plus frustes : irritabilité, anorexie, apathie, insomnie. Cet état peut évoluer vers deux complications graves mettant en jeu le pronostic vital : l’œdème pulmonaire et l’œdème cérébral de haute altitude.
6.1.2 Prévention
La prévention repose sur une ascension progressive et une adaptation à l’altitude de quelques jours, au repos. Le traitement préventif du mal d’altitude est possible ; il est à commencer 2 jours avant l’arrivée en haute altitude et à poursuivre pendant 2 jours après avoir atteint le point culminant. Plusieurs médicaments peuvent être recommandés : acétazolamide, administré en deux prises quotidiennes de 125 mg (chez l’enfant, 2,5 à 5 mg/kg/j en 2 prises, maximum 125 mg/prise) en l’absence de contre-indications aux sulfamides, ou dexaméthasone (4 mg deux fois par jour), voire, hors AMM, en particulier pour la prévention de l’œdème pulmonaire, la nifédipine 21.
En cas de mal d’altitude, le premier geste à faire (dans la mesure du possible) est de redescendre le plus rapidement possible à une altitude inférieure.
6.2 Plongée sous-marine avec bouteilles
La pratique de la plongée sous-marine avec bouteilles, programmée ou possible, doit faire l’objet d’un avis médical spécialisé avant le départ.
Il est recommandé d’informer les personnes désirant pratiquer la plongée sous-marine avec bouteilles de ne pas plonger 24 heures avant un voyage en avion ou un séjour en altitude. Le principal risque encouru est la survenue d’une embolie gazeuse.
6.3 Baignades
Quel que soit le lieu de baignade, il existe des risques d’hydrocution et de contracter certaines maladies telles que des gastro-entérites (risque féco-oral), des dermatites, des otites, des conjonctivites ou des infections respiratoires.
Il existe, de plus, des risques propres à chaque situation de baignade.
En mer, ces risques sont de deux sortes :
- noyade due aux courants violents ;
- envenimation par contact avec des méduses, des poissons venimeux (poisson-pierre…) ou des coraux.
La situation est aggravée dans les pays en développement, en l’absence de surveillance des plages et de moyens de secours. Il convient donc de se renseigner localement, de respecter strictement les consignes de sécurité lorsqu’elles existent et d’éviter les baignades à partir de plages désertes.
Dans des piscines : dans de nombreux pays il n’existe pas de norme pour l’utilisation des piscines et notamment pas de dispositifs permettant d’interdire l’accès à de jeunes enfants non accompagnés, ou pas de dispositifs d’alarme en cas de chute dans l’eau. Pour éviter la noyade de jeunes enfants, la vigilance parentale est essentielle.
Dans des spas : leur utilisation est associée au risque de transmission de légionellose et d’infections cutanées à bacille pyocyanique.
En eau douce, les baignades exposent à des infections transmises par voie cutanée comme la leptospirose, la bilharziose, ou dans une moindre mesure la naegleriose (infection par des amibes libres).
6.4 Exposition à la chaleur
6.4.1 Risques
Le coup de chaleur est la conséquence d’une élévation de la température corporelle centrale dans des conditions climatiques particulières (température extérieure élevée, hygrométrie élevée). Il se traduit par une hyperthermie, d’abord accompagnée de sudation puis sèche, sans sudation, associée à un épuisement. Il se complique de troubles de la conscience et de déshydratation. Le pronostic vital peut être engagé : c’est une urgence médicale. Les nourrissons, les jeunes enfants et les personnes âgées sont particulièrement à risque.
La déshydration secondaire à l’exposition à la chaleur peut favoriser la survenue d’autres manifestations telles que les coliques néphrétiques par exemple.
6.4.2 Prévention
Les mesures suivantes permettent de prévenir le coup de chaleur :
- éviter de s’exposer au soleil ;
- bien s’hydrater (boire souvent, prendre des douches…) ;
- préférer les lieux ventilés, voire climatisés ;
- limiter les activités physiques ;
- éviter les voyages prolongés en situation de confinement.
L’acclimatation aide également à préparer le corps à la chaleur extrême : il suffit de s’exposer à la chaleur de façon progressive et d’éviter les efforts physiques les premiers jours.
6.5 Exposition au soleil
Il convient d’informer les voyageurs des risques liés au soleil et de rappeler que l’utilisation d’écrans solaires n’autorise pas pour autant une surexposition au soleil.
6.5.1 Risques
Les effets délétères du soleil sont dus aux radiations solaires, dont les UVA et UVB. Les UVB sont principalement responsables de l’érythème solaire, des coups de soleil et des carcinomes spinocellulaires. Les autres effets indésirables des radiations UV sont le veillissement cutané accéléré, les réactions allergiques, la kératose actinique (considérée comme une lésion pré-cancéreuse), le carcinome basocelullaire et le mélanome.
Les voyageurs les plus exposés aux complications de l’ensoleillement excessif sont les enfants, les personnes aux phototypes clairs (roux, blonds, châtains), les patients prenant des médicaments photosensibilisants et les personnes immunodéprimées.
La doxycycline, conseillée en traitement préventif du paludisme, est photosensibilisante. Le risque exact, à doses préventives, est inconnu mais il est recommandé, pour diminuer ce risque, de prendre le médicament le soir au dîner.
Il existe également des conséquences au niveau ophtalmologique (ophtalmie des neiges). L’ophtalmie des neiges ou photokératite est due à l’exposition des yeux aux rayons ultraviolets en altitude ou en milieu polaire, l’intensité des UV augmentant de 10 à 12% par 1 000 mètres d’altitude et la neige réfléchissant jusqu’à 80% des rayons UV. La kératite est souvent accompagnée de conjonctivite. Elle peut aller jusqu’à la cécité, mais celle-ci est transitoire. La prévention repose sur le port de lunettes à verres larges et à forte absorption des UV pendant toute la durée de l’exposition, même un jour nuageux.
6.5.2 Prévention
Les mesures recommandées pour se protéger du soleil sont :
- éviter les périodes les plus lumineuses (entre 12h et 16h) ;
- porter des vêtements couvrants (voire photoprotecteurs) ;
- porter des lunettes de soleil, à verres filtrants (norme CE, de préférence CE3 ou CE4) et un chapeau à larges bords protégeant les yeux et le visage ;
- utiliser un écran solaire adapté à son phototype (de roux à noir) à appliquer régulièrement. Un écran solaire appliqué correctement (2 mg/cm2 de peau exposée) filtrera 93% des rayons UVB, pour un indice de protection solaire de 15, et 98% des UVB pour un indice de 50 22. Appliquer le répulsif après l’écran solaire (Cf. chapitre 2 Paludisme)
6.6 Exposition au grand froid
Le grand froid peut mettre en danger les personnes fragilisées, notamment les personnes âgées, les enfants, les personnes handicapées, les personnes atteintes de certaines pathologies chroniques ou de certaines pathologies spécifiques.
6.6.1 Risques
Les gelures sont fréquentes. Les symptômes de l’hypothermie sont progressifs : chair de poule, frissons, engourdissement des extrémités sont des signaux d’alarme. En cas de persistance ils peuvent nécessiter une aide médicale.
6.6.2 Prévention
Les mesures à prendre pour prévenir les risques liés à l’exposition au grand froid sont les suivantes :
- éviter les expositions prolongées au froid et au vent ;
- s’habiller chaudement, de plusieurs couches de vêtements, avec une couche extérieure imperméable au vent et à l’eau, se couvrir la tête, les mains et les pieds, ne pas garder de vêtements humides ;
- éviter les efforts brusques.
Concernant les enfants, une vigilance accrue doit être exercée car ils présentent plusieurs facteurs de moindre résistance au froid 23.
6.7 Pratiques sportives
Les risques liés à la pratique du sport sont augmentés en raison de la fatigue du voyage, du décalage horaire, des conditions climatiques, du possible manque d’entrainement, du manque d’encadrement, d’une mauvaise appréciation du risque et des difficultés d’accès à une prise en charge adéquate en cas d’accident.
6.8 Animaux autres que les arthropodes
À l’exception des animaux répondant aux conditions réglementaires d’importation (espèces dont le commerce est autorisé, statut sanitaire et vaccinal faisant l’objet d’un certificat officiel), l’importation d’animaux domestiques ou sauvages est strictement interdite et peut donner lieu à des sanctions pénales et financières lourdes (7).
6.8.1 Animaux venimeux
Les animaux venimeux (serpents, autres reptiles, batraciens, poissons, coquillages) provoquent des envenimations ou des intoxications.
Il est recommandé de ne pas toucher ces animaux. Comme pour les arthropodes venimeux, toute piqûre ou morsure qui entraîne des troubles importants nécessite une visite au service des urgences le plus proche.
6.8.2 Mammifères et oiseaux
Les lésions causées par morsure ou coup de bec sont les dommages les plus importants causés par les mammifères et les oiseaux, mais de nombreuses zoonoses peuvent également être transmises à l’être humain. Certaines sont graves, voire mortelles.
La règle générale est de ne pas approcher les animaux, même familiers, même jeunes, même morts, de ne pas les caresser et de consulter rapidement en cas de morsure, de griffure ou de léchage sur une peau lésée ou une muqueuse.
Dans ce cas, il est important de laver la plaie ou la zone léchée à l’eau et au savon, d’appliquer un antiseptique, puis de contacter les structures médicales locales qui prendront si besoin des mesures de prophylaxie post-exposition.
En ce qui concerne la rage, le chien est le principal réservoir du virus dans les pays en développement, mais tous les mammifères peuvent être atteints, notamment les chauves-souris et les singes. Le virus est présent dans la salive de l’animal infecté, qui peut le transmettre par morsure ou léchage, sans présenter encore les symptômes de la maladie : il est donc contaminant avant d’être malade.
Il existe un vaccin contre la rage (Cf. chapitre 1, § 1.10).
Il est strictement interdit de rapporter en France des animaux, en particulier des chiens, dont le statut sanitaire et vaccinal n’a pas fait l’objet d’un certificat officiel.
6.9 Hygiène corporelle
Une bonne hygiène corporelle est importante : se laver régulièrement à l’eau et au savon et bien se sécher. Apporter un soin particulier en cas de plaie ou de blessure cutanée :
- laver, couvrir, ne pas laisser macérer ;
- ne pas marcher pieds nus sur les plages. Ne pas s’allonger à même le sable (risque de Larva migrans cutanée ankylostomienne) ;
- porter des chaussures fermées sur les sols boueux ou humides (risque d’anguillulose, d’ankylostomose, etc.) ;
- ne pas marcher ou se baigner dans les eaux douces (risque de bilharziose, de leptospirose, etc.) ;
- éviter l’ensoleillement excessif et se protéger du soleil (ombre, lunettes de soleil, chapeaux, vêtements longs et légers, crème écran d’indice de protection UV élevé dont l’application doit être renouvelée régulièrement), même pendant les baignades ;
- porter un habillement léger, lavable aisément, perméable (coton et tissus non synthétiques) ;
- éviter de laisser sécher le linge à l’extérieur ou sur le sol (risque de myiase), à défaut le repasser des deux côtés ;
- éviter les contacts avec les animaux (être particulièrement vigilant avec les enfants).
7. Risques liés à certains comportements
7.1 Risques liés aux comportements sexuels
Les infections sexuellement transmissibles (IST) sont cosmopolites, et le voyage peut induire des comportements à risque.
Certaines IST engagent le pronostic vital (VIH, hépatite B) et ne bénéficient pas de traitement curatif radical, d’autres sont curables mais hautement contagieuses ou présentant des risques de complications (syphilis, gonococcie, herpès, chlamydioses, papillomaviroses).
L’usage du préservatif masculin ou féminin est le principal moyen de prévention contre les IST.
Pour l’hépatite B, la vaccination constitue la meilleure protection.
Pour les infections à certains papillomavirus humains (HPV) oncogènes, la vaccination constitue une protection efficace lorsqu’elle est effectuée dans les tranches d’âge recommandées dans le calendrier vaccinal en vigueur.
Il faut conseiller aux voyageurs ayant eu des conduites sexuelles à risque de consulter au plus tôt, dans les 24 heures suivantes, pour un éventuel traitement post-exposition notamment pour le VIH, dans leur intérêt et celui de leurs partenaires actuels et futurs. Dans ce cas, une consultation de dépistage des IST peut être également conseillée.
7.2 Risques liés aux soins
Le développement du tourisme médical (soins dentaires, chirurgie froide, chirurgie plastique) partout dans le monde expose ceux qui le pratiquent à des risques particuliers.
7.2.1 Risques liés à des injections ou des actes invasifs
Dans la plupart des pays aux structures sanitaires insuffisantes, les transfusions sanguines représentent un risque majeur de transmission par le sang d’agents pathogènes, notamment les virus des hépatites B et C, et le virus de l’immunodéficience humaine (VIH).
Les soins médicaux avec injection intraveineuse (IV), intramusculaire (IM) et sous-cutanée (SC), incision, endoscopie, acupuncture, mésothérapie exposent également à des risques infectieux.
Afin de limiter ces risques :
- refuser tout geste pour lequel il n’est pas sûr qu’il sera effectué avec du matériel neuf à usage unique (aiguilles, seringues, aiguilles d’acupuncture, ventouses scarifiées) ou soumis préalablement à une stérilisation appropriée ;
- se munir avant le départ, si besoin, de matériel (seringues, aiguilles) à usage unique.
Le personnel médical et paramédical en mission dans un pays à prévalence élevée d’infection à VIH doit pouvoir, en cas d’accident d’exposition au sang, bénéficier d’un traitement anti-rétroviral au mieux dans les quatre heures, et au plus tard dans les 48 heures, après conseil médical spécialisé.
7.2.2 Risques liés à une hospitalisation
Les infections nosocomiales sont particulièrement fréquentes dans les pays en développement et les bactéries en cause sont souvent multirésistantes : staphylocoques dorés résistant à la méticilline et sécréteurs de la toxine de Panton-Valentine, entérobactéries sécrétrices de bêta-lactamases à spectre étendu, tuberculose MDR (multirésistante) et XDR (ultra-résistante), entérobactéries sécrétrices de carbapénémases, Acinetobacter baumanii résistant à l’imipénème, Pseudomonas aeruginosa multi-résistant et mycobactéries environnementales.
Tout patient rapatrié sanitaire ou ayant été hospitalisé à l’étranger au cours de l’année précédente doit subir, lors d’une d’hospitalisation en France, un écouvillonnage rectal à la recherche du portage d’une bactérie multirésistante et être éventuellement isolé 24.
7.3 Risques liés aux pratiques de tatouages et de piercing
La pratique de tatouages et de piercing (dont le perçage des oreilles) représente un risque majeur de transmission par le sang d’agents pathogènes, notamment les virus des hépatites B et C et le virus de l’immunodéficience humaine (VIH). Ils exposent aussi au risque d’infections par des mycobactéries environnementales. Les tatouages éphémères noirs à base de henné exposent à des risques d’eczéma de contact (eczéma allergique) 25.
Il est important de déconseiller le recours à ces pratiques.
7.4 Risques liés aux drogues
L’usage de drogues au cours d’un voyage expose à un certain nombre de risques parfois mortels : risque infectieux, risque juridique (législation locale), troubles du comportement pouvant favoriser des prises de risque (accident, relations sexuelles, noyade…), intoxications ou surdosages (par consommation de produits de composition qualitative ou quantitative variable).
8. Précautions en fonction des personnes
Plusieurs risques liés au voyage sont exacerbés dans certaines catégories de population du fait :
- de la diminution des capacités d’adaptation physiologique à une situation aiguë ;
- des difficultés de récupération après un effort ;
- de la sensibilité à la déshydratation.
En ce qui concerne les vaccinations, la prévention du paludisme, la prévention et la prise en charge des diarrhées il faut se reporter aux chapitres 1, 2 et 4), et pour les précautions générales se reporter aux chapitres 5 et 6.
8.1 Enfants
Une vigilance accrue doit être exercée sur :
- l’exposition au soleil et à des températures élevées :
- protéger l’enfant du soleil (crèmes à coefficient de protection élevé à renouveler fréquemment et après chaque baignade, chapeau à larges bords, vêtements longs, légers, en coton, port d’un T-shirt pour les activités aquatiques) ;
- éviter les déplacements trop longs en pays très chauds, sources de déshydratation et de coup de chaleur (cf. § 6.4) ;
- donner souvent à boire à l’enfant de l’eau ou des solutés de réhydratation orale ;
- porter des vêtements légers, lavables aisément, perméables (coton et tissus non synthétiques), afin d’éviter le risque de sudamina (bourbouille) ;
- l’exposition au grand froid, les enfants présentant plusieurs facteurs de moindre résistance au froid 23 :
- habiller chaudement, de plusieurs couches de vêtements avec une couche extérieure imperméable au vent et à l’eau ;
- couvrir chaudement la tête, les mains et les pieds ;
Le volume céphalique proportionnellement plus important chez l’enfant, peut représenter une source importante de perte de chaleur en l’absence de protection. Les gelures chez l’enfant entraînent un risque spécifique de troubles de croissance et de déformations ultérieures par destruction des épiphyses ou des cartilages de croissance 26 ; - proscrire les porte-bébés par temps froid car l’immobilité de l’enfant favorise l’hypothermie et le portage favorise les compressions des membres, sources de gelures.
- le danger des transports en voiture ; appliquer les mesures de sécurité (ceinture, siège-auto, enfant placé à l’arrière) dans toute la mesure du possible ;
- le risque de noyade, en l’absence fréquente de dispositif de sécurité (Cf. § 6.3) ;
- les contacts avec les animaux ;
- une hygiène corporelle rigoureuse notamment pour le jeune enfant, comprenant une douche quotidienne (avec savonnage), terminée par un séchage soigneux des plis ;
- les risques d’accidents domestiques, notamment pour les enfants qui retournent pour les vacances dans le pays d’origine de leur famille. Les parents doivent être sensibilisés particulièrement au risque de brûlure par chute dans un foyer posé à même le sol, et à celui d’ingestion de produits pétroliers ou caustiques, de pesticides déconditionnés ou stockés à portée des enfants.
Un voyage avec de très jeunes nourrissons, dans les pays tropicaux, dans des conditions précaires est à déconseiller.
8.2. Femmes enceintes
Une vigilance accrue doit être exercée sur :
- le voyage en avion et notamment le risque particulier de thrombophlébite (cf. § 5.2). Les longs voyages aériens sont déconseillés en fin de grossesse. La plupart des compagnies aériennes refusent les femmes enceintes au-delà du 7e mois de grossesse, certaines à partir du 6e mois ;
- les longs voyages en voiture (état des routes, pistes …) ;
- les activités physiques inadaptées (trekking, plongée…) ;
- le risque de contracter une hépatite E, plus grave chez la femme enceinte, nécessite donc de respecter scrupuleusement les précautions d’hygiène alimentaire.
Un avis de l’obstétricien est recommandé avant le départ.
8.3. Personnes âgées
L’âge en tant que tel n’est pas une contre-indication aux voyages. Compte tenu de l’augmentation nette des pathologies chroniques au-delà de 65 ans et des risques liés au voyage, une consultation médicale est recommandée avant le départ afin de faire le point sur la compatibilité entre l’état de santé et le type de voyage.
Une vigilance accrue doit être exercée sur :
- l’existence de pathologies chroniques plus fréquentes ;
- la diminution des capacités d’adaptation physiologique ;
- la sensibilité à une déshydratation ;
- lors de voyages exposant à de fortes chaleurs (Cf. § 6.4) ;
- lors de voyages exposant à des grands froids (Cf. § 6.6).
8.4. Personnes atteintes d’affections chroniques
Une vigilance accrue doit être exercée sur :
- la compatibilité de l’état de santé avec le type de voyage prévu, en particulier en présence de troubles cognitifs ou locomoteurs ;
- le risque de décompensation de co-morbidités (insuffisance cardiaque ou respiratoire, diabète, épilepsie, maladies neurodégénératives, etc.) ;
- le risque lié à certains traitements selon les conditions du voyage (par ex. : diurétique et chaleur, etc.) ;
- le risque d’interaction du traitement au long cours avec de nouveaux médicaments prescrits pour le voyage ;
- l’exposition à de fortes chaleurs (Cf. § 6.4) ;
- l’exposition à des grands froids (Cf. § 6.6).
Une consultation médicale avant le départ est nécessaire afin de faire le point sur :
- les maladies chroniques ;
- les traitements suivis ;
- les contre-indications éventuelles à certaines vaccinations ;
- la constitution d’un dossier médical de voyage (Cf. § 10.2) ;
- les conditions du voyage, en particulier en cas de voyage aérien (Cf. § 5.2).
8.5 Personnes vivant avec le VIH et personnes immunodéprimées
Les personnes pour lesquelles une consultation spécialisée est justifiée avant le départ sont notamment les personnes :
- vivant avec le VIH ;
- hypospléniques ou aspléniques ;
- transplantées d’organe solide ;
- greffées de cellules souches hématopoïétiques ;
- sous chimiothérapie pour tumeur solide ou hémopathie maligne ;
- traitées par immuno-suppresseurs, biothérapie et/ou corticothérapie pour une maladie auto-immune ou inflammatoire chronique ;
- présentant un déficit immunitaire congénital.
Une vigilance accrue doit être exercée sur :
- le risque lié à certaines maladies infectieuses chez le sujet porteur du VIH (leishmanioses, salmonelloses, tuberculose, infections dues à des coccidies intestinales, histoplasmoses et les autres infections fongiques contractées par inhalation, etc.) ;
- la nécessité de précautions d’hygiène notamment alimentaire ;
- les vaccinations (cf. chapitre 1) ; les recommandations doivent être adaptées en fonction des types d’immunodépression. Un avis de juillet 2012 du HCSP les formalise.
- Les vaccins vivants atténués tel que le vaccin de la fièvre jaune, sont généralement contre-indiqués (Cf. Tableau 4). Chez le patient vivant avec le VIH, un nombre de CD4 >200 / mm3 (>15% chez l’enfant âgé de moins de 5 ans) autorise la vaccination contre la fièvre jaune, mais le délai d’acquisition de l’immunité post-vaccinale semble augmenté et la durée de protection peut être inférieure à 10 ans.
- Chez ces patients, le BCG est par ailleurs contre-indiqué quels que soient l’âge et le taux de CD4.
- Les vaccins inactivés sont recommandés comme à l’ensemble des voyageurs 27.
- les interactions médicamenteuses entre le traitement de fond et les médicaments prescrits pour le voyage et notamment la prescription des antipaludiques :
- diminution de la concentration plasmatique de l’indinavir par l’atovaquone ;
- diminution des concentrations plasmatiques d’atovaquone et de proguanil par l’efavirenz, les associations lopinavir/ritonavir et atazanavir/ritonavir avec donc un risque d’échec des prophylaxies antipaludiques correspondantes dans ces situations 28 ;
- les personnes vivant avec le VIH, le paludisme augmentant la charge virale et donc le risque de progression de la maladie ;
- le risque de photosensibilisation provoqué par les sulfamides souvent utilisés par les personnes infectées vivant avec le VIH. Une protection solaire (vêtements et crèmes écran) est fortement recommandée ;
- l’exposition au soleil (Cf. § 6.5), les personnes immunodéprimées étant plus à risque de cancer de la peau.
8.6 Personnes se rendant à un grand rassemblement type pèlerinage en Arabie saoudite (Hadj et Umra)
Aux risques habituels liés à la destination s’ajoutent les risques liés à la foule : bousculades, piétinement, transmission accrue de maladies infectieuses, surtout si les participants internationaux sont nombreux.
Les conséquences constatées le plus fréquemment lors des grands rassemblements sont les traumatismes, les problèmes cardiaques et respiratoires, les pathologies liées à la chaleur et les pathologies gastro-intestinales.
Les règles de prévention s’appliquent à tous les grands rassemblements en France ou à l’étranger (pèlerinages, Journées mondiales de la jeunesse (JMJ), Kumbhamellas…)
Les pèlerinages en Arabie saoudite peuvent plus particulièrement présenter des risques du fait :
- de la fréquentation souvent très élevée, notamment pour le Hadj avec plusieurs millions de pèlerins, qui favorise promiscuité et confinement dans un espace géographique limité ; de l’âge élevé et de l’état de santé des pèlerins (polypathologies) ;
- des conditions climatiques en Arabie saoudite, surtout lorsque le pèlerinage se déroule pendant les mois d’été ;
- des contraintes imposées par le rituel, qui entraînent une fatigue pouvant aller jusqu’à l’épuisement.
8.6.1 Mesures préventives d’ordre général
Une vigilance accrue doit être exercée pour :
- les infections les plus fréquentes rencontrées pendant ces voyages : infections respiratoires ubiquitaires ou spécifiques (méningite, grippe, MERS-CoV, pour le Hadj), infections gastro-intestinales ;
- les pathologies en rapport avec la chaleur ;
- les traumatismes possibles ;
- l’épuisement ;
- la décompensation d’affections chroniques pré-existantes (maladies cardio-vasculaires, diabète, HTA, etc.) (Cf. § 8.4).
Une information sur ces risques doit être donnée aux voyageurs avant leur départ, ainsi que sur les moyens de s’en prémunir :
- hygiène des mains et hygiène alimentaire (Cf. chapitre 4) ;
- hydratation correcte ;
- protections contre la chaleur et protection solaire ;
- risques traumatiques.
8.6.2 Vaccinations
Vaccinations obligatoires
- La vaccination contre les infections invasives à méningocoques avec un vaccin tétravalent A,C,Y,W135 est obligatoire pour l’obtention des visas pour le pèlerinage en Arabie saoudite. Les vaccins méningococciques monovalent C et bivalent A+C ne répondent pas à cette obligation.
- Elle doit être réalisée au moins 10 jours avant le départ.
- D’autres vaccinations sont exigées pour l’obtention des visas, pour les pèlerins en transit en provenance de pays où existe un risque de transmission de poliomyélite ou de fièvre jaune. Les dispositions et recommandations sanitaires pour l’obtention des visas sont publiées chaque année par l’OMS dans un Relevé épidémiologique hebdomadaire : « Dispositions sanitaires pour les voyageurs se rendant en Arabie saoudite pour le pèlerinage de la Mecque (Hadj) » http://www.who.int/wer/fr/
Vaccinations recommandées
- La mise à jour des vaccinations du calendrier vaccinal (notamment les vaccinations contre la diphtérie, le tétanos, la poliomyélite, la coqueluche et la rougeole) ainsi que la vaccination contre la grippe (si le pèlerinage a lieu pendant une période de circulation d’un virus de la grippe) et celle contre l’hépatite A sont recommandées pour tous les grands rassemblements.
- La vaccination contre les infections à pneumocoques est également recommandée aux pèlerins à risque (âgés de 60 ans et plus, souffrant d’insuffisance respiratoire...).
8.7 Militaires
Les recommandations sanitaires pour les militaires s’appuient principalement sur les recommandations sanitaires pour les voyageurs. Cependant, lors des missions en dehors de la France métropolitaine, les militaires sont soumis à des risques sanitaires particuliers et peuvent également, en cours de mission, être déployés dans d’autres pays que ceux prévus initialement.
Par ailleurs, au-delà de la santé individuelle des militaires, les armées ont aussi une contrainte de protection collective dans un objectif de maintien de la capacité opérationnelle des forces déployées.
Ceci explique pourquoi, dans certains domaines comme la chimioprophylaxie du paludisme ou les vaccinations par exemple, les recommandations spécifiques faites aux militaires sont d’un niveau de protection plus élevé que les recommandations sanitaires pour les voyageurs. Ainsi, les militaires français sont soumis à un calendrier vaccinal spécifique, réévalué chaque année pour tenir compte de l’évolution des recommandations nationales, de l’évolution du contexte épidémiologique et des contraintes spécifiques liées à leur métier. De la même façon, la prescription de la chimioprophylaxie antipaludique est encadrée par une circulaire du ministère de la Défense actualisée chaque année.
En particulier, pour toute mission hors métropole, les militaires doivent être à jour des vaccinations contre la fièvre jaune, les méningites à méningocoque, la fièvre typhoïde et la grippe. Ils peuvent également être tenus de prendre une chimioprophylaxie même dans des zones de faible niveau de transmission du paludisme.
Les recommandations pour les personnes accompagnant les militaires sont celles préconisées en population générale, notamment celles concernant les vaccinations et la protection contre le paludisme.
9. Trousse à pharmacie
Il n’existe pas de trousse de pharmacie type. Sa composition est à adapter en fonction du voyage. Les médicaments doivent être emportés dans leur emballage et non pas en vrac (gain de place dans les bagages mais source possible d’erreurs).
La trousse à pharmacie pourrait comporter notamment :
• Des médicaments systémiques :
- antalgique et antipyrétique (le paracétamol est préférable) ;
- antibiotique (cf. encadré ci-après) ;
- sels de réhydratation, antidiarrhéique antisécrétoire éventuellement (cf. chapitre 4) ;
- antiémétique si nécessaire (pour le mal des transports) ;
- antihistaminiques dernière génération (anti H1).
• Une protection contre le paludisme :
- répulsif contre les moustiques (Cf. Tableau 11) ;
- produit pour imprégner les moustiquaires et les vêtements (Cf. Tableau 10) ;
- antipaludique à usage préventif.
• D’autres produits :
- collyre antiseptique (conditionnement monodose) ;
- crème pour les brûlures ;
- pansements stériles et sutures adhésives ;
- antiseptique cutané ;
- dosettes de sérum physiologique (unidose) ;
- crème écran solaire (indice de protection maximal) ;
- bande de contention ;
- gel ou solution hydro-alcoolique pour l’hygiène des mains ;
- thermomètre incassable ;
- pince à épiler ;
- préservatifs (norme NF).
Cas particuliers
• Pour l’enfant
La trousse à pharmacie doit comporter :
- les mêmes médicaments (présentés sous leur forme pédiatrique) avec leur mode d’utilisation ;
- les produits suivants supplémentaires :
- crème solaire ayant un indice élevé de protection (IP 50+) ;
- sachets de réhydratation type OMS (Unicef) ;
- il convient d’éviter les suppositoires.
• Pour le voyageur atteint d’une ou plusieurs maladies chroniques
La trousse à pharmacie doit associer, en plus des traitements liés au voyage :
- le traitement des pathologies chroniques en quantité suffisante ;
- le matériel d’injection si nécessaire (diabétiques) avec un certificat médical.
Il est souhaitable que le voyageur dispose de la totalité de son traitement pour le séjour, voire plus en cas de retard au retour ou de perte. Pour des séjours de longue durée (3-6 mois), une autorisation de délivrance doit être demandée à l’Assurance maladie.
Il est préférable que les médicaments voyagent dans le bagage à main en cabine, du fait du risque d’égarement ou de retard des bagages en soute. Il faut pouvoir disposer des ordonnances (rédigées avec la dénomination commune internationale) pour les contrôles et un éventuel achat sur place.
Les formes liquides ou suppositoires ne sont pas préconisées. Les traitements qui requièrent des seringues, aiguilles ou stylos injecteurs peuvent être acceptés en cabine avec un certificat en anglais précisant le caractère indispensable des injections. Certains médicaments doivent être gardés à basse température et voyager en conditionnement isotherme (se renseigner auprès des compagnies aériennes).
La fréquence des médicaments contrefaits dans beaucoup de pays exotiques doit inciter à la plus grande prudence quant à l’utilisation de médicaments achetés sur place.
• Pour les voyages à risque particulier
Proposer une trousse à pharmacie sur mesure comprenant notamment, en sus des propositions ci-dessus :
- antipaludique à usage présomptif si nécessaire (cf. chapitre 2 Paludisme) ;
- produit pour désinfection de l’eau de boisson ;
- gouttes auriculaires antibiotiques (si risque d’otite externe) par exemple en cas de baignade ;
- set de matériel à usage unique (aiguilles, seringues, matériel à suture, etc.) (avec un certificat bilingue français/anglais à l’intention des contrôles douaniers).
Antibiotiques
Dans le contexte croissant de l’antibiorésistance pour des germes communs ou des pathologies du voyage, il paraît important de ne délivrer des antibiotiques qu’en formulant certaines recommandations : ils doivent être utilisés en cas d’accès aux soins limité, et toute antibiothérapie nécessite un diagnostic médical. Les modalités de prise de l’antibiotique (posologie, durée, conditions d’arrêt) et le contexte (diagnostic possible) de la mise en route de l’antibiothérapie doivent être explicités.
Le choix d’un antibiotique, si jugé nécessaire, doit s’établir sur plusieurs critères :
- lieu et durée de voyage ;
- accessibilité aux soins ;
- antécédents personnels de l’individu ;
- site potentiel d’infection selon les susceptibilités individuelles et les risques encourus.
Il est recommandé de se référer aux règles de bon usage des antibiotiques.
10. Aspects administratifs
Des renseignements sur chaque pays, notamment d’ordre sanitaire (épidémie, médecins, hôpitaux et cliniques identifiés par l’ambassade de France dans le pays) sont fournis sur les sites du ministère des Affaires étrangères et du Cimed :
10.1 Prise en charge médicale, assistance et rapatriement
Il est indispensable de vérifier la couverture et la validité de son contrat d’assistance et de son assurance maladie avant le départ.
Il est possible de s’inscrire sur l’application Ariane du Ministère des Affaires étrangères qui propose de recevoir des alertes sécuritaires et sanitaires par SMS ou par courriel : http://www.diplomatie.gouv.fr/fr/conseils-aux-voyageurs/infos-pratiques-20973/preparer-son-depart-20975/ariane
10.1.1 Assurance maladie
Pour les séjours au sein de l’Union européenne (UE), de l’Espace économique européen (EEE) ou de la Suisse, la Carte européenne d’Assurance maladie peut être obtenue par Internet ou auprès de sa caisse d’assurance maladie.
Pour les séjours hors pays de l’UE :
- Pour les séjours inférieurs à six mois, il est recommandé de contracter un contrat d’assurance couvrant les frais médicaux non pris en charge par l’Assurance maladie française.
- Pour les séjours dépassant six mois effectifs, il est indispensable de contracter un contrat d’assurance maladie auprès de la Caisse des français de l’étranger ou d’un assureur privé.
Les renseignements sur les démarches et les documents nécessaires pour avoir une assurance maladie lors des voyages se trouvent sur le site de l’Assurance maladie, que ce soit pour les voyages en Europe ou hors d’Europe :
- http://www.ameli.fr/assures/droits-et-demarches/a-l-etranger/index.php
- http://www.diplomatie.gouv.fr/fr/conseils-aux-voyageurs
10.1.2 Assistance rapatriement
L’assistance aux voyageurs est différente de l’assurance maladie (remboursement des soins). Le rapatriement sanitaire est l’une des possibilités offerte par un contrat d’assistance.
Pour les séjours supérieurs à trois mois effectifs, il est recommandé de souscrire un contrat d’assistance spécifique.
Pour les séjours inférieurs à trois mois, de nombreux contrats d’assistance sont liés aux contrats d’assurances habitations, véhicules, ou liés aux cartes bancaires.
Il existe des informations complémentaires sur le site de la Maison des Français de l’étranger : http://www.mfe.org/index.php
10.1.3 Réserve de médicaments pour long séjour
Une autorisation de délivrance d’un traitement pour six mois dans une pharmacie française peut être demandée auprès de sa caisse d’assurance maladie en cas de maladie chronique (diabète, insuffisance thyroïdienne, etc.).
10.2 Dossier médical
Tout voyageur atteint d’une ou plusieurs maladies chroniques emportera avec lui :
- un compte-rendu médical, traduit dans la langue du pays de destination ou au moins en anglais ;
- les coordonnées d’une structure de santé ou d’un médecin correspondant spécialiste : http://www.diplomatie.gouv.fr/fr/conseils-aux-voyageurs ;
- l’ordonnance pour traitement régulier sous sa dénomination commune internationale ;
- un certificat médical pour le matériel d’injection d’un traitement (diabétiques) ;
- les certificats reconnaissant les maladies chroniques nécessitant un suivi rapproché et les carnets de suivi des traitements chroniques nécessitant une surveillance.
11. Retour de voyage et santé publique : reconnaitre les situations à risque et savoir alerter
En termes de santé publique, il existe un certain nombre de pathologies émergentes, notamment infectieuses, qui nécessitent une attention plus particulière au retour de voyage car elles peuvent diffuser directement ou indirectement dans la population générale et être ainsi introduites sur le territoire français, métropolitain ou ultramarin.
Comment « alerter »
Les pathologies de retour susceptibles de diffuser en France doivent faire l’objet d’un signalement rapide aux Agences régionales de santé (ARS). Dans le cadre des activités de veille et de gestion des alertes sanitaires assurées par les ARS, un dispositif a été mis en place pour réceptionner les alertes et signalements émanant des professionnels de santé, des établissements de santé ou du grand public, pendant et en dehors des heures d’ouverture de l’agence (Cellule de veille, d’alerte et de gestion sanitaire : CVAGS). Chaque ARS dispose d’une ligne téléphonique et de télécopie dédiée ainsi que d’une adresse courriel (http://www.ars.sante.fr/portail.0.html).
11.1 Infections respiratoires émergentes
Les infections respiratoires sont une des trois principales causes de morbidité chez le voyageur et la grippe est considérée comme la plus fréquente des maladies du voyageur pouvant être prévenues par une vaccination. Les infections respiratoires aiguës peuvent être dues à des agents pathogènes nouveaux, l’émergence de nouvelles souches d’agents pathogènes respiratoires déjà connues, des recombinaisons de virus aviaires de type A(H7N9) ou de nouveaux virus comme celui du syndrome respiratoire du Moyen-Orient (Middle East Respiratory Syndrome Coronavirus, MERS-CoV) ou le SRAS, aujourd’hui disparu.
11.1.1 Grippes aviaires
A(H7N9) - Depuis mars 2011, l’OMS rapporte des cas humains d’un virus de la grippe aviaire identifié comme A(H7N9) en Chine. À ce jour, tous les cas ont été signalés dans des régions voisines dans l’est et le sud-est de la Chine. Des cas liés au voyage ont été rapportés à Hong Kong, à Taïwan et en Malaisie. Au 01/04/2015, l’OMS rapporte 631 cas confirmés de A(H7N9), dont 221 décès. D’autres confirmations de cas sont attendues. La plupart des personnes infectées ont développé une pneumonie grave et certaines sont décédées (létalité au 1er avril 2015 : 35%). Il semble que la contamination se fasse lors d’un contact étroit avec des oiseaux infectés (sauvages ou domestiques) qui eux ne présentent pas de signes cliniques apparents.
A(H5N1) - Depuis 2003, l’OMS rapporte des cas humains d’un virus de la grippe aviaire identifié comme A(H5N1). Au 01/04/2015, l’OMS a rapporté 812 cas confirmés de A(H5N1) dont 439 décès (létalité proche de 55%). Fin 2014 et début 2015, de nombreux cas ont été signalés en Egypte. La présence de la souche asiatique du virus de l’influenza aviaire A(H5N1) chez les oiseaux sauvages et chez la volaille a été confirmée dans plusieurs pays en Asie, Europe, Afrique et Moyen-Orient. Les cas humains ont été décrits en Asie et en Afrique. Peu de cas sont signalés chez les voyageurs (le premier cas diagnostiqué sur le continent américain, au Canada, a été décrit chez un voyageur revenant de Chine, fin 2013).
Un contact direct avec la volaille infectée ou des surfaces/objets contaminés par les excréments est présentement considéré comme la principale voie de transmission de l’infection humaine.
Recommandations pour les grippes aviaires
- À ce jour, Il n’y a pas de vaccin disponible pour l’homme, dirigé contre A(H7N9) ni A(H5N1).
- Si vous vous rendez dans une région où il existe un risque de grippe aviaire :
- évitez les endroits à risque élevé, comme les fermes d’élevage de volaille et les marchés d’animaux vivants ;
- évitez tout contact direct avec les oiseaux, notamment les poules, poulets, canards et oiseaux sauvages ;
- évitez les surfaces contaminées par des excréments ou des sécrétions d’oiseaux ;
- observez les règles d’hygiène des mains et d’hygiène alimentaire.
11.1.2 Grippe humaine saisonnière
L’incidence de la grippe 29 a été récemment estimée à 1 pour 100 voyageurs et par mois de séjour à l’étranger. Un grand nombre d’épidémies de grippe ont été observées dans des groupes particuliers de voyageurs : participation à de grands rassemblements ou à de grandes tournées commerciales, fréquentation de foules, voyage à bord de navires de croisière.
La vaccination antigrippale n’est pas pratiquée, à ce jour, chez les voyageurs en dehors de ceux pour lesquels cette mesure est normalement conseillée par le calendrier vaccinal. Cette vaccination semble cependant intéressante à titre individuel et collectif (vaccination altruiste) pour limiter la diffusion des souches grippales et le coût économique engendré par cette affection. Ainsi, la vaccination antigrippale est indiquée chez les personnels de l’industrie des voyages en contact avec des groupes de voyageurs (guides…), le personnel navigant des compagnies aériennes et maritimes, ainsi que pour les voyageurs en groupe ou les pèlerins... Néanmoins, la prévention vaccinale chez le voyageur est rendue compliquée par les problèmes de délivrance du vaccin et l’inadéquation fréquente des souches vaccinales, incluses dans le vaccin disponible, aux souches circulant dans l’hémisphère opposé.
11.1.3 Coronavirus, SRAS et MERS-CoV 30
Les coronavirus sont ubiquitaires et peuvent infecter aussi bien les animaux que les humains. Ils causent en général des maladies des voies respiratoires supérieures d’intensité faible à modérée. Le SRAS, en 2003, avait pour origine un coronavirus.
Depuis avril 2012, et au 1er avril 2015, des cas de MERS-CoV ont été rapportés dans 23 pays : Arabie saoudite, Qatar, Jordanie, Émirats arabes unis, Oman, Koweït, Yémen, Liban, Iran, Royaume-Uni, France, Tunisie, Italie, Malaisie, Philippines, Grèce, Egypte, USA, Pays-Bas, Algérie, Autriche, Turquie et Allemagne. Tous les cas européens et celui d’Afrique du Nord ont eu un contact direct ou indirect avec la péninsule arabique. Cependant, des cas de transmission interhumaine, locale et limitée, parmi les contacts étroits des cas (n’ayant pas voyagé au Moyen-Orient) ont été observés en France, en Italie, en Tunisie et au Royaume-Uni. Au 1er avril 2015, l’OMS a rapporté 1 090 cas confirmés de MERS-CoV, dont 412 décès (létalité observée : 38%). La source de contamination liée à une infection à MERS-CoV ainsi que le mode de transmission restent à l’heure actuelle encore mal connus. Il n’existe ni vaccin, ni traitement spécifique face à ce virus émergent. Bien que l’importation de cas de MERS-CoV au sein de l’Union européenne reste possible, le risque de transmission soutenue d’humain à humain en Europe et en France est considéré comme faible.
11.2 BMR / BHRe
Les BHRe (bactéries hautement résistantes et émergentes) font l’objet de recommandations spécifiques qui ont été revues en 2011 par le HCSP, avec une incitation à un dépistage systématique à l’hôpital de tout patient ayant été hospitalisé à l’étranger dans l’année qui précède son hospitalisation en France (8). Les plus courantes et liées à un séjour à l’étranger, pour la France, sont les entérobactéries productrices de carbapénémases (EPC) et les entérocoques résistants aux glycopeptides (ERG).
11.2.1 Entérobactéries productrices de carbapénémases (EPC)
Les entérobactéries sont des bacilles Gram négatifs constituant l’une des plus importantes familles de bactéries : elles sont de plus en plus résistantes aux antibiotiques. Les carbapénèmases conduisent ainsi à une inefficacité partielle ou totale des antibiotiques de la classe des carbapénèmes (imipénème, méropénème et ertapénème), considérés comme des traitements de dernier recours. Les EPC restent rares en France en comparaison avec d’autres pays, mais une augmentation des épisodes impliquant des EPC signalés à l’InVS est observée depuis 2009. Cette augmentation invite à la plus grande vigilance. Le rôle du tourisme médical, décrit notamment comme facteur d’introduction du mécanisme NDM (New Delhi metallo-ß-lactamase) en Angleterre chez des patients colonisés/infectés ayant subi des hospitalisations récentes dans le sous-continent Indien, est majeur et préoccupant. Étant donné la circulation des EPC dans de nombreux pays étrangers, le rôle du voyage et de l’hospitalisation à l’étranger est parfaitement démontré sur les données françaises notamment (9).
11.2.2 Entérocoques : Enterococcus faecium résistant aux glycopeptides (ERG)
Des entérocoques résistants aux antibiotiques, comme la vancomycine et la teicoplanine, ont émergé au milieu des années 1980 (10) : ils sont appelés entérocoques résistants aux glycopeptides (ERG). La plupart des ERG sont des E. faecium. Au niveau européen, l’Irlande est le pays qui a signalé le plus d’ERG en 2012, suivie par la République tchèque, le Royaume-Uni, l’Allemagne, la Grèce et le Portugal. En France, les signalements ont été en augmentation jusqu’en 2008, puis en diminution à compter de 2009 et stables depuis 2010. Le taux de résistance dans l’espèce, selon les données EARS-Net, reste inférieur ou proche de 1% : l’émergence est à ce jour contrôlée mais les efforts doivent se poursuivre.
11.2.3 Risque d’importation de SARM
Les voyageurs peuvent aussi être à risque d’infections par des Staphylococcus aureus résistants à la méticilline (SARM) ou avec un profil inhabituel de résistance aux antibiotiques. Il est donc recommandé de prélever les patients avec des infections cutanées présumées staphylococciques (impétigo, folliculite, furoncle, abcès) pour établir un antibiogramme. L’antibiothérapie empirique devrait aussi prendre en compte le risque de SARM voire d’autres résistances. Ces voyageurs devraient être identifiés pour prévenir une diffusion de ces souches résistantes dans la communauté 31.
Le risque de portage de Staphylococcus aureus porteur de la leucocidine de Panton-Valentine (LPV) est aussi à prendre en compte. De tels Staphylococcus aureus sont source d’infections plus sévères et peuvent se transmettre plus facilement dans l’environnement familial et communautaire 32.
11.3 Tuberculoses résistantes
Pour la plupart des voyageurs, le risque de développer une infection tuberculeuse latente ou une tuberculose active est faible. Cependant, un voyage pour visite familiale ou à des amis dans un pays où l’incidence de tuberculose est élevée, peut constituer un risque 33. Le risque de tuberculose maladie est plus élevé chez les voyageurs qui ont déjà été atteints d’une tuberculose active ou qui ont été en contact étroit avec des personnes atteintes d’une tuberculose active ou soupçonnées de l’être. Les voyageurs immunodéprimés (personnes infectées par le VIH, personnes traitées par des stéroïdes et celles atteintes de diabète), les personnes sous anti-TNF et les enfants âgés de moins de 5 ans courent aussi un plus grand risque de voir leur infection tuberculeuse évoluer vers la tuberculose active. De plus en plus de patients sont infectés par des souches de Mycobacterium tuberculosis résistantes, soit multi-résistantes de type MDR (Multi Drug Resistant) soit ultrarésistantes de type XDR (Extensively Drug Resistant).
Les zones géographiques à forte incidence tuberculeuse, selon les estimations de l’OMS et en tenant compte de certaines imprécisions liées aux difficultés du recueil fiable des données épidémiologiques dans certains pays, sont :
- le continent africain dans son ensemble ;
- le continent asiatique dans son ensemble, y compris les pays du Proche et du Moyen-Orient ;
- les pays d’Amérique centrale et du Sud ;
- les pays d’Europe centrale et de l’Est, y compris les pays de l’ex-URSS ;
- dans l’Union européenne : Bulgarie, Estonie, Hongrie, Lettonie, Lituanie, Pologne, Portugal et Roumanie.
Tuberculose : comment signaler
La tuberculose étant une maladie à déclaration obligatoire depuis 1964, les médecins ou hôpitaux doivent la notifier à l’Agence régionale de santé (ARS) de leur région. Les fiches de déclaration sont transmises par les déclarants (cliniciens ou laboratoires) à l’ARS de leur région (http://www.ars.sante.fr/portail.0.html) qui partage les informations avec les Clat (Centres de lutte antituberculeuse) afin que les investigations autour des cas puissent être menées.
11.4 Arboviroses : Chikungunya, Dengue, Zika
11.4.1 Chikungunya & Dengue
La dengue et le chikungunya représentent une part importante des épisodes fébriles dans les problèmes de santé au retour de voyage, hors paludisme.
Depuis son identification dans les années 1950 et jusqu’en 2005, l’infection à chikungunya était restée peu documentée. L’importante épidémie des années 2005-2006 qui a affecté l’Océan Indien a permis de mettre en évidence des formes graves jusque-là méconnues, notamment chez des nouveau-nés infectés en per partum, et a révélé la fréquence des séquelles articulaires parfois invalidantes. Depuis décembre 2013, une épidémie de chikungunya sévit dans les Caraïbes et en Guyane et s’est propagée sur le continent américain (pour la première fois, du chikungunya est rapporté dans cette zone géographique), puis dans certaines îles du Pacifique (Polynésie française, Kiribati, Îles Cook, Samoa…) (Carte 5). Ces épidémies confirment le potentiel de diffusion de la maladie par les voyageurs dans des populations non immunes et l’adaptation du virus à son environnement.
La dengue est l’arbovirose qui se développe le plus tant en nombre de cas qu’en dispersion spatiale (Cf. chapitre 3.1.2).
Le risque d’introduction et d’implantation est particulièrement important dans des zones jusque-là indemnes où un des vecteurs potentiels est présent. C’est notamment le cas en Europe et dans le sud de la France.
Ainsi, dès 2006 en France métropolitaine, afin de prévenir et limiter la circulation de ces virus, le ministère de la Santé a mis en place un dispositif de lutte contre le risque de dissémination de la dengue et du chikungunya en France métropolitaine. Ce dispositif est établi en lien avec les ARS, les conseils généraux et les communes concernés, ainsi que les agences nationales de santé et les structures chargées de la surveillance entomologique et de la démoustication.
Ce dispositif, actualisé chaque année, instaure :
- une surveillance entomologique (c’est-à-dire des populations de moustiques), renforcée à partir du 1er mai dans les zones où le moustique est présent ou susceptible de s’implanter. Cette surveillance vise à détecter l’activité du moustique afin d’agir le plus précocement possible pour ralentir la progression de son implantation géographique ;
- une sensibilisation des personnes résidant dans les zones où le moustique est présent et actif, afin de détruire autour et dans leur habitat toutes les sources d’eaux stagnantes, gîtes potentiels de reproduction des moustiques. Des actions d’information et de communication sont menées tout au long de la période estivale par les ARS, en lien avec les conseils généraux et les communes concernés ;
- une surveillance des cas humains, renforcée à partir du 1er mai : un dispositif de signalement accéléré est mis en place du 1er mai au 30 novembre dans les départements où le moustique Aedes albopictus est implanté (11). Ce dispositif de surveillance épidémiologique renforcé est lié à la période d’activité du moustique (mai à novembre). Toute personne de retour de voyage d’une zone endémique (moins de 15 jours) et présentant au moins un des symptômes de dengue ou de chikungunya (cf. encadré ci-après) doit être signalée à l’ARS et faire l’objet d’une demande de confirmation biologique en utilisant la fiche de signalement, téléchargeable sur le site de l’InVS. Cette procédure permet l’intervention rapide des services de lutte antivectorielle autour des cas suspects afin d’éviter la transmission du virus. Sans attendre la confirmation biologique, il doit être conseillé aux cas suspects de se protéger de toute piqûre de moustique (répulsif, moustiquaire etc.) et de rester autant que possible à domicile pour éviter la mise en place d’une chaîne de transmission de la maladie.
Chikungunya et Dengue de retour de voyage, quand y penser ?
- Tout cas de chikungunya (importé) défini par la mise en évidence d’une fièvre supérieure à 38,5°C d’apparition brutale et de douleurs articulaires invalidantes et consécutives à un voyage en zone endémique dans les 15 jours précédant les signes.
- Tout cas de dengue (importé) défini par la mise en évidence d’une fièvre supérieure à 38,5°C d’apparition brutale, d’au moins un signe algique (céphalées, arthralgies, myalgies, lombalgies, douleur rétro-orbitaire) consécutifs à un voyage en zone endémique dans les 15 jours précédant les signes.
11.4.2 Zika (12)
Le virus Zika (ZIKV) est un arbovirus, flavivirus de la même famille que la dengue et la fièvre jaune. Les formes asymptomatiques sont fréquentes (13) et, quand les symptômes sont présents, la présentation clinique est de type syndrome dengue-like associant, à des degrés divers, des arthralgies, des œdèmes des extrémités, une fièvre modérée, des céphalées, des douleurs rétro-orbitaires, une hyperhémie conjonctivale et des exanthèmes maculo-papuleux. Les signes persistent généralement de 2 à 5 jours. La transmission est essentiellement vectorielle (moustiques Aedes) et le réservoir n’est pas encore formellement identifié. En 2007, ZIKV a été responsable d’une épidémie sur les îles de Yap (Micronésie) 34. Le virus Zika est considéré comme émergent depuis 2007. Le virus Zika a été responsable d’une épidémie majeure en Polynésie française qui a débuté en octobre 2013) (13), suivie d’une épidémie en Nouvelle-Calédonie, en janvier 2014) et de cas sporadiques sur les Îles de Pâques et Cook dans le Pacifique, puis en 2015 à nouveau en Nouvelle-Calédonie, aux Îles Salomon et au Vanuatu. Des cas ont été exportés au Japon, en Norvège, en Australie et en France. L’infection à virus Zika est à l’origine, en moins d’une décennie, de deux épidémies majeures dans le Pacifique, dans des territoires préalablement naïfs. Cette arbovirose émergente transmise par les moustiques du genre Aedes, avec des cas importés dans d’autres pays indemnes, est à haut potentiel de diffusion dans les pays où le vecteur est présent. Pour les voyageurs, actuellement, il n’existe pas de traitement spécifique ni de vaccin. Le traitement est symptomatique et la prévention de l’infection passe par la protection contre les piqûres de moustiques (répulsifs, moustiquaire, etc., Cf. tableau 10).
En cas de suspicion, contactez votre ARS.
11.5 FHV Ebola
Le 22 mars 2014, le ministère de la Santé guinéen a notifié à l’OMS une épidémie de fièvre hémorragique virale (FHV) liée au virus Ebola, souche « Zaïre », dans le sud de la Guinée. Fin mars, l’épidémie s’est propagée au Liberia et en Sierra Leone voisins, puis au Nigeria en août et au Mali fin octobre 2014. C’est la première fois que des cas de FHV liés à Ebola sont rapportés dans ces pays d’Afrique de l’Ouest. Des cas sporadiques avaient été rapportés en Côte d’Ivoire en 1994 mais cette FHV est généralement rapportée en Afrique centrale (14). L’épidémie actuelle est sans précédent, tant du point de vue du nombre de cas rapportés que de son étendue géographique et de la transmission avérée en zones urbaines et dans des capitales. Au 1er avril, l’OMS a colligé un total de 24 872 cas (suspects, probables et confirmés), dont 10 311 décès dans les trois pays actuellement affectés en Afrique de l’Ouest (Guinée, Liberia et Sierra Leone). Le personnel de santé a payé un lourd tribut dans cette lutte contre le virus Ebola.
Le risque d’importation du virus Ebola par le biais des voyageurs (hors pays d’Afrique de l’Ouest frontaliers ou proches) est faible mais ne peut être totalement exclu. Des cas d’Ebola ont été diagnostiqués au Sénégal, en Espagne, au Royaume-Uni et aux USA : ces cas, directement importés des pays affectés en Afrique de l’Ouest, ont donné lieu à des cas de transmissions secondaires en Espagne et aux USA. Enfin, au 1er avril 2015, 33 cas d’Ebola ont été rapatriés dont 13 vers l’Europe (trois en Allemagne, deux en Espagne, en France et au Royaume-Uni, un en Norvège, en Italie, aux Pays Bas et en Suisse).
Depuis le début de l’épidémie, une surveillance renforcée a été mise en place en France. Son objectif est d’identifier au plus tôt un éventuel cas importé afin, d’une part, d’assurer la meilleure prise en charge possible du malade et, d’autre part, de mettre en œuvre la prévention de la transmission du virus, tout en maintenant un haut degré de sécurité pour les soignants.
Il est important de rappeler que, dans la région ouest africaine, d’autres pathologies endémiques telles que le paludisme ou d’autres virus responsables de FHV circulent (FHV de Lassa ou la fièvre jaune) et peuvent compliquer le diagnostic.
Pour toute personne revenant d’une zone d’épidémie, se référer à l’Avis du HCSP du 24 octobre 2014 35.
11.6 Rage (Cf. chapitre 6.8.2)
La quasi-totalité des cas de rage survenus en France ces dernières années était la conséquence de l’importation clandestine illégale de jeunes chiens et chats. Une des dernières alertes, liée à l’importation illégale d’un chiot depuis le Maroc, remonte à 2004 dans la région de Bordeaux. Elle a entrainé le traitement post-exposition de 187 personnes en contact avec cet animal. Aucun cas de rage humaine n’a été déclaré sur le territoire français après cette alerte.
L’importation d’animaux domestiques ou sauvages est strictement interdite en France (sanctions pénales et financières lourdes), sauf s’ils répondent aux conditions réglementaires d’importation (espèces dont le commerce est autorisé, statut sanitaire et vaccinal faisant l’objet d’un certificat officiel).
Tout animal rapporté en France sans certificat officiel doit être immédiatement signalé aux services vétérinaires.
Rage : comment signaler
La rage justifie une intervention urgente locale, nationale ou internationale. Les médecins et les biologistes qui suspectent ou diagnostiquent une rage doivent le signaler sans délai et par tout moyen approprié (téléphone, télécopie) au médecin de l’Agence régionale de santé (ARS) de leur lieu d’exercice. (http://www.ars.sante.fr/portail.0.html)
Le signalement permet au médecin de l’ARS de mettre en place les mesures de prévention individuelle et collective autour des cas et, le cas échéant, de déclencher des investigations pour identifier l’origine de la contamination et agir pour la réduire.
La notification intervient après le signalement et le plus souvent après confirmation du diagnostic. Les médecins ou les biologistes déclarants notifient le cas au médecin de l’ARS du lieu d’exercice au moyen d’une fiche spécifique à chaque maladie.
11.7 Punaises de lit
Les punaises de lit, Cimex lectularius (commun) et hemipterus (tropical), famille des Cimicidae, sont des petits insectes ubiquitaires de couleur brun-rouge, environ de la taille d’un pépin de pomme aplati (de 4 à 7 mm de longueur) qui s’infiltrent à peu près partout dans l’environnement humain. Leur repas sanguin dure de 3 à 5 minutes tous les trois jours, et elles peuvent piquer plusieurs fois en une nuit : les lésions cutanées les plus caractéristiques se présentent sous forme de maculo-papules érythémateuses et prurigineuses de 5 mm à 2 cm de diamètre avec un point hémorragique central, localisées au niveau des bras, des jambes et du cou 36. La punaise peut être véhiculée facilement en se camouflant dans les vêtements, les bagages et autres articles personnels, si bien que le voyageur international pourra transmettre sa nuisance de retour dans son pays (transport passif). Les endroits où les voyageurs courent le plus grand risque sont ceux où la rotation de personnes est élevée : autobus, trains, avions mais aussi hôtels, même de luxe, complexes touristiques, bateaux de croisière…
À ce jour, il n’a pas été décrit de transmission de maladies infectieuses par l’intermédiaire de ces punaises ; des surinfections bactériennes, notamment par grattage avec des mains contaminées, ne peuvent cependant pas être exclues. Par ailleurs, l’infestation du domicile par les punaises de lit peut être source de troubles psychologiques phobiques variés.
En cas de doute (piqûres lors du voyage, traces suspectes dans les bagages et effets personnels), éviter les infestations domiciliaires de punaises des lits au retour :
- isoler tous les bagages, les effets personnels (brosse à cheveux, trousse de maquillage, etc.) dans des sacs en plastique, sur une surface carrelée, loin de tout endroit que les punaises pourraient coloniser (zone de sommeil) ;
- un traitement systématique devra être entrepris, mécanique (aspirateur, congélation à -20°C au minimum pendant 48h selon la taille de l’objet) associé à un traitement chimique (perméthrine) ; laver l’ensemble des vêtements à 60°C au moins ou recourir au nettoyage vapeur à 120°C, qui détruit tous les stades de punaises, au niveau des recoins ou des tissus d’ameublement.
En cas de difficulté, s’adresser à la mairie ou à un professionnel spécialisé.
POUR EN SAVOIR PLUS
• Les centres de vaccination contre la fièvre jaune
- Envoi de la liste sur demande au Bureau des risques infectieux et de la politique vaccinale, Direction générale de la santé, 14 avenue Duquesne, 75350 PARIS 07 SP.
- Les coordonnées de ces Centres de vaccination anti-amarile sont également consultables et téléchargeables sur le site Internet du ministère en charge de la Santé, rubrique « Les dossiers de la santé de A à Z », Vaccinations / Informations sur les vaccins / Où se faire vacciner : http://www.sante.gouv.fr/IMG/pdf/TABLEAU_DES_CVFJ_MAJ_28_mars_2014.pdf
• Guide des vaccinations 2012
Téléchargeable sur le site de l’Institut national de prévention et d’éducation à la santé (Inpes) : http://www.inpes.fr/10000/themes/vaccination/guide-vaccination-2012/index.asp
• Les services de maladies infectieuses et tropicales ainsi que les laboratoires de parasitologie des CHU et CHR.
• Les sites Internet
- Ministère des Affaires sociales et de la Santé http://www.sante.gouv.fr/recommandations-sanitaires-aux-voyageurs.html
- Ministère des Affaires étrangères ; site « conseil aux voyageurs » : http://www.diplomatie.gouv.fr/fr/conseils-aux-voyageurs_909/index.html
- Cimed (Comité d’informations médicales) http://www.cimed.org
- Institut Pasteur (Centre médical) http://cmip.pasteur.fr
- Institut de veille sanitaire (InVS) http://www.invs.sante.fr/Dossiers-thematiques/Populations-et-sante/Voyageur-s-Recommandations-sanitaires-aux-voyageurs
- Organisation mondiale de la santé (OMS) http://www.who.int/ith
- Centers for Disease Control and Prevention (CDC), USA http://www.cdc.gov/travel
Références
/2008/9789242580419_fre.pdf
avisrapportsdomaine?clefr=372
Publications-et-outils/Points-epidemiologiques/Tous-les-numeros/International/Virus-Zika-en-Polynesie-2013-2014-et-ile-de-Yap-Micronesie-2007-Janvier-2014